
| 催化剂 |

| △c |
| △t |
| 0.1mol/L |
| 2s |
| 1 |
| 2 |
| 1 |
| 2 |
| ||
| 10-14 | ||
|


科目:高中化学 来源: 题型:
| A、简单氢化物的热稳定性:Y>X |
| B、简单离子的半径:Z>X>Y |
| C、Z的最高价氧化物对应水化物既能与强酸反应又能与强碱反应生产盐和水 |
| D、由Y、W、Q三种元素形成的某种化合物,可用于检查司机酒后驾车 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ||||||
| ③ | ④ | ⑤ | ⑥ | ⑦ |
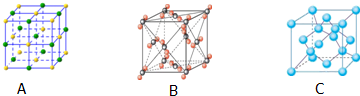
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
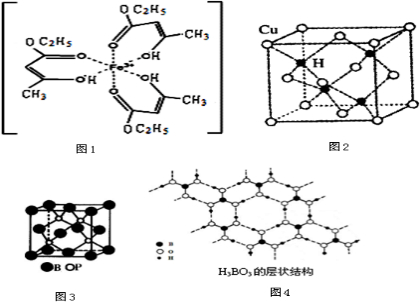
查看答案和解析>>
科目:高中化学 来源: 题型:
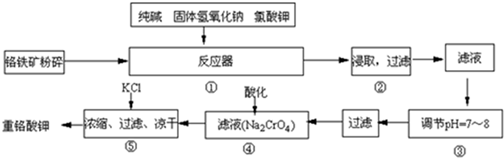
Ⅲ x |
Ⅲ (2-x) |
查看答案和解析>>
科目:高中化学 来源: 题型:
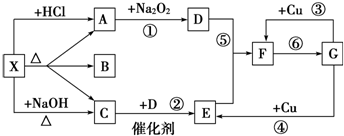
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com