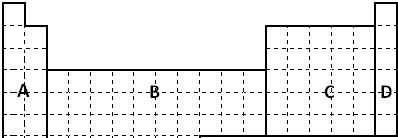
不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.
Ⅰ.氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图1所示.
(1)此配合物中,铁离子的价电子排布式为
.
(2)此配合物的-C
2H
5中C-H间形成化学键的原子轨道分别是
;
.
Ⅱ、(1)已知CrO
5中Cr为+6价,则CrO
5的结构式为
.
(2)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)
n,与Ni(CO)
n中配体互为等电子体的离子的化学式为
(写出一个即可).
(3)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途.已知CuH晶体结构单元如图2所示.该化合物的密度为ρg/cm
3,阿伏加德罗常数的值为N
A,则该晶胞中Cu原子与H原子之间的最短距离为
cm(用含ρ和N
A的式子表示).
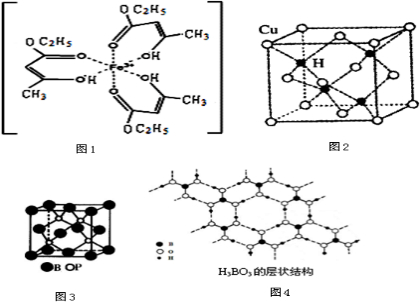
Ⅲ、硼元素在化学中有很重要的地位,硼及其化合物广泛应用于永磁材料、超导材料、富燃料材料、复合材料等高新材料领域应用.
(1)三氟化硼在常温常压下为具有刺鼻恶臭和强刺激性的无色有毒腐蚀性气体,其分子的立体构型为,B原子的杂化类型为
.
(2)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层.如图3示意的是磷化硼的晶体结构单元,则磷化硼的化学式为,微粒间存在的作用力为
.
(3)正硼酸(H
3BO
3)是一种片层状结构白色晶体,层内的H
3BO
3分子间通过氢键相连(如图4).
①1mol H
3BO
3的晶体中有
mol氢键.
②硼酸溶于水应生成弱电解质一水合硼酸H
2O?B(OH)
3,它电离生成少量[B(OH)
4]
-和的H
+离子.则硼酸为元酸,[B(OH)
4]
-含有的化学键类型为
.


 ,
, ;
;

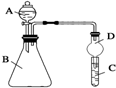 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.