
����Ŀ��(1)����������ȷ����____________________
A�����й��ۼ��Ļ�����һ���ǹ��ۻ�����
B�����ѷ��ֵ�����Ԫ�صĵ����ڳ��³�ѹ�¶�������
C������A��Ԫ�ص�ԭ�ӣ���뾶Խ��Խ���õ�����
D����n����Ԫ����������������ʽΪR2On���⻯�����ʽΪRHn (n��4)
E����������Ԫ����������ϼ۵�������������
F��ϡ������ԭ����ͬ����I A����A��Ԫ�صļ������Ӿ�����ͬ�ĺ�������Ų�
G�����ۻ������в����ܺ������Ӽ�
H��ֻ�зǽ���ԭ�Ӽ�����γɹ��ۼ�
I���ǽ���ԭ�Ӽ䲻�����γ����ӻ�����
(2)д���������ʵĵ���ʽ
MgBr2 ___________________ CCl4_______________HClO_______________
N2 ___________________ NH4Cl_______________NH3_______________
���𰸡�BG ![]()
![]()
![]()
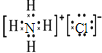
![]()
��������
��1��A�����й��ۼ��Ļ����ﲻһ���ǹ��ۻ����Ҳ���������ӻ������NaOH����A����
B��ϡ��������Ӽ�������С�����ѷ��ֵ�����Ԫ�صĵ����ڳ��³�ѹ�¶������壬��B��ȷ��
C���ڢ�A��Ԫ�ص�ԭ�ӣ���뾶Խ�˶Ե��ӵ�����ԽС��Խ�ѵõ����ӣ���C����
D����n����Ԫ��������������Ӧ�Ļ�ѧʽΪR2On����������ϼ�Ϊ+n�����������Ϊ-��8-n���������⻯�ﻯѧʽΪRH��8-n����n��4����H��8-n��R����D����
E����������Ԫ�أ��������=��������������Ԫ�ء���Ԫ��һ��û�������ϼۣ�����E����
F��ϡ������Heԭ����ͬ����H��������H+�ĺ�������Ų���ͬ����F����
G�����ݹ��ۻ�����Ķ��壬���ۻ������в����ܺ������Ӽ�����G��ȷ��
H�������ǽ���ԭ�Ӽ�Ҳ�����γɹ��ۼ�����AlCl3����H����
I���ǽ���ԭ�Ӽ�����γ����ӻ������NH4Cl����I����
��ѡBG��
��2��MgBr2Ϊ���ӻ������������Ҫ����������ӣ�![]() ��
��
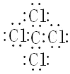
CCl4 �ǹ��ۻ����C���м䣬��Χ8�����ӣ�Clԭ�������ܣ�ÿ����ԭ����ΧҲ��8�����ӣ�ÿ��Clԭ�Ӷ���C�����������ӣ��������Ȼ�̼�ĵ���ʽ
HClOΪ���ۻ���������д���1���������1��Cl-O����������ĵ���ʽΪ��![]() ��
��
N2 ��Nԭ�������Ϊ5�����ӣ�����Nԭ�Ӽ��γ��������õ��Ӷԣ������ĵ���ʽΪ��![]() ��
��
NH4Cl�Ȼ��Ϊ���ӻ��������ʽ����Ҫ�����������������ɣ��Ȼ�淋ĵ���ʽΪ��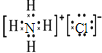 ��
��
NH3����Ϊ���ۻ���������д���3�����������ԭ�������ﵽ8�����ȶ��ṹ�������ĵ���ʽΪ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�NOx��CO2���������ã��Դٽ���̼���Ĺ����ͻ����ı���������Ҫ���塣
(1)��֪C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) ��H=a kJ��mol-1
N2(g)+O2(g)=2NO(g) ��H=b kJ��mol-1
H2O(l)=H2O(g) ��H=c kJ��mol-1
��C2H4(g)+6NO(g)![]() 3N2(g)+2CO2(g)+2H2O(l)�ķ�Ӧ����H=______��
3N2(g)+2CO2(g)+2H2O(l)�ķ�Ӧ����H=______��
(2)��NH3����ԭNOx�������������������Ⱦ������ͼ������NH3����ԭ����������һ��������ͨ�����ֲ�ͬ�����������ݳ������е������ﺬ�����Ӷ�ȷ�������ѵ��ʣ��ѵ��ʼ����������ת���ʣ�����Ӧԭ��Ϊ��NO(g)+NO2(g)+2NH3(g)![]() 2N2(g)+3H2O(g) ��H<0��
2N2(g)+3H2O(g) ��H<0��

����˵����ȷ����______��
A.�����١��ڷֱ��ʺ���250���450�������ѵ�
B.ʹ�õڢ��ִ��������������NOx��ƽ��ת����
C.��ͬ�����£��ı�ѹǿ���ѵ���û��Ӱ��
D.�ڽ����A��������ʹ�����ִ�����������Ӧ��δ��ƽ�⡣
(3)��ҵ�ϳ����صķ�Ӧ���£�2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(l) ��H<0���ں㶨�¶��£���NH3��CO2��2��1�����ʵ���֮�ȳ���һ���Ϊ10L���ܱ������У���������������䣬�������������Բ��ƣ�����20min�ﵽƽ�⣬�����ʵ�Ũ�ȱ仯������ͼ��ʾ��
CO(NH2)2(l)+H2O(l) ��H<0���ں㶨�¶��£���NH3��CO2��2��1�����ʵ���֮�ȳ���һ���Ϊ10L���ܱ������У���������������䣬�������������Բ��ƣ�����20min�ﵽƽ�⣬�����ʵ�Ũ�ȱ仯������ͼ��ʾ��
��������ƽ��ʱ���¶Ⱥ�ѹǿ���䣬���������г���3mol��CO2�����ʱv������______v���棩����>��<��=�����жϵ�������______��
��������ƽ��ʱ���¶Ⱥ�������䣬25minʱ���������г���2mol��NH3��1 mol CO2����40minʱ���´ﵽƽ�⣬����ͼ�л���25~50min��NH3��Ũ�ȱ仯���ߡ�______��

(4)���������������ٷŵ������Ӷ��ε������ԭ��������ͼ��ʾ(EMI+Ϊ�л������ӡ���ع���ʱ����Һ�����������)���õ�طŵ�ʱ�ĸ�����Ӧ����ʽΪ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ṥҵ�����У�Ϊ��������SO2��ת�������ܳ���������ܣ��������м����Ƚ������ĽӴ��ң�����ͼ��������˵���������
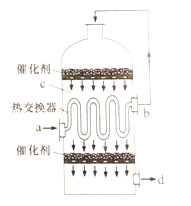
A. a��b�����Ļ������ɷֺ�����ͬ���¶Ȳ�ͬ
B. c��d�����Ļ������ɷֺ�����ͬ���¶Ȳ�ͬ
C. �Ƚ�������������Ԥ�ȴ���Ӧ�����壬��ȴ��Ӧ�������
D. c�����徭�Ƚ������ٴδ�������Ŀ�������SO2��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯����(������Һ)��ת����ϵ����֪�ڳ��³�ѹ�£�A�ǹ��壬B��C��D��E�Ƿǽ��������Ҷ������壬C�ʻ���ɫ��������F�ǵ���ɫ���壬������G����ɫ��ӦΪ��ɫ����������Jͨ��״���³���̬��D��E��Ӧ����һ�ִ̼�����ζ�����塣
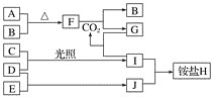
��ش��������⣺
(1)E��J�Ļ�ѧʽ�ֱ���________��________��
(2)д��F��CO2��Ӧ�Ļ�ѧ����ʽ���õ����ŷ���ʾ����ת�Ƶ������_________��
(3)����������Cͨ��ʢ�е��۵⻯����Һ���Թ��У���Һ����ɫ���÷�Ӧ�����ӷ���ʽΪ_________��
(4)�����3.36 L����B��A��ȫ��Ӧ��ת�Ƶ��ӵ���ĿΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2����Ҫ���������壬Ҳ��һ�ֹ�ҵԭ�ϡ���������CO2�����ڻ�������ЧӦ�����Ļ������⡣
(1)�ҹ���ѧ��ͨ������һ�������ϴ������ɹ�ʵ����CO2ֱ�Ӽ�����ȡ������ֵ���͡�
��֪��2H2 (g)+O2 (g) =2H2O(l) ��H = -571.6 kJ/mol
2C8H18(l)+25O2(g) =16CO2(g)+18H2O(l) ��H = -11036 kJ/mol
25�桢101kPa�����£�CO2��H2��Ӧ��������(��C8H18��ʾ)��Һ̬ˮ���Ȼ�ѧ����ʽ��_________��
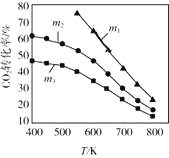
(2)CO2������ϳ��Ҵ��ķ�Ӧԭ���ǣ�2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) ��H =-173.6 kJ/molͼ����ʼͶ�ϲ�ͬʱ��CO2��ƽ��ת�������¶ȵı仯��ϵ��mΪ��ʼʱ��Ͷ�ϱȣ���m=
C2H5OH(g)+3H2O(g) ��H =-173.6 kJ/molͼ����ʼͶ�ϲ�ͬʱ��CO2��ƽ��ת�������¶ȵı仯��ϵ��mΪ��ʼʱ��Ͷ�ϱȣ���m=![]() ��m1��m2��m3Ͷ�ϱȴӴ�С��˳��Ϊ_________��������_________��
��m1��m2��m3Ͷ�ϱȴӴ�С��˳��Ϊ_________��������_________��
(3)��Cu/ZnO���������£���CO2��H2��Ͽɺϳɼ״���ͬʱ������������ƽ�з�Ӧ��
��Ӧ�� CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ��H1=-53.7 kJ/mol��
CH3OH(g)+H2O(g) ��H1=-53.7 kJ/mol��
��Ӧ�� CO2(g)+H2(g) ![]() CO(g)+H2O(g)�� ����H2=+41.2 kJ/mol
CO(g)+H2O(g)�� ����H2=+41.2 kJ/mol
����һ����CO2��H2��ʼͶ�ϱȣ�����ͬѹǿ��,������ͬ��Ӧʱ��������ʵ������(�������״�ѡ��������ָת����CO2�����ɼ״��İٷֱ�)��
ʵ����� | T/K | ���� | CO2ת����/% | �״�ѡ����/% |
ʵ��1 | 543 | Cu/ZnO���װ� | 12.3 | 42.3 |
ʵ��2 | 543 | Cu/ZnO����Ƭ | 10.9 | 72.7 |
ʵ��3 | 553 | Cu/ZnO���װ� | 15.3 | 39.1 |
ʵ��4 | 553 | Cu/ZnO����Ƭ | 12.0 | 71.6 |
�ٶԱ�ʵ��1��ʵ��3�ɷ��֣�ͬ�����������£��¶����ߣ�CO2ת�������ߣ� ���״���ѡ����ȴ���ͣ�����ͼ״�ѡ���Խ��͵Ŀ���ԭ��_______________��
�ڶԱ�ʵ��1��ʵ�� 2�ɷ��֣���ͬ���¶��£�����Cu/ZnO����ƬʹCO2ת���ʽ��ͣ� ���״���ѡ����ȴ��ߣ�����ͼ״���ѡ������ߵĿ���ԭ��____________��
�����������CO2ת��ΪCH3OHƽ��ת���ʵĴ�ʩ��_______��
a��ʹ��Cu/ZnO���װ�������
b��ʹ��Cu/ZnO����Ƭ������
c�����ͷ�Ӧ�¶�
d��Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ��
e������![]() �ij�ʼͶ�ϱ�
�ij�ʼͶ�ϱ�
(4)������������ĤΪ�����缫��ϡ����Ϊ�������Һ����һ��������ͨ��CO2����⣬���������Ƶõ��ܶȾ���ϩ![]() (���LDPE)��
(���LDPE)��
�ٵ��ʱ�������ĵ缫��Ӧʽ��_____________��
�ڹ�ҵ������1.4��104 kg ��LDPE����������Ҫ��״����______L ��CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ü۵��ӶԻ������ۣ�VSEPR������Ԥ��������ӻ����ӵĿռ乹�ͣ�Ҳ���Ʋ���Ǵ�С�������ж���ȷ���ǣ� ��
A.BF3��PCl3Ϊ������B.SO3��CO32-Ϊƽ��������
C.SO2���Ǵ���120oD.BF3�������η���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��̬���ڱ�״�����ܶ�Ϊ2.59 g��L��1��
(1)����Է�����������________��
(2)�����ĺ�̼��Ϊ82.8%���������̼����ԭ�ӵĸ�������________������ʽ��________��
(3)���ܵĽṹ��ʽ��������______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��2-���ȱ���(CH2C1CHClCH3)��һ����Ҫ�Ļ���ԭ�ϣ���ҵ�Ͽ��ñ�ϩ�ӳɷ��Ʊ�����Ҫ������Ϊ3-�ȱ�ϩ(CH2=CHCH2C1)����Ӧԭ��Ϊ��
I��CH2=CHCH3(g)+C12(g)![]() CH2C1CHC1CH3(g) ��H1=��134kJ��mol-1
CH2C1CHC1CH3(g) ��H1=��134kJ��mol-1
II��CH2=CHCH3(g)+C12(g)![]() CH2=CHCH2C1(g)+HC1(g)��H2=��102kJ��mol-1
CH2=CHCH2C1(g)+HC1(g)��H2=��102kJ��mol-1
��ش��������⣺
(1)��֪CH2=CHCH2C1(g)+HC1(g)![]() CH2C1CHC1CH3(g)�Ļ��Ea(��)Ϊ132kJ��mol-1����÷�Ӧ�Ļ��Ea(��)Ϊ______kJ��mol-1��
CH2C1CHC1CH3(g)�Ļ��Ea(��)Ϊ132kJ��mol-1����÷�Ӧ�Ļ��Ea(��)Ϊ______kJ��mol-1��
(2)һ���¶��£�������ܱ������г�������ʵ�����CH2=CHCH3(g)��C12(g)���ڴ��������·�����ӦI���������������ѹǿ��ʱ��ı仯���±���ʾ��
ʱ��/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
ѹǿ/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
���õ�λʱ���������ѹ�ı仯����ʾ��Ӧ���ʣ���![]() ����ǰ120min��ƽ����Ӧ����v(CH2C1CHC1CH3)=______kPa��min-1��(����С�����2λ)��
����ǰ120min��ƽ����Ӧ����v(CH2C1CHC1CH3)=______kPa��min-1��(����С�����2λ)��
�ڸ��¶��£���ƽ��ʱHC1���������Ϊ![]() �����ϩ��ƽ����ת����
�����ϩ��ƽ����ת����![]() _______����ӦI��ƽ�ⳣ��Kp=_____kPa-1(KpΪ�Է�ѹ��ʾ��ƽ�ⳣ��������С�����2λ)��
_______����ӦI��ƽ�ⳣ��Kp=_____kPa-1(KpΪ�Է�ѹ��ʾ��ƽ�ⳣ��������С�����2λ)��
(3)ij�о�С�����ܱ������г���һ������CH2=CHCH3��C12���ֱ���A��B���ֲ�ͬ���������·�����Ӧ��һ��ʱ�����CH2C1CHC1CH3�IJ������¶ȵĹ�ϵ����ͼ��ʾ��
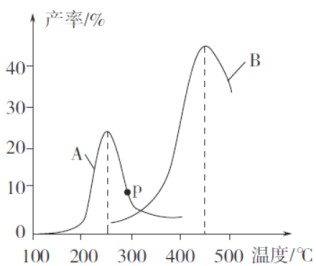
������˵���������___________(�����)��
a��ʹ�ô���A������¶�ԼΪ250��
b����ͬ�����£��ı�ѹǿ��Ӱ��CH2C1CHC1CH3�IJ���
c�����ִ������ܽ��ͷ�Ӧ�Ļ�ܣ�����H����
d�����CH2C1CHC1CH3��Ӧѡ���ԵĹؼ������ǿ����¶�
���ڴ���A�����£��¶ȵ���200��ʱ��CH2C1CHC1CH3�IJ������¶����߱仯������Ҫԭ����_______________________________________________________________��
��p���Ƿ�Ϊ��Ӧ�¶���CH2C1CHC1CH3��ƽ����ʣ��ж�������_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ��ij������N2��H2��Ӧ�����������仯������ͼ������������ȷ����( )
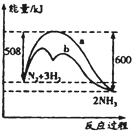
A. �÷�Ӧ���Ȼ�ѧ����ʽΪ��N2+3H2![]() 2NH3 ��H=��92kJ��mol-1
2NH3 ��H=��92kJ��mol-1
B. ����Ӧ�Ļ�ܴ����淴Ӧ�Ļ��
C. b�����Ǽ������ʱ�������仯����
D. ʹ�ô�����Ӧ���ʱ��С��N2ת��������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com