
下列说法正确的是
A.使用量筒量取一定体积的浓硫酸配制一定物质的量浓度的稀硫酸,将浓硫酸转移至烧杯后须用蒸馏水洗涤量筒,并将洗涤液一并转移至烧杯
B.现需使用480ml 0.1mol/L硫酸铜溶液,则使用容量瓶配制溶液需要 7.68g硫酸铜固体
C.使用托盘天平称量固体药品时左码右物,可能会导致所配溶液浓度偏低
D.容量瓶在使用前须用待配溶液润洗
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃,101 时:
时:


 则在25℃,101
则在25℃,101 时:
时: .
.
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:
已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值 (填“增大”、“减小”或“不变”);
②1100℃时测得高炉时, ,在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是 。
,在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是 。
③目前工业上可用 来生产燃料甲醇,有关反应为:
来生产燃料甲醇,有关反应为:
 。现向体积为1L的密闭容器中,充入1mol
。现向体积为1L的密闭容器中,充入1mol 和3mol
和3mol ,反应过程中测得
,反应过程中测得 和
和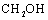 (g)的浓度随时间的变化如图所示。
(g)的浓度随时间的变化如图所示。
Ⅰ、从反应开始到平衡,氢气的平均反应速率 ;
;
Ⅱ、下列措施能使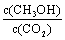 增大的是 (填符号)。
增大的是 (填符号)。
A.升高温度 B.再充入
C.再充入 D.将
D.将 (g)从体系中分离
(g)从体系中分离
E.充入He(g),使体系压强增大

查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组性质的比较中,不正确的是 ( )
A.碱性:NaOH>Mg(OH)2 B.热稳定性:NH3>PH3
C.失电子能力:K>Na D.原子半径:CI>S
查看答案和解析>>
科目:高中化学 来源: 题型:
现有X、Y、Z、W四种元素,其原子序数依次递增。已知有如下情况:
①X、Y、Z的单质在常温下均为气体。
② X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色。
③ XZ极易溶于水,在水溶液中电离出X+和Z-。XZ的水溶液可使石蕊试液变红。
④ 两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体。
⑤ Z的单质溶于X2Y中,所得溶液具有漂白作用。
⑥由Y、Z、W三种元素组成的化合物M受热催化分解,可制得元素Y的单质。
请完成下列问题:
(1)化合物M的化学式为 ▲ ,1molM中含有的电子的物质的量为 ▲ 。
(2)用化学方程式表示Z单质的实验室检验方法 ▲ 。
(3)写出Z的单质溶于X2Y中反应的化学方程式: ▲ ,若该反应中有2mol电子发生转移,则参加反应的Z单质在标况下的体积为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验对应的结论正确的是

A.①能组成Zn、Cu原电池
B.②能证明非金属性:S>C>Si
C.③说明反应2NO2 N2O4 △H>0
N2O4 △H>0
D.④ 白色沉淀为BaSO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.少量的钠通常保存在煤油中,少量白磷通常保存在水中
B.能使润湿的淀粉KI试纸变成蓝色的物质只能是氯气、臭氧、二氧化氮等气态物质
C.要将溶解在CCl4中的碘分离出来,可以用蒸馏法,因为碘易升华,先分离出来
D.某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
 把在空气中久置的镁条7.2g投入盛有500mL 0.5mol·L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题:
把在空气中久置的镁条7.2g投入盛有500mL 0.5mol·L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题:
(1)曲线由0→a段不产生氢气的原因 ,有关的离子方程式为 ;
(2)曲线由b→c段,产生氢气的速率逐渐增大的主要原因 ;
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因 。
(4) 在b到c这段时间内,收集到氢气VL(标准状况),则这段时间内用硫酸表示的
平均速率为 mol/(L·s)(假设反应前后溶液体积不变)。
(5) 对于足量镁条和100ml 2mol/L硫酸生成氢气的反应,下列措施能减缓反应速率,但又不影响生成氢气的总量的是 。
①加NaOH固体;②加BaCl2溶液;③加KNO3溶液;④加H2O;⑤加CH3COONa固体;⑥加小苏打溶液;⑦加少量CuSO4溶液;⑧加Na2SO4溶液;⑨将2 mol/L硫酸换成160mL 2.5mol/L的盐酸 ;⑩将镁条换成镁粉。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com