
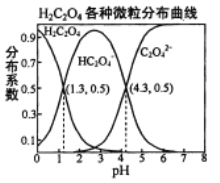
����Ŀ�������£�0.1 mol/L��H2C2O4��Һ��H2C2O4��HC2O4-��C2O42-��������ռ���ʵ����������ֲ�ϵ������pH�仯�Ĺ�ϵ����ͼ��ʾ�����б�������ȷ����
A. HC2O4-![]() H+��C2O42-��K��1��10-4.3
H+��C2O42-��K��1��10-4.3
B. �������ʵ�����NaHC2O4��Na2C2O4����ˮ����������ҺpHǡ��Ϊ4.3
C. ������HF��K��1��10-3.4��������H2C2O4��Һ���뵽����NaF��Һ���������ķ�ӦΪ��H2C2O4��F-��HF��HC2O4-
D. ��0.1 mol/L NaHC2O4��Һ����������Ũ�ȴ�С��ϵΪ��c(Na+)��c(HC2O4-)��c(H+)��c(C2O42-)��c(OH-)
���𰸡�B
��������
A����HC2O4-H++C2O42-����֪K=![]() ��pH=4.3ʱ��c(C2O42-)=c(HC2O4-)������K=c(H+)=1��10-4.3����A��ȷ��B���������ʵ�����NaHC2O4��Na2C2O4����ˮ�У�HC2O4-����̶ȴ���C2O42-��ˮ��̶ȣ�������Һ��c(C2O42-)��c(HC2O4-)������ҺpH����4.3����B����C������ͼ���A�ķ�����������H2C2O4��K1=10-1.3��K2=10-4.3��HF��K=1��10-3.45�������ԣ�H2C2O4��HF��HC2O4-�����Խ�����H2C2O4��Һ���뵽����NaF��Һ�У������ķ�ӦΪH2C2O4+F-=HF+HC2O4-����C��ȷ��D������ͼ��NaHC2O4��Һ�����ԣ���HC2O4-�ĵ���Ϊ��������Һ��HC2O4-���ֵ��룬�������Ũ�ȴ�С��ϵΪ��c(Na+)��c(HC2O4-)��c(H+)��c(C2O42-)��c(OH-)����D��ȷ����ѡB��
��pH=4.3ʱ��c(C2O42-)=c(HC2O4-)������K=c(H+)=1��10-4.3����A��ȷ��B���������ʵ�����NaHC2O4��Na2C2O4����ˮ�У�HC2O4-����̶ȴ���C2O42-��ˮ��̶ȣ�������Һ��c(C2O42-)��c(HC2O4-)������ҺpH����4.3����B����C������ͼ���A�ķ�����������H2C2O4��K1=10-1.3��K2=10-4.3��HF��K=1��10-3.45�������ԣ�H2C2O4��HF��HC2O4-�����Խ�����H2C2O4��Һ���뵽����NaF��Һ�У������ķ�ӦΪH2C2O4+F-=HF+HC2O4-����C��ȷ��D������ͼ��NaHC2O4��Һ�����ԣ���HC2O4-�ĵ���Ϊ��������Һ��HC2O4-���ֵ��룬�������Ũ�ȴ�С��ϵΪ��c(Na+)��c(HC2O4-)��c(H+)��c(C2O42-)��c(OH-)����D��ȷ����ѡB��


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������װ�ü��Լ���װһ��װ�ã�������������ȡ���������Cl2�����ռ���������֤�����Cl2�ͳ�ʪ��Cl2����Ư���ԡ������������������װ���������������� a ��i,j��g��f��e��d��b��c��h���Իش�

��1��Fװ���е��Լ�ӦΪ��_________��������_______________________��
��2��Aװ���е���Ҫ���������У��ƾ��ơ�Բ����ƿ��________________��
��3��Aװ���з�����Ӧ�Ļ�ѧ����ʽ��_______________________________��
��4��Eװ���з�����Ӧ�����ӷ�Ӧ����ʽ��_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����F��Cl��Br��I˳���������
A. ��Χ����B. ԭ�Ӱ뾶C. �縺��D. ��һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л��������У����ж�������ţ�
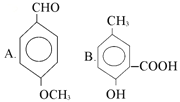
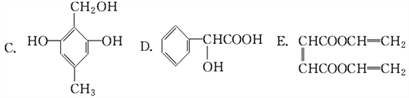
��1�����Կ���������ǣ������ţ���ͬ��________________��
��2�����Կ����������_________________��
��3�����Կ������������_________________��
��4�����Կ����������_________________��
��5�����Կ���ȩ�����_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������ܶ�Ϊ1.84 g/cm3�����ʵ���������Ϊ98 %�����ᣬ����250 mL���ʵ���Ũ��Ϊ0.46 mol/L�����ᡣ
(1)98 %��Ũ��������ʵ���Ũ��Ϊ_________��
(2)�������м��ֹ�����Ͳ��Ӧѡ��______������ţ���
��5 mL��Ͳ ��10 mL��Ͳ ��50 mL��Ͳ ��100 mL��Ͳ
(3)ʵ����Ҫ���²��裺
�ٶ��ݢ���ȡ��ҡ�Ȣ�ϴ�Ӣ�ת�Ƣ���ȴ�����װƿ��ϡ�ͽ���˳��Ϊ_______��
(4)���в���ʹ������Һ�����ʵ���Ũ��ƫ�ߵ���__________��
A��������ƿ��ת����Һʱ������Һ�彦��
B��δϴ��ϡ��ŨH2SO4��С�ձ�
C������ʱ���ӿ̶���
D��ϴ������ƿδ���T����������Һ
E�����ݺ�����ƿ������ҡ�ȣ����ú�Һ�治���̶��ߣ��ټ�ˮ���̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ������ͼװ�ý���ʵ�飬֤����ͭ��ϡ���ᷴӦ������NO��ʵ��ʱ������ע�����ڼ���һ������ϡ���ᣬ�ž�ע�����ڵĿ�����Ѹ�ٽ�����ͭ˿����Ƥñ���ϣ�һ��ʱ���ע����������ɫ���������

��1��ͭ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ_________________��
��2��NO�Ǵ�����Ⱦ��֮һ��Ŀǰ��һ��������������400�����ҡ��д������ڵ�����£��ð�����NO��ԭΪ������ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ4NH3+6NO![]() 5N2+6H2O��ÿ��5 mol N2���ɣ����������뻹ԭ��������ʵ���֮��Ϊ__________��
5N2+6H2O��ÿ��5 mol N2���ɣ����������뻹ԭ��������ʵ���֮��Ϊ__________��
��3����������ϡ���ỻ��Ũ���ᣬ�����ɵ�����ͨ��ˮ�У���������ˮ��Ӧ�Ļ�ѧ����ʽΪ______________________________________________��
��4����д��ʵ������NH4Cl��Ca(OH)2������ȡ�����Ļ�ѧ����ʽ__________��
��������Ȫʵ�飬����ˮ�м����̪���õ���ɫ��Ȫ����ʵ�������˰�����������Ҫ���ʷֱ���________________________��___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݱ�����2002��10��26�ն���˹���ֲ����ڽ������ʱ����ʹ���˷�����������̫ū�⣬��������һ���������ñ����ǿ100���ķ��飬��֪����Ļ�ѧʽΪC2HClBrF3����е㲻ͬ������������
A. 3��B. 4��C. 5��D. 6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CuƬ����0.1 mol��L1 FeCl3��Һ�У���Ӧһ��ʱ���ȡ��CuƬ����Һ��c(Fe3+)��c(Fe2+)��2��1����Cu2+��ԭ��Һ�е�Fe3+�����ʵ���֮��Ϊ(����)
A. 4��1 B. 1��4 C. 1��6 D. 6��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com