
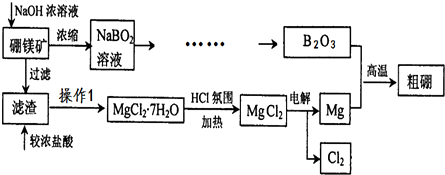

���� ��þ����Ҫ�ɷ�ΪMg2B2O5•H2O��������þ����ȡ����þ������Ĺ�����������þ�������������Ũ��Һ���˵õ��Ȼ�þ������Ũ�����ܽ�ͨ������Ũ���õ��Ȼ�þ�ᾧˮ������Ȼ��������м��ȵõ��Ȼ�þ���壬�����õ�þ��þ��B2O3�ڸ������������ɴ���
��1�����Ȼ�þ��Һ�л���Ȼ�þ�������ͨ������Ũ�������½ᾧ�ķ�����ã�
��2���Ȼ�þ��ˮ��Һ��ˮ������������þ��
��3����ˮ��Һ�����ԣ�ѡ����ʽ�ζ��ܣ��ζ��յ�ʱ����Һ�еĵ���ȫ��Ӧ��������Һ�е���ɫ�仯���ж��յ㣻���ݷ�Ӧ����ʽ���ζ����ݼ������������ĺ�����
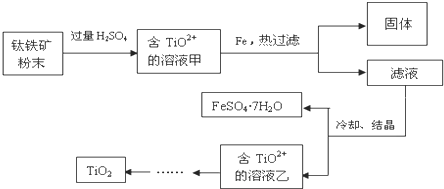
��4����֪TiO2+����ˮ���������ᣨH2TiO3������������Ԫ���غ�д����Ӧ�����ӷ���ʽ��
��5���ɹ�������ͼ��������Ϣ��֪��Ӧ��Ϊ�������������Ѻͽ�̿��������Ϊ���Ȼ��Ѻ�һ�ֿ�ȼ�����壬���ݷ�Ӧǰ��Ԫ������䣬��֪�˿�ȼ����������̼Ԫ�غ���Ԫ����ɵ�һ����̼��д����Ӧ�Ļ�ѧ����ʽ���ɣ������Ȼ�ѧ����ʽ��˹���ɼ���õ������Ȼ�ѧ����ʽ��
��� �⣺��þ����Ҫ�ɷ�ΪMg2B2O5•H2O��������þ����ȡ����þ������Ĺ�����������þ�������������Ũ��Һ���˵õ��Ȼ�þ������Ũ�����ܽ�ͨ������Ũ���õ��Ȼ�þ�ᾧˮ������Ȼ��������м��ȵõ��Ȼ�þ���壬�����õ�þ��þ��B2O3�ڸ������������ɴ���
��1�����Ȼ�þ��Һ�л���Ȼ�þ�������ͨ������Ũ�������½ᾧ�ķ�����ã��ʴ�Ϊ������Ũ�������½ᾧ��
��2��MgCl2•7H2O��Ҫ��HCl��Χ�м��ȣ���Ϊ�˷�ֹ�Ȼ�þˮ������������þ���ʴ�Ϊ����ֹMgCl2ˮ������Mg��OH��2��
��3����ˮ��Һ�����ԣ�ѡ����ʽ�ζ��ܣ��ζ��յ�ʱ����Һ�еĵ���ȫ��Ӧ�����Եζ��յ�ʱ������Ϊ�μ����һ��Na2S2O3��Һ����ƿ����ɫǡ����ȥ���Ұ���Ӳ��ָ�ԭɫ����������Ƶ����ʵ���Ϊ��0.30mol/L��0.018L=0.0054mol�����ݹ�ϵʽ��B��BI3��$\frac{3}{2}$I2��3S2O32-��n��B��=$\frac{1}{3}$n��S2O32-��=0.0018mol��
�������Ϊ��11g/mol��0.0018mol=0.0198g����������ĺ���Ϊ��$\frac{0.0198g}{0.02g}$��100%=99%��
�ʴ�Ϊ����ʽ���μ����һ��Na2S2O3��Һ����ƿ����ɫǡ����ȥ���Ұ���Ӳ��ָ�ԭɫ��99%��
��4����֪TiO2+����ˮ���������ᣨH2TiO3�������������ӣ������ӷ���ʽΪTiO2++2H2O�TH2TiO3��+2H+���ʴ�Ϊ��TiO2++2H2O�TH2TiO3��+2H+��
��5����Ӧ���ɹ�������ͼ��������Ϣ��֪��Ӧ��Ϊ�������������Ѻͽ�̿��������Ϊ���Ȼ��Ѻ�һ�ֿ�ȼ�����壬���ݷ�Ӧǰ��Ԫ������䣬��֪�˿�ȼ����������̼Ԫ�غ���Ԫ����ɵ�һ����̼����Ӧ�Ļ�ѧ����ʽΪ��2Cl2+TiO2+2C$\frac{\underline{\;����\;}}{\;}$TiCl4+2CO�����ݢ�Mg��s��+Cl2��g���TMgCl2��s����H=-641kJ•mol-1
��Cl2��g��+$\frac{1}{2}$Ti��s���T$\frac{1}{2}$TiCl4��l����H=-385kJ•mol-1���ɸ�˹���ɢ١�2-�ڡ�2���õ��Ȼ�ѧ����ʽΪ��2Mg��s��+TiCl4��l���T2MgCl2��s��+Ti��s����H=-512kJ/mol��
�ʴ�Ϊ��2Cl2+TiO2+2C$\frac{\underline{\;����\;}}{\;}$TiCl4+2CO��2Mg��s��+TiCl4��l���T2MgCl2��s��+Ti��s����H=-512kJ/mol��
���� ����������Ϣ�����⣬�漰���Ȼ�ѧ����ʽ����д������˹���ɵļ���Ӧ�ã����ص缫�жϺ͵缫��Ӧ��д�����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�


 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ���йظ����ʵ�˵������ȷ���ǣ�������
���йظ����ʵ�˵������ȷ���ǣ�������| A�� | ���ڷ����廯���� | |
| B�� | �ܷ�����ȥ��Ӧ��������Ӧ | |
| C�� | 1 mol���л���������NaOH��Һ��Ӧ������5 mol NaOH | |
| D�� | �ֱܷ������Na��NaHCO3��Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KSP��AB2��С��KSP��CD������AB2���ܽ��һ��С��CD���ܽ�� | |
| B�� | ���Ȼ����ij����ܽ�ƽ����ϵ�У���������ˮ���Ȼ�����KSP���� | |
| C�� | ���Ȼ����ij����ܽ�ƽ����ϵ�У�����⻯�ع��壬�Ȼ���������ת��Ϊ�⻯������ | |
| D�� | ��̼��Ƶij����ܽ�ƽ����ϵ�У�����ϡ���ᣬ�ܽ�ƽ�ⲻ�ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com