
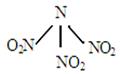
| A.分子中N、O原子间形成的共价键是非极性键 |
| B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 |
| D.分子中四个氮原子围成一个空间正四面体 |
科目:高中化学 来源:不详 题型:单选题
| A.硼电负性和硅相近 |
| B.π键是由两个p电子“头碰头”重叠形成的 |
| C.原子和其它原子形成共价键时,其共价键数一定等于原子的价电子数 |
| D.组成和结构相似的物质随相对分子质量的增大,熔沸点升高,所以NO的沸点应该介于N2和O2之间 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.P4和NO2都是共价化合物 |
| B.次氯酸的结构式为H-Cl-O |
| C.在CaO和SiO2晶体中,都不存在单个小分子 |
| D.CCl4和NH4Cl都是以共价键结合的分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙酸的沸点比甲酸甲酯高 |
| B.邻羟基苯甲酸的沸点比对羟基苯甲酸的沸点高 |
| C.HF是一种非常稳定的化合物,这是由于氢键所致 |
| D.冰中存在范德华力和氢键,而液态水中只存在范德华力 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分子晶体中范德华力没有方向性和饱和性,所以分子晶体一般都采取密堆积,但要受到分子形状的影响。 |
| B.由于共价键的方向性和饱和性,原子晶体堆积的紧密程度大大降低。 |
| C.配位数就是配位键的数目 |
| D.离子晶体一般都是非等径球的密堆积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子晶体的晶格能:Mg0> KCI> NaCl |
| B.“冰,水为之,而寒于水”说明相同质量的水和冰,冰的能量高 |
| C.对于反应2H202=2H20+02↑,加入Mn02或升高温度都能加快02的生成速率 |
| D.对羟基苯甲醛的沸点大于邻羟基苯甲醛,原因是后者分子之间存在氢键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.“墙内开花,墙外香”——分子在不断地运动 |
| B.湿衣服晾在有太阳的地方比晾在没有太阳的地方容易干——温度高分子的运动速度加快 |
| C.热胀冷缩——分子的大小随着温度的改变而改变 |
| D.水电解生成氢气和氧气——在化学变化中,分子分解成原子,原子又构成新的分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com