
【题目】短周期元素 X、Y、Z 组成的化合物 Y2X 和 ZX2。Y2X 溶于水形成的溶液能与 ZX2 反应生成一种化合物 Y2ZX3。已知三种元素原子的质子总数为 25,且 Z 和 Y 的原子序数之和比 X 的 原子序数2倍还多 1,Z 原子有2个电子层,最外层电子数是核外电子数的 2/3 倍,试回答:
(1)Y 元素在元素周期表中的位置_____。
(2)Y2X 对应水化物的电子式_____。
(3)X 的氢化物比同主族的氢化物的熔沸点明显偏高的原因_____。
(4)X、Y 两种元素还可以形成除 Y2X 之外的另一种化合物,试用电子式表示该物质的形成 过程_________,该化合物与 1mol ZX2完全反应,则反应中电子转移的数目 为_____。(用 NA表示阿伏加德罗常数的值)
【答案】第三周期第ⅠA 族 ![]() 水分子间存在氢键
水分子间存在氢键 ![]() NA
NA
【解析】
Z 原子有2个电子层,最外层电子数是核外电子数的 2/3 倍,Z是C元素;X、Y、Z三种元素原子的质子总数为 25,且 Z 和 Y 的原子序数之和比 X 的 原子序数2倍还多 1,则X是O元素、Y是Na元素。
根据以上分析,(1)Y 是Na元素,在元素周期表中的位置是第三周期第ⅠA 族;
(2)Y2X是Na2O对应水化物是NaOH,电子式是![]() ;
;
(3)X的氢化物是H2O,水分子间存在氢键,所以比同主族的氢化物的熔沸点明显偏高;
(4) O、Na 两种元素可以形成Na2O、Na2O2 ,用电子式表示Na2O2的形成过程![]() ,Na2O2与CO2反应生成碳酸钠和氧气,Na2O2既是氧化剂又是还原剂,1mol CO2完全反应,电子转移的数目为NA。
,Na2O2与CO2反应生成碳酸钠和氧气,Na2O2既是氧化剂又是还原剂,1mol CO2完全反应,电子转移的数目为NA。


科目:高中化学 来源: 题型:
【题目】根据![]() 时某些物质的溶解度
时某些物质的溶解度![]() 数据:
数据:
|
|
|
|
|
|
|
|
下列说法不正确的是( )
A.碳酸镁悬浊液中存在![]()
![]()
![]()
B.用![]() 溶液浸泡锅炉中的水垢,可将水垢中的
溶液浸泡锅炉中的水垢,可将水垢中的![]() 转化为
转化为![]()
C.向![]() 悬浊液中滴加
悬浊液中滴加![]() ,沉淀变为红褐色,说明溶解度
,沉淀变为红褐色,说明溶解度![]()
D.向2mL饱和![]() 溶液中先后滴加
溶液中先后滴加![]() 的
的![]() 、NaOH溶液各2滴,产生的白色沉淀只有
、NaOH溶液各2滴,产生的白色沉淀只有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是生产生活中的常见有机物的分子式、结构式、结构简式或名称有关说法正确的是
①![]() ②
②![]() ③
③![]() ④
④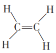 ⑤CH3CH2OH⑥C6H12O6⑦CH3COOH⑧硬脂酸甘油酯⑨蛋白质⑩聚乙烯
⑤CH3CH2OH⑥C6H12O6⑦CH3COOH⑧硬脂酸甘油酯⑨蛋白质⑩聚乙烯
A.能跟溴的四氯化碳溶液发生加成反应并使之褪色的有①②④⑩
B.含碳量最高、有毒、常温下为液体且点燃时有浓烟的是①
C.属于高分子材料的是⑧⑨⑩
D.投入钠能产生H2的是⑤⑦⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1 L 0.1 mol/L的醋酸溶液用蒸馏水稀释到10 L,下列叙述正确的是( )
A. c(CH3COOH)变为原来的1/10
B. c(H+)变为原来的![]()
C. c(CH3COO-)/c(CH3COOH)的比值增大
D. 溶液的导电性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构与H2O2类似,熔点为193K,沸点为411K,遇水很容易水解,产生的气体能使品红褪色,S2Cl2可由干燥氯气通入熔融的硫中制得。下列有关说法正确的是
A. S2Cl2的电子式为![]()
B. 固态时S2Cl2属于原子晶体
C. S2Cl2与NaOH的化学方程式可能为:S2Cl2+6NaOH=2NaCl+Na2SO3+Na2S+3H2O
D. S2Cl2是含有极性键和非极性键的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(N2H4)可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀,其中一种可能的反应机理如图所示。回答下列问题:
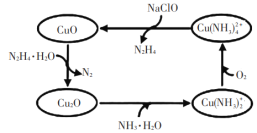
(1)1 mol N2H4·H2O含σ键的数目为______。
(2)Cu2O与NH3·H2O反应能形成较稳定的![]() 的原因是____。
的原因是____。
(3)N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃),沸点(114℃)分别远远高于O2的熔点(218℃),沸点(183℃),原因是____。
(4)NaClO发生水解可生成HClO,HClO的空间构型是___,中心原子的杂化类型是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,3.2 g 18O2所含的原子数为0.2NA
B.标准状况下,18 g H2O所含的氧原子数目为NA
C.室温下,8g CH4中含有5NA原子
D.常温常压下,1 mol CO2与SO2的混合气体中含原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0. 100 0 mol·L-1 NaOH溶液滴定20. 00 mL 0.100 0 mol·L-1 CH3COOH溶液所得滴定曲线如图。下列说法正确的是( )

A.点①所示溶液中:c(CH3COO-)+2c(OH-)=c(CH3COOH)+c(H+)
B.点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-)
C.滴定过程中可能出现:c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
D.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列叙述正确的是( )
A.某氨水的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a<b-1
B.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-)
C.1.0×10-3mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0
D.若10mLpH=a的硫酸溶液跟100mLpH=b的NaOH溶液混合后,溶液呈中性,则a+b=13
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com