
| A、二氧化硫使品红褪色是因为其漂白性,二氧化硫使酸性高锰酸钾褪色也是因为其漂白性 |
| B、CaCO3与稀硝酸反应生成CO2,CaSO3与稀硝酸反应生成SO2 |
| C、Fe与Cl2反应产生FeCl3,与硫单质反应产生Fe2S3 |
| D、H2CO3的酸性比HClO强,推出CO2通入NaClO溶液中能生成HClO |


科目:高中化学 来源: 题型:
A、14g C3H6中含有C-C键的数目一定为
| ||
| B、标准状况下,46g NO2气体中所含分子总数NA | ||
| C、常温常压下,133.5g AlCl3(即1mol)溶于1L水中可形成的氢氧化铝胶体粒子数小于NA | ||
| D、标准状况下,11.2L SO3中含有的原子总数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、431kJ?mol-1 |
| B、896kJ?mol-1 |
| C、649kJ?mol-1 |
| D、945.6kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为了降低成本,用工业酒精来兑酒 |
| B、油脂水解可制得肥皂 |
| C、使用太阳能等代替化石燃料,符合低碳节能减排的要求 |
| D、棉花与合成纤维的主要成分均为纤维素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol Na2O和Na2O2的混合物中所含阴离子数为NA |
| B、1.7g H2O2中含有的电子数为0.9NA |
| C、1mol Na2O2与足量的CO2反应,电子转移数为2NA |
| D、标准状况下,2.24L CO2和CO中所含分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
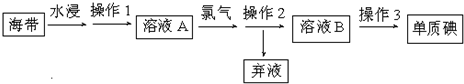
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(mg) | 255 | 385 | 459 |
| 气体体积(mL) | 280 | 336 | 336 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com