
【题目】金属及其化合物在人类生产、生产中发挥着重要的作用.
(1)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是(填化学式,下同);适宜做耐火材料的是 .
(2)若Na2CO3粉末中混有少量NaHCO3杂质,最适宜的除杂方法是 , 反应的化学方程式 .
(3)取少量FeCl2溶液,按如图所示操作,使其跟NaOH溶液反应.可观察到的实验现象是 . 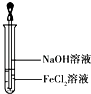
(4)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是(填序号).
A.有铜无铁
B.有铁无铜
C.铁、铜都有
D.铁、铜都无.
【答案】
(1)Na2O2;Al2O3
(2)加热;2NaHCO3 ![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
(3)试管中出现白色絮状沉淀,继而变成灰绿色,最后变成红褐色
(4)B
【解析】解:(1)钠的氧化物有氧化钠和过氧化钠,铝的氧化物有氧化铝,铁的氧化物有氧化亚铁、氧化铁和四氧化三铁,其中过氧化钠具有极强的氧化性;适合作耐火材料的氧化物必须具有高熔点,所以答案是:Na2O2 , Al2O3;(2)NaHCO3不稳定,可加热除杂,方程式为2NaHCO3 ![]() Na2CO3+H2O+CO2↑,所以答案是:加热,2NaHCO3
Na2CO3+H2O+CO2↑,所以答案是:加热,2NaHCO3 ![]() Na2CO3+H2O+CO2↑;(3)氯化亚铁和氢氧化钠反应生成白色氢氧化亚铁沉淀,迅速变为灰绿色,氢氧化亚铁不稳定易被氧化生成氢氧化亚铁红褐色沉淀,涉及的反应方程式为:FeCl2+2NaOH=Fe(OH)2↓+2NaCl,4Fe(OH)2+O2+2H2O=4Fe(OH)3↓,所以答案是:试管中出现白色絮状沉淀,继而变成灰绿色,最后变成红褐色;(4)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉, A.加入铁和铜的混合物,铁首先与氯化铁反应,可能铁全部反应而铜有剩余,故A正确; B.加入铁和铜的混合物,铁首先与氯化铁反应,铜后参加反应,不会出现有铁无铜的情形,故B错误; C.若氯化铁的量少,加入的铁粉和铜粉可能剩余,故C正确; D.若氯化铁的量多,加入的铁粉和铜粉全部参加反应,不会有剩余,故D正确;所以答案是:B.
Na2CO3+H2O+CO2↑;(3)氯化亚铁和氢氧化钠反应生成白色氢氧化亚铁沉淀,迅速变为灰绿色,氢氧化亚铁不稳定易被氧化生成氢氧化亚铁红褐色沉淀,涉及的反应方程式为:FeCl2+2NaOH=Fe(OH)2↓+2NaCl,4Fe(OH)2+O2+2H2O=4Fe(OH)3↓,所以答案是:试管中出现白色絮状沉淀,继而变成灰绿色,最后变成红褐色;(4)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉, A.加入铁和铜的混合物,铁首先与氯化铁反应,可能铁全部反应而铜有剩余,故A正确; B.加入铁和铜的混合物,铁首先与氯化铁反应,铜后参加反应,不会出现有铁无铜的情形,故B错误; C.若氯化铁的量少,加入的铁粉和铜粉可能剩余,故C正确; D.若氯化铁的量多,加入的铁粉和铜粉全部参加反应,不会有剩余,故D正确;所以答案是:B.


科目:高中化学 来源: 题型:
【题目】某芳香烃A有如下转化关系: 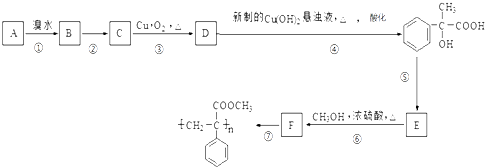
按要求填空:
(1)写出D中所含官能团的名称 , 指出⑤的反应类型 .
(2)反应②的反应条件是
(3)写出A和F结构简式:A;F
(4)写出反应③对应的化学方程式:
(5)写出D与新制Cu(OH)2悬浊液反应的化学方程式:
(6)E符合下列条件的同分异构体有多种,任写其中一种能同时满足下列条件的异构体的结构简式 .
a.苯环上的一氯代物有两种
b.遇FeCl3溶液发生显色反应
c.能与Br2/CCl4发生加成反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下图判断,下列叙述正确的是( ) 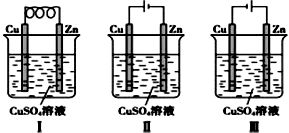
A.Ⅰ是原电池,Ⅱ是电镀装置
B.Ⅰ、Ⅱ装置中锌极上均发生氧化反应
C.Ⅱ、Ⅲ装置中,铜极均发生氧化反应而溶解
D.Ⅱ、Ⅲ装置中Cu2+浓度基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在托盘天平的两盘中各放入一个质量相等的烧杯,两烧杯中各盛有100mL1mol/L 硫酸溶液,向两烧杯中分别加入各组中的两种物质,反应后天平保持平衡的是( )
A.0.1mol Zn,0.1mol Fe
B.1mol Fe,1mol Zn
C.1g Zn,1g Fe
D.10g Zn,10g Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】试回答下列问题:
(1)9g水的物质的量是mol,含有mol 氢原子,含有个电子.
(2)等物质的量的SO2 和SO3 所含的原子个数之比是 , 质量比是 .
(3)0.4molNH3 中所含氢原子数与克水中所含氢原子数相等.
(4)质量分数为49%的硫酸溶液,其密度为1.4g/cm3 , 则其物质的量浓度为 .
(5)在aL Al2(SO4)3 和(NH4)2SO4 的混合溶液中加入b mol BaCl2 , 恰好使溶液中的SO42﹣完全沉淀;若加入足量NaOH 并加热可得到c mol NH3 , 则原溶液中Al3+的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医学研究证明,用放射性 ![]() I治疗肿瘤可收到一定疗效.下列有关
I治疗肿瘤可收到一定疗效.下列有关 ![]() I叙述正确的是( )
I叙述正确的是( )
A.![]() I是碘的一种同素异形体
I是碘的一种同素异形体
B.![]() I是一种新发现的元素
I是一种新发现的元素
C.![]() I位于元素周期表中第4周期Ⅳ族
I位于元素周期表中第4周期Ⅳ族
D.![]() I核内的中子数与核外电子数之差为29
I核内的中子数与核外电子数之差为29
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】698K时,向某V L的密闭容器中充入3mol H2(g)和3mol I2(g),发生反应:H2(g)+I2(g)2HI(g),测得各物质的物质的量浓度与时间变化的关系如右图所示.请回答下列问题: 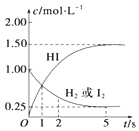
(1)容器的体积V=L.
(2)反应达到最大限度的时间是s,该时间内平均反应速率v(HI)= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com