
����Ŀ������������һ����ɫ����ζ�����Ҳ���ȼ�����壬�ڰ뵼��ӹ���̫���ܵ�������Һ����ʾ�������еõ��㷺Ӧ�ã�NF3��һ�������ͷ��ӣ�����102�����е���129��������ͭ�Ĵ���������F2����NH3��Ӧ�õ���
��1��д���Ʊ� NF3�Ļ�ѧ��Ӧ����ʽ�� ��
��2��NF3�ķе��NH3�ķе㣨��33�����͵ö����Ҫԭ���� ��
��3��NF3��NԪ�ز�ȡ ��ʽ�ӻ���
��4��������HF��NaAlO2��NaCl��6��1��2�����ʵ���֮��ǡ�÷�Ӧ����HCl��H2O��һ������ˮ����Ҫԭ�ϣ������ʺ�������Ԫ�أ�������ʵĻ�ѧʽΪ �����������ǣ���λ��Ϊ ��
��5����֪����Ԫ�أ���O����S����Se����Te������ҵ�Ͽ���Al2Te3���Ʊ�H2Te��������л�ѧ����ʽ��
Al2Te3+ �T Al��OH��3��+ H2Te��
��6����֪�ڳ����£�����17g H2S�ų�56.1KJ����������д������ֽ���Ȼ�ѧ����ʽ ��
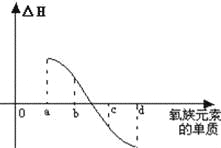
��7����ͼ��ʾΪ����Ԫ�ص�����H2��Ӧ�����е������仯ʾ��ͼ������a��b��c��d�ֱ��ʾ������ijһԪ�صĵ��ʣ���HΪ��ͬ���ʵ����ĵ�����H2��Ӧ�ķ�Ӧ�ȣ���b���� ��d���� ����д�������ƣ���
���𰸡���1��4NH3+3F2=NF3+3NH4F��
��2��NH3���γ������NF3ֻ�з��»�����
��3��sp3��
��4��Na3AlF6��Al3+��6��
��5��6H2O��2��3��
��6��H2S��g��=H2��g��+S��s����H="+112.2" kJmol��1��
��7������������
�������������������1��F2����NH3��Ӧ�õ�NF3��NH4F�����ԭ���غ������
��2��NH3�����������NF3ֻ���ڷ��Ӽ�����������������ô��ڷ��Ӽ���������
��3����������ԭ�ӵļ۲���Ӷ����жϣ�
��4��HF��NaAlO2��NaCl��6��1��2�����ʵ���֮��ǡ�÷�Ӧ����HCl��H2O��һ������ˮ����Ҫԭ�ϣ���Ӧ�Ļ�ѧ����ʽ��6HF+NaAl02+2NaCl�T2HCl+2H2O+Na3AlF6��Na3AlF6��������ΪAl3+����λ��Ϊ6��
��5����Al2Te3���Ʊ�H2Te����Ԫ���غ��֪����ˮ�μӣ�����Al��OH��3��H2Te��
��6���ڳ����£�����17g H2S�ų�56.1KJ����������1molH2S�ֽ�����112.2KJ������
��7����������Ԫ�صĵ������������ϵ�Խ��Խ�ѣ��Ƶ���a��b��c��d�ֱ�ΪTe��Se��S��O2��
�⣺��1�����ݷ�Ӧ����������Լ������غ㶨�ɿ�֪��Ӧ��Ӧ��NH4F���ɣ�
�ʴ�Ϊ��4NH3+3F2=NF3+3NH4F��
��2��NH3�����������NF3ֻ���ڷ��Ӽ�������������������ǰ�߽�ǿ�����ʵķе�ϸߣ�
�ʴ�Ϊ��NH3���γ������NF3ֻ�з��»�����
��3��NF3��Nԭ�ӵļ۲���Ӷ���=3+![]() ��5��3��1��=4���������ӻ�����Ϊsp3��
��5��3��1��=4���������ӻ�����Ϊsp3��
�ʴ�Ϊ��sp3��
��4���������֪�÷�Ӧ�Ļ�ѧ����ʽӦΪ��6HF+NaAl02+2NaCl�T2HCl+2H2O+Na3AlF6��������Ϊ��Na3AlF6����������ΪAl3+����λ��Ϊ6��
�ʴ�Ϊ��Na3AlF6��Al3+��6��
��5����ҵ�Ͽ���Al2Te3���Ʊ�H2Te����Ԫ���غ�������غ��֪���䷴Ӧ����ʽΪA12Te3+6H2O=2A1��OH��3��+3H2Te����
�ʴ�Ϊ��6H2O��2��3��
��6����H2��S��Ӧ����17g H2S�ų�56.1KJ������������ֽ���Ȼ�ѧ����ʽ��H2S��g��=H2��g��+S��s����H="+112.2" kJmol��1��
�ʴ�Ϊ��H2S��g��=H2��g��+S��s����H="+112.2" kJmol��1��
��7��������Ԫ�صĵ������������ϵ�Խ��Խ�ѣ��Ƶ���a��b��c��d�ֱ�ΪTe��Se��S��O2��
�ʴ�Ϊ������������


 ���ݼ���ϵ�д�
���ݼ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]()
![]()
![]() H+��H2������˵����ȷ���ǣ� ��
H+��H2������˵����ȷ���ǣ� ��
A. ������ͬ��������
B. ���в�ͬ�ĵ�����
C. ��Щ������ͬλ��
D. ��������Ԫ�ز�ͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȳ��C2H2�������������Ӧ�ܲ������»��棬����ʦ��������Ȳ���и�ӽ�������Ȳ��̼���ƣ���״���壬��ѧʽΪCaC2����ˮ��Ӧ���ɣ�ͬʱ����һ�ְ�ɫ���壮
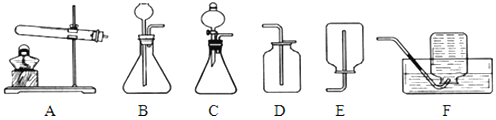
��1����֪̼������ˮ��Ӧ�dz����ң���Ȳ���ܶȱȿ�����С��ʵ��������ȡ���ռ���������Ȳ��Ҫ��������Լ����ȫ����ѡ���װ����______��ѡ��ͼ��װ����ţ���
��2��д����Ȳ�ڿ�����ȼ�յĻ�ѧ����ʽ����������������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��D��E��FΪԭ������������������ֶ���������Ԫ�أ��ǽ���Ԫ��A����������������������ͬ��B����������������������������2����B������D�����г��ȼ������������ۻ�����BD2��E+��D2��������ͬ�ĵ�������A������F������ȼ�գ���������ˮ�õ�һ��ǿ�ᡣ����Ӧ����ѧ�����ش��������⣺
��1��A�����ڱ��е�λ���� ��AFD�ĵ���ʽΪ ��
��2�� BD2�ĽṹʽΪ �� BD2�γɾ��������Ϊ ��
��3��Ԫ��D��E ��F�γɵļ����ӵİ뾶�ɴ�СΪ �������ӷ��ű�ʾ����
��4��д��ʵ�����Ʊ�����F�����ӷ���ʽ ��
��5��д��E��D�γɵļȺ����Ӽ��ֺ����ۼ��Ļ�������ˮ��Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͨ�������£��������ֵ���ֱ�ӻ��϶��ɵ������ǣ� ��
A��CuO B��NO2 C��FeCl2 D��SO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��Һ��ֻ���ܺ������������е������֣�����ˮ���������H����OH������H+��NH4����K����Mg2����Fe3+��Al3����NO3һ��CO32һ��SO42������ȡ����100 mL��Һ��������ʵ�飺
�� ��һ�ݼ�����AgNO3��Һ���а�ɫ����������
�� �ڶ��ݼ�����BaCl2��Һ���а�ɫ������������ϴ�ӡ������������Ϊ4.66 g��
�� ��������εμ�NaOH��Һ����ó�����NaOH��Һ�������ϵ����ͼ��
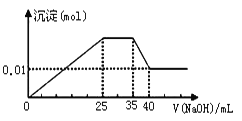
��������ʵ�飬�����Ʋ�����ȷ������ ��
A�����ݵ���غ㣬ԭ��Һ��NO3�������ʵ���ӦΪ0.03 mol
B��ԭ��Һһ��������H����Fe3����CO32��
C��ԭ��Һȷ����Mg2����Al3����NH4������n(Mg2��)��n(Al3��)��n( NH4��) = 1��1��2
D��ʵ�����ӵ�NaOH��Ũ��Ϊ2 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10�֣�
þ����Ͻ���һ����;�ܹ�Ľ������ϣ�Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ġ���Ҫ�������£�
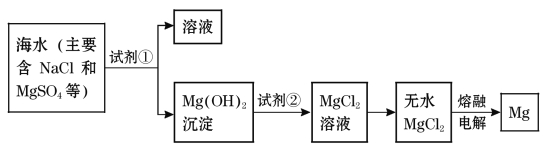
��1��Ϊ��ʹMgSO4ת��ΪMg(OH)2���Լ�������ѡ��___________��ҪʹMgSO4��ȫת��Ϊ�����������Լ�������Ӧ_________________��
��2�������Լ������ܹ�����õ�Mg(OH)2�����ķ�����_______________��
��3���Լ�������ѡ��___________________________��
��4����ˮMgCl2������״̬�£�ͨ�������Mg��Cl2��д���÷�Ӧ�Ļ�ѧ��ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E�Ƕ����ڵ���������Ԫ�أ�AԪ�ص�ij��ԭ�ӣ������û�����ӣ�BԪ�صĻ�̬ԭ��2p�����ֻ��һ�ԳɶԵ��ӣ�C��B����ͬһ���ڣ���ԭ�Ӱ뾶С��B��D��C��ͬ����Ԫ�أ�EԪ�ص�һ�������Ӻ�CԪ�ص������Ӿ�����ͬ�ĵ��Ӳ�ṹ������������Ϣ�ش��������⣺
��1��BԪ�ص�ԭ�ӽṹʾ��ͼ�� ��CԪ��ԭ�ӵĹ����ʾʽ�� ��DԪ��ԭ�ӵļ۵����Ų�ʽ�� ��
��2��AԪ�طֱ���C��D��Ԫ���γɵĻ�������ȶ�����ǿ������˳���ǣ��û�ѧʽ��ʾ�� ��
��3����B��D��E����Ԫ����ɵ�ij�ֻ������ˮ��Һ��ʹpH��ֽ�ȱ�������ɫ��д���û�����Ļ�ѧʽ ����һ�����ӷ���ʽ�����û�����ˮ��ҺʹpH��ֽ�ȱ�������ɫ��ԭ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2H��H2�ų�437.6 kJ������������˵����ȷ���ǣ� ��
A������������ÿ����ԭ�Ӷ��ﵽ��8�����ȶ��ṹ
B��1 mol H2��������2 mol H��������
C��1 mol H2����2 mol HҪ�ų�437.6 kJ����
D����ԭ�Ӳ�������ӻ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com