
| A. | 常温下,7.8g固体Na2O2中,含有的阴阳离子总数为0.4 NA | |
| B. | 4.48L氨气分子中含0.6NA个N-H键 | |
| C. | 铁、Cu片、稀硫酸组成的原电池,当金属铁质量减轻5.6g时,流过外电路的电子为0.3NA | |
| D. | 4℃时,20g2H216O中含有共用电子对数为2NA |
分析 A.过氧化钠中含有的阴离子为过氧根离子,0.1mol过氧化钠中含有0.2mol钠离子、0.1mol过氧根离子,总共含有0.3mol离子;
B.没有告诉标况下,不能使用标况下的气体摩尔体积计算;
C.铁与稀硫酸反应生成的是硫酸亚铁,0.1mol铁反应失去0.2mol电子;
D.该水的摩尔质量为20g/mol,其分子中含有2个共用电子对.
解答 解:A.7.8g过氧化钠的物质的量为:$\frac{7.8g}{78g/mol}$=0.1mol,0.1mol过氧化钠中含有0.2mol钠离子、0.1mol过氧根离子,总共含有0.3mol离子,含有的阴阳离子总数为0.3NA,故A错误;
B.不是标况下,不能使用标况下的气体摩尔体积计算4.48L氨气的物质的量,故B错误;
C.5.6g铁的物质的量为:$\frac{5.6g}{56g/mol}$=0.1mol,0.1mol铁与稀硫酸反应生成0.2mol电子,根据电子守恒,流过外电路的电子为0.2NA,故C错误;
D.20g2H216O的物质的量为:$\frac{20g}{20g/mol}$=1mol,1mol水分子中含有2mol氧氢键,所以含有共用电子对数为2NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.


科目:高中化学 来源: 题型:解答题
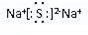 ,所含化学键类型离子键;
,所含化学键类型离子键;查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 氨基酸态氮的含量是将有质量的重要指标,这些氨基酸是通过大豆中的蛋白质发生分解反应生成的 | |
| B. | 配料清单中的苯甲酸钠属于防腐剂 | |
| C. | 小麦中的主要营养物质是纤维素 | |
| D. | “铁强化酱油”可帮助预防缺铁性贫血,但过量服用补铁剂也可能引起铁中毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠与水反应:2Na2O2+2H2O═4Na++4OH-+O2↑ | |
| B. | 用氢氧化钡溶液中和硫酸溶液:Ba2++OH-+H++SO42-═H2O+BaSO4↓ | |
| C. | 金属钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 在澄清石灰水中通入过量的CO2:Ca2++2OH-+2CO2═Ca(HCO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为226 | B. | 电子数为138 | C. | 中子数为138 | D. | 质量数为314 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+不一定存在 | B. | 100 mL溶液中含0.01 mol CO32- | ||
| C. | Cl-可能存在 | D. | Ba2+一定不存在,Mg2+可能存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其他分散系的根本原因是胶体有丁达尔效应 | |
| B. | 氯化铁溶液加入到冷水中可以制得氢氧化铁胶体 | |
| C. | 分散系中分散质粒子直径由小到大的正确顺序是:溶液<胶体<浊液 | |
| D. | 胶体的分散质可以通过过滤从分散剂中分离出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCOOCH2Cl | B. | ClCH2CH2OH | C. | CH2ClCHO | D. | HOCH2CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是4He的同素异形体 | B. | 比4He少一个电子 | ||
| C. | 是4He的同位素 | D. | 比4He少一个质子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com