
【题目】氨气有广泛用途,工业上利用反应N2(g)+3H2(g) ![]() 2NH3(g) H<0合成氨,其基本合成过程如下:
2NH3(g) H<0合成氨,其基本合成过程如下:

(1)某小组为了探究外界条件对反应的影响,以c0 mol/L H2参加合成氨反应,在a、b两种条件下分别达到平衡,如图A。
①a条件下,0~t0的平均反应速率v(N2)=___________mol·L-1·min-1。
②相对a而言,b可能改变的条件是______________________________。
③在a条件下t1时刻将容器体积压缩至原来的1/2,t2时刻重新建立平衡状态。请在答题卡相应位置画出t1~t2时刻c(H2)的变化曲线________。

(2)某小组往一恒温恒压容器充入9 mol N2和23 mol H2模拟合成氨反应,图B为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。若体系在T2、60MPa下达到平衡。
① 此时N2的平衡分压为__________MPa,H2的平衡分压为___________MPa。(分压=总压×物质的量分数)
② 列式计算此时的平衡常数Kp=____。(用平衡分压代替平衡浓度计算,结果保留2位有效数字)
(3)分离器中的过程对整个工业合成氨的意义是_____________________。
【答案】 (c0-c1)/300t0 增大c(N2)  9 15 0.043(Mpa)-2 及时分离出液氨,c(NH3)减小,使平衡往生成NH3的方向移动,增大原料利用率(或NH3产率)。
9 15 0.043(Mpa)-2 及时分离出液氨,c(NH3)减小,使平衡往生成NH3的方向移动,增大原料利用率(或NH3产率)。
【解析】(1)①a条件下,0~t0的平均反应速率v(N2)= ![]() v(H2)=
v(H2)= ![]() ×
×![]() =
=![]() ×
×![]() =
=![]() mol/(L·min),故答案为:
mol/(L·min),故答案为: ![]() ;
;
②a、b氢气起始浓度相同,b到达平衡的时间缩短,说明反应速率增大,平衡时氢气的浓度减小,说明平衡正向移动,所以改变的条件是增大c(N2),故答案为:增大c(N2);
③在a条件下t1时刻将容器体积压缩至原来的![]() ,t2时刻重新建立平衡状态,t1时刻变成2c1,t1~t2时刻的趋势逐渐减小,终点达到新的平衡时浓度大于c1,
,t2时刻重新建立平衡状态,t1时刻变成2c1,t1~t2时刻的趋势逐渐减小,终点达到新的平衡时浓度大于c1, ,故答案为:
,故答案为: ;
;
(2)①若体系在T2、60MPa下达到平衡,相同温度下,气体的体积分数等于其物质的量分数,
设平衡时n(NH3)=xmol,
N2(g)+3H2(g) ![]() 2NH3(g)
2NH3(g)
开始(mol) 923 0
反应(mol) 0.5x1.5x x
平衡(mol)9-0.5x 23-1.5x x
平衡时氨气体积分数=![]() ×100%=60%,x=12,氮气分压=
×100%=60%,x=12,氮气分压=![]() ×60MPa=9MPa;氨气的分压=60%×60MPa=36MPa,氢气分压=60MPa-9MPa-36MPa=15MPa,此时的平衡常数Kp=
×60MPa=9MPa;氨气的分压=60%×60MPa=36MPa,氢气分压=60MPa-9MPa-36MPa=15MPa,此时的平衡常数Kp= =0.043(MPa)-2,故答案为:9;15;0.043(MPa)-2;
=0.043(MPa)-2,故答案为:9;15;0.043(MPa)-2;
(3)分离器中的过程是分离出氨气促进平衡正向进行,及时分离出液氨,c(NH3)减小,使平衡往生成NH3的方向移动,增大原料利用率(或NH3产率);故答案为:及时分离出液氨,c(NH3)减小,使平衡往生成NH3的方向移动,增大原料利用率(或NH3产率)。


科目:高中化学 来源: 题型:
【题目】将2 mol过氧化钠与4 mol碳酸氢钠固体混合,在密闭容器中,120°C充分反应后,排出气体,冷却,有固体残留。下列分析正确的是
A. 残留固体是4 mol Na2CO3
B. 残留固体是Na2CO3和NaOH的混合物
C. 反应中转移4 mol电子
D. 排出的气体是3 mol氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向l0mL0.1mol/L氨水中缓缓加蒸馏水稀释到1L后,下列说法不正确的是
A. OH-数目增大,H+数目减小 B.  不变
不变
C. 电离程度增大,导电能力减弱 D. c(H+)与c(OH-)的乘积不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下将0.1 mol N2和0.3 mol H2置于密闭容器中发生反应N2+3H2![]() 2NH3。下列关于该反应的说法正确的是
2NH3。下列关于该反应的说法正确的是
A. 最终可生成0.2 mol NH3 B. 当n(N2):n(H2)=1:3时,反应一定达化学平衡
C. 升高温度反应速率增大 D. 增大压强反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期主族元素a、b、c的原子序数依次增大,a和b同主族,且b的核电荷数是a的质子数的2倍,下列说法正确的是
A. b的含氧酸的酸性比c的含氧酸的酸性弱
B. a与b形成的共价化合物在常温下为气体
C. ba2和c2均用作漂白剂,混合使用效果会更好
D. bac2在水中发生水解,可以生成两种酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖喱是一种烹饪辅料,若白衬衣被咖喱汁玷污后,用普通肥皂洗涤该污渍时会发现,黄色污渍变为红色。经水漂洗后红色又变为黄色。据此现象,你认为咖喱汁与下列何种试剂可能有相似的化学作用( )
A.品红溶液
B.石蕊溶液
C.氯水
D.KI淀粉溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJmol﹣1
②CH3OH(g)+ ![]() O2(g)═CO2(g)+2H2(g)△H=﹣192.9kJmol﹣1
O2(g)═CO2(g)+2H2(g)△H=﹣192.9kJmol﹣1
下列说法正确的是( )
A.CH3OH的燃烧热为192.9 kJmol﹣1
B.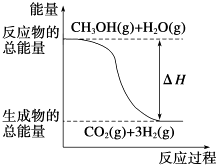
反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2(g)的△H>﹣192.9 kJmol﹣1
O2(g)═CO2(g)+2H2(g)的△H>﹣192.9 kJmol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com