
【题目】常温下向l0mL0.1mol/L氨水中缓缓加蒸馏水稀释到1L后,下列说法不正确的是
A. OH-数目增大,H+数目减小 B.  不变
不变
C. 电离程度增大,导电能力减弱 D. c(H+)与c(OH-)的乘积不变
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示:

(1)在25℃时,有一pH = 12的NaOH溶液100 mL ,欲使它的pH降为11。如果加入蒸馏水,就加入_______ mL;如果加入pH = 10的NaOH溶液,应加入_______mL(忽略溶液混合后体积的微小变化);
(2)当温度升高到B点时,水的离子积为________;加酸_______(填能或不能)使水的离子积由E点变到B点;
(3)在100℃下,将pH=8的氢氧化钠溶液与pH=5的盐酸溶液混合并保持100℃,欲使溶液的pH=7,则氢氧化钠溶液与盐酸的体积比为_________(忽略溶液混合后体积的微小变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
A. 向久置的氯水中滴入紫色石蕊试液,溶液先变红后褪色
B. pH在5.6~7之间的降水通常称为酸雨
C. 合金的熔点一般比成分金属的低
D. 硫粉在过量的纯氧中燃烧可生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列图像描述正确的是

A. 图①可表示将氨气通入醋酸溶液至过量过程中溶液导电性的变化
B. 根据图②可判断可逆反应A2(g)+3B2(g)![]() 2AB3(g)的ΔH>0
2AB3(g)的ΔH>0
C. 图③表示等体积、等pH的盐酸与醋酸溶液分别与足量的锌粉发生反应产生氢气的体积(V)随时的变化的示意图
D. 图④可表示压强对可逆反应A(g)+B(g)![]() 2C(g)+D(g)的影响,乙的压强大
2C(g)+D(g)的影响,乙的压强大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向明矾溶液中逐滴加入Ba(OH)2溶液,生成沉淀的物质的量与消耗Ba(OH)2的物质的量的关系如下图所示,下列说法正确的是

A. O~b点间的任意一点a的溶液均显酸性
B. b、c两点溶液均呈中性
C. b、c两点沉淀的物质的量之比为4:3
D. c点溶液呈碱性,原因是A1O2-+H++H2O===Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乙醇、乙酸和乙酸乙酯能用饱和碳酸钠溶液鉴别
B.乙醇和乙酸中都存在碳氧双键
C.常温下,Imol乙醇可与足量的金属钠反应生成11.2L氢气
D.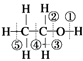
己知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键为②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气有广泛用途,工业上利用反应N2(g)+3H2(g) ![]() 2NH3(g) H<0合成氨,其基本合成过程如下:
2NH3(g) H<0合成氨,其基本合成过程如下:

(1)某小组为了探究外界条件对反应的影响,以c0 mol/L H2参加合成氨反应,在a、b两种条件下分别达到平衡,如图A。
①a条件下,0~t0的平均反应速率v(N2)=___________mol·L-1·min-1。
②相对a而言,b可能改变的条件是______________________________。
③在a条件下t1时刻将容器体积压缩至原来的1/2,t2时刻重新建立平衡状态。请在答题卡相应位置画出t1~t2时刻c(H2)的变化曲线________。

(2)某小组往一恒温恒压容器充入9 mol N2和23 mol H2模拟合成氨反应,图B为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。若体系在T2、60MPa下达到平衡。
① 此时N2的平衡分压为__________MPa,H2的平衡分压为___________MPa。(分压=总压×物质的量分数)
② 列式计算此时的平衡常数Kp=____。(用平衡分压代替平衡浓度计算,结果保留2位有效数字)
(3)分离器中的过程对整个工业合成氨的意义是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A. 摩尔是物质的质量的单位 B. 碳的摩尔质量为12g
C. 阿伏加德罗常数约为6.02×1023mol-1 D. 一个碳原子的质量为12g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com