
下表为元素周期表的一部分,请参照元素①一⑧在表中的位置,用化学用语回答下列问题: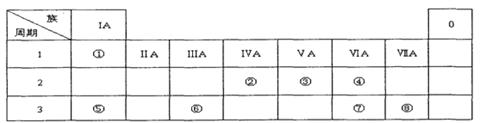
Ⅰ.(1)请画出元素⑧的阴离子结构示意图 。
(2)④、⑤、⑦的原子半径由小到大的顺序为 。
(3)⑤和⑥的最高价氧化物对应水化物的碱性强弱为 > 。
(4)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为 。
Ⅱ.由表中①一⑧中的一种或几种元素形成的常见物质A、B、C可发生以下反应(副产物已略去),试回答:
(1)若X是一种常见过渡金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是 ;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式 。
(2)若A、B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为 ,写出A与C两溶液反应的离子方程式____ 。
Ⅰ.(1)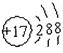 (1分)
(1分)
(2)Na>S>O (2分)
(3) NaOH >Al(OH)3 (2分)
(4)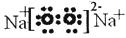 (2分)
(2分)
Ⅱ.(1)先加入KSCN溶液不显红色,再加入氯水显红色。(或加入氢氧化钠溶液,产生白色沉淀,然后变成灰绿色,最后变成红褐色。)。(2分) H2O2+2Fe2++2H+=2Fe3++2H2O (2分)
(2)Al(OH)3 (1分); Al3++3AlO2-+6H2O=4Al(OH)3↓(2分)
解析试题分析:Ⅰ.由元素在周期表中的位置可知,①为H,②为C,③为N,④为O,⑤为Na,⑥为Al,⑦为S,⑧为Cl;(1)⑧为Cl,氯离子的结构示意图为 ;(2)根据原子半径比较原则:电子层越多,半径越大,同周期从左向右原子半径在减小,原子半径为Na>S>O;(3)⑤为Na,⑥为Al,金属性Na>Al,则最高价氧化物的水化物的碱性为NaOH >Al(OH)3;(4)④、⑤两种元素的原子按1:1组成的常见化合物为Na2O2,其电子式为
;(2)根据原子半径比较原则:电子层越多,半径越大,同周期从左向右原子半径在减小,原子半径为Na>S>O;(3)⑤为Na,⑥为Al,金属性Na>Al,则最高价氧化物的水化物的碱性为NaOH >Al(OH)3;(4)④、⑤两种元素的原子按1:1组成的常见化合物为Na2O2,其电子式为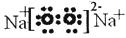 ;Ⅱ.(1)向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,C中含有Cl元素,X是一种常见过渡金属单质,则X为铁,A为氯气,B为氯化铁,C为氯化亚铁,C中的阳离子为亚铁离子,检验亚铁离子的步骤为先滴加KSCN溶液不显红色,再加入氯水显红色(或者加NaOH溶液,先产生白色沉淀,迅速变成灰绿色,最后变成红褐色);在酸性溶液中亚铁离子能被双氧水氧化,离子反应为H2O2+2Fe2++2H+═2Fe2++2H2O;(2)若A、B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,由转化关系可知,A为可溶性铝盐,B为Al(OH)3,C为偏铝酸盐,X为氢氧化钠,(或A为偏铝酸盐,B为Al(OH)3,C为可溶性铝盐,X为盐酸),则A与C反应的离子反应为
;Ⅱ.(1)向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,C中含有Cl元素,X是一种常见过渡金属单质,则X为铁,A为氯气,B为氯化铁,C为氯化亚铁,C中的阳离子为亚铁离子,检验亚铁离子的步骤为先滴加KSCN溶液不显红色,再加入氯水显红色(或者加NaOH溶液,先产生白色沉淀,迅速变成灰绿色,最后变成红褐色);在酸性溶液中亚铁离子能被双氧水氧化,离子反应为H2O2+2Fe2++2H+═2Fe2++2H2O;(2)若A、B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,由转化关系可知,A为可溶性铝盐,B为Al(OH)3,C为偏铝酸盐,X为氢氧化钠,(或A为偏铝酸盐,B为Al(OH)3,C为可溶性铝盐,X为盐酸),则A与C反应的离子反应为
Al3++3AlO2-+6H2O═4Al(OH)3↓。
考点:考查无机物的推断及元素周期律、元素周期表。


科目:高中化学 来源: 题型:填空题
在下列物质转化关系中,反应的条件和部分产物已略去。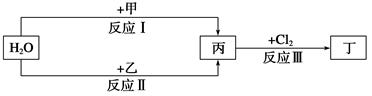
回答下列问题:
(1)若甲、乙是两种常见金属,反应Ⅲ是工业制盐酸的反应。
①反应Ⅰ中,甲在通常条件下和水剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是________(填字母)。
A.热分解法 B.热还原法 C.电解法
②反应Ⅱ中,乙与H2O在高温下反应,除丙外,还生成一种有磁性的物质,则反应Ⅱ的化学方程式是______________________________________。
③通过比较反应Ⅰ、Ⅱ的反应条件,可得出甲的金属性比乙的金属性________(填“强”或“弱”),比较二者金属性强弱的依据还可以是(写出一种即可)__________________。
(2)若甲、乙是化合物,且反应Ⅲ是工业制漂白粉的反应。
①反应Ⅲ的化学方程式是__________________________________________________。
②反应Ⅰ的另一种产物为有机物,则该有机物的电子式是______________。
③在饱和氯水中加块状石灰石,能制得较浓HClO溶液,同时放出一种气体。其反应的离子方程式是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知A~G有如图所示的转化关系(部分生成物已略去),其中A、G为单质,D是能使湿润的红色石蕊试纸变蓝色的气体,E、F均能与NaOH溶液反应。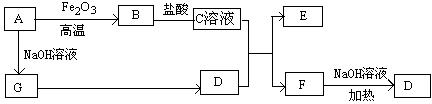
请回答下列问题:
(1)写出F的电子式:
(2)①C溶液与D反应的离子方程式为
②F溶液与NaOH溶液共热反应的化学方程式为
(3)①请用离子方程式解释C溶液为何显酸性
②F溶液中离子浓度由大到小的顺序为
(4)将5.4gA投入200mL 2.0mol/L某溶液中有G单质产生,且充分反应后有金属剩余,则该溶液可能是 (填代号)
A.HNO3溶液 B.H2SO4溶液 C.NaOH溶液 D.HCl溶液
(5)将1molN2和3molG及催化剂充入容积为2L的某密闭容器中进行反应,已知该反应为放热反应。平衡时,测得D的物质的量浓度为a mol/L。
①如果反应速率v(G)=1.2mol/(L·min),则v(D)= mol/(L·min)
②在其他条件不变的情况下,若起始时充入0.5molN2和1.5molG达到平衡后,D的物质的量浓度 (填“大于”、“小于”或“等于”)a/2 mol/L。
③该条件下的平衡常数为 (用含a的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A~F是中学化学中常见物质,常温下A、C、E、F为气体,B、D为液体,其中B的分子为4原子分子,D在常温下不具有挥发性。F的浓溶液与X共热通常用于实验室制备单质C,X是
一种黑色粉末。这些物质之间满足如下图所示的转化关系,图中部分生成物已略去。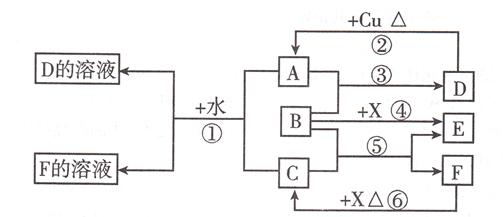
(1)写出下列物质的化学式:A______,F______。
(2)B的电子式是______。根据图中信息,B、C、X的氧化性由强到弱的顺序是_ _____(用化学式表示)。
(3)反应⑥的离子方程式是__ ____。
(4)在反应⑥中,F表现的性质是___ ____,当生成0.75mol C时,被氧化的还原剂的物质的量是___ ____。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知:A、B、C为中学常见的单质,A为淡黄色固体;D、E、F、M为中学常见的氧化物,E是磁铁矿的主要成分(是黑色固体);H、K为中学常见的盐;M是一种常见的无色液体。各物质间的转化关系如下图所示(某些条件已略去)。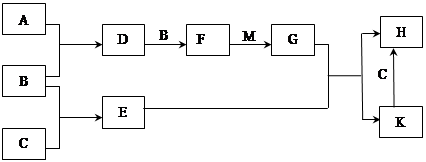
请回答:
(1)物质H的化学式为 。
(2)由F与M作用生成G的化学反应基本类型为 。
(3)A与C在加热条件下反应的化学方程式为: 。
(4)G的浓溶液在加热条件下能跟C反应,该反应中G体现了 (填序号)。
A.氧化性 B.还原性 C.漂白性 D.酸性
(5)若先将D气体通入BaCl2溶液中,再通入NH3,实验过程中的现象为 。
(6)H溶液在空气中长期放置会出现红褐色浑浊,请用一个离子方程式表示其变化的原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
中学化学常见物质A在一定条件下发生如下反应:A+B→E+F+H2O(未配平)
(1)若A为小苏打,F为气体。该反应的离子方程式为 。
(2)若A为紫红色金属单质,气体F是由两种位于同一主族的短周期元素组成。则反应的化学方程式为_____________________。
(3)若A是磁铁矿的主要成分,B是盐酸。写出反应的化学方程式为 。
(4)若A为黄氯色气体单质,F的碱性溶液吸收废气中SO2的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E是中学常见的几种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。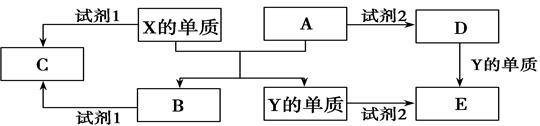
回答下列问题:
(1)X的单质与A反应的化学方程式是________________________________。
(2)若C溶液显碱性,则试剂1是 ____溶液(写化学式);若C溶液显酸性,则显酸性的原因是(用离子方程式表示) 。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是 ;
②写出D→E反应的离子方程式 ;
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠(NaNO2)为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在下列物质转化关系中,反应的条件和部分产物已略去。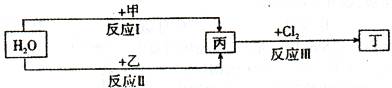
回答下列问题:
(1)若甲、乙是两种常见金属,反应Ⅰ是工业制盐酸的反应。
①反应I中,甲在通常条件下和水剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,
则工业上生产甲的一般方法是_ 。
A.热分解法 B.热还原法 C.电解法
②反应Ⅱ中,乙与H2O在高温下反应,除丙外,还生成一种有磁性的物质,则反应a的化学方程式是
③通过比较反应I、II的反应条件,可得出甲的金属性比乙的金属性_ (填“强”或“弱”)。
(2)若甲、乙是化合物,且反应Ⅲ是工业制漂白粉的反应。
①反应II是化合反应。目前常用乙作为燃煤的脱硫剂,则乙脱硫的主要反应的化学方程
式是
②在饱和氯水中加块状石灰石,能制得较浓HClO溶液,同时放出一种气体。其反应的离
子方程式是
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知A是生产生活中用量最大的金属,B为淡黄色粉末。在常温下C为无色液体,E、G、H、I、J为气体,其中H为黄绿色,其它为无色。J能使湿润的红色石蕊试纸变蓝(图中部分产物已略去)。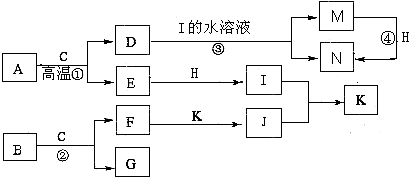
请填写下列空白
(1)写出化学式:D ,K 。
(2)写出②的离子方程式 。
(3)反应④不属于下列何种反应类型 (填字母序号)。
A.化合反应 B.氧化还原反应 C.离子反应 D.置换反应
(4)若要确定③反应后所得溶液中含有M物质,所选试剂为 (填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN
C.浓氨水 D.酸性高锰酸钾溶液
(5)将F加入到M的溶液里并露置在空气中,可以观察到整个过程的现象是:
。
(6)常温下,H与过量的J反应产生浓厚的白烟,另一生成物是空气的主要成分之一,请写出该反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com