
(10分)将含镁、钾的盐湖水蒸发,最后得到的产物中含光卤石(xKCl·yMgCl2·zH2O)。
它在空气中极易潮解,易溶于水,是制造钾肥和提取金属镁的重要原料,其组成可通过下列实验测定。
①准确称取5.550 g样品溶于水,配成100 mL溶液。
②将溶液分成二等份,在一份中加入足量的NaOH溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.580 g。
③在另一份溶液中加入足量的硝酸酸化的AgNO3溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体4.305 g。
(1)步骤②中检验白色固体已洗净的方法是 。
(2)已知某温度下Mg(OH)2的Ksp = 6.4×10-12,当溶液中c(Mg2+)≤1.0×10-5 mol·L-1 可视为沉淀完全,则应保持溶液的OH-的浓度≥ mol·L-1 。
(3)通过计算确定样品的组成(写出计算过程)。
(1)取最后一次洗涤液少许,滴加硝酸酸化的硝酸银溶液,若不产生沉淀,则已经洗涤干净;
(2)8.0×10-4;
(3)5.550g样品中含有n(Mg2+)=n(Mg(OH)2)=(0.580g÷58 g/mol)×2=0.0200mol;
n(MgCl2)= 0.0200mol;n(Cl-)= n(AgCl)=(4.305g÷143. 5g/mol)×2=0.0600mol;
n(KCl)=0.0600mol-2×0.0200mol=0.0200mol;
n(H2O)= (5.550g-0.0200mol×95g/mol-0.0200mol×74.5g/mol)÷18g/mol=0.120mol.
样品中n(KCl):n(MgCl2):n(H2O)=1:1: 6。所以光卤石的化学式是KCl·MgCl2·6H2O.
【解析】
试题分析:(1)将向含光卤石(xKCl·yMgCl2·zH2O)的水溶液中加入过量的NaOH溶液,会发生离子反应:Mg2++2OH-=Mg(OH)2↓,而K+、Na+、Cl-则留在滤液中。在步骤②中若要检验白色固体已洗净,只要证明在滤液中无Cl-即可,方法是取最后一次洗涤液少许,滴加硝酸酸化的硝酸银溶液,若不产生沉淀,则已经洗涤干净;
(2)在某温度下Mg(OH)2的Ksp = 6.4×10-12,即c(Mg2+)·c2(OH-)≥6.4×10-12,当溶液中c(Mg2+)≤1.0×10-5 mol·L-1 可视为沉淀完全,则应保持溶液的OH-的浓度c2(OH-)≥6.4×10-12÷1.0×10-5 mol·L=6.4×10-7mol/L; c(OH-)≥8×10-4mol/L;
(3) 5.550g样品中含有n(Mg2+)=n(Mg(OH)2)=(0.580g÷58 g/mol)×2=0.0200mol;
n(MgCl2)= 0.0200mol;n(Cl-)= n(AgCl)=(4.305g÷143. 5g/mol)×2=0.0600mol;
n(KCl)=0.0600mol-2×0.0200mol=0.0200mol;
n(H2O)= (5.550g-0.0200mol×95g/mol-0.0200mol×74.5g/mol)÷18g/mol=0.120mol.
样品中n(KCl):n(MgCl2):n(H2O)=1:1: 6。所以光卤石的化学式是KCl·MgCl2·6H2O.
考点:考查沉淀的洗涤、溶度积常数的应用、守恒等知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年山东省菏泽市高三1月月考化学试卷(解析版) 题型:选择题
将6molA和2molB在2L的密闭容器中混合并在一定条件下发生如下反应:3A(g)+B(S) 2C(g) ΔH<0,4s(秒)后反应达到平衡状态,此时测得C的浓度为1mol·L-1,下列说法中正确的是
2C(g) ΔH<0,4s(秒)后反应达到平衡状态,此时测得C的浓度为1mol·L-1,下列说法中正确的是
A.4s内用物质B表示的反应速率为0.125mol·L-1·S-1
B.达到平衡后若向容器中通入惰性气体,则A的转化率增大
C.此时,A、B、C的物质的量之比为3:1:2
D.达平衡后若升高温度,C的浓度将增大
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:选择题
反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
A.增加铁的量
B.将容器体积缩小一半
C.升高温度
D.压强不变,充入N2使容器体积增大
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏徐州市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列有关碳酸钠和碳酸氢钠性质的说法中正确的是
A.25℃时,碳酸氢钠在水中的溶解度比碳酸钠的小
B.用澄清石灰水能将碳酸钠溶液和碳酸氢钠溶液区别开来
C.加热时,碳酸钠、碳酸氢钠固体均能反应并都生成二氧化碳气
D.常温下,浓度均为0.l mol.L-1溶液的pH大小:NaHCO3 >Na2CO3
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏徐州市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列物质中,既能导电又属于电解质的是
A.蔗糖 B.熔融的氯化钠 C.氯化氢气体 D.锌片
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二第一学期化学试卷(解析版) 题型:填空题
(14分)W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子最外层电子排布为3s23p1,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)则W为 ,X为 ,Y为 ,Z为 。(填元素符号)
W的气态氢化物稳定性比H2O(g) (填“强”或“弱”)。
(2)Z原子的基态原子核外电子排布式是 ,Y的电负性比X的________(填“大”或“小”),W的第一电离能比O的 (填“大”或“小”)。
(3)X的最高价氧化物对应水化物与NaOH溶液反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二第一学期化学试卷(解析版) 题型:选择题
向ZnSO4溶液中加入Na2S溶液时,得到白色沉淀,然后向白色沉淀上滴加CuSO4溶液,发现沉淀变为黑色,则下列说法不正确的是
A.白色沉淀为ZnS,而黑色沉淀为CuS
B.利用该原理可实现一种沉淀转化为更难溶的沉淀
C.该过程破坏了ZnS的溶解平衡
D.上述现象说明ZnS的Ksp小于CuS的Ksp
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
某温度时,在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系的比较正确的是
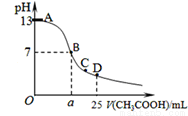
A.在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
B.在C点:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
D.在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省怀化市小学课改高二上学期期末化学试卷(解析版) 题型:选择题
今有如下三个热化学方程式:
H2(g)+1/2O2(g) = H2O(g) ΔH=a kJ·mol-1
H2(g)+1/2O2(g) = H2O(l) ΔH=b kJ·mol-1
2H2(g)+O2(g) = 2H2O(l) ΔH=c kJ·mol-1
关于它们的下列表述,正确的是
A.它们都是吸热反应 B.氢气的燃烧热为ΔH=a kJ·mol-1
C.反应热的关系:a=b D.反应热的关系:2b=c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com