
强酸与强碱的稀溶液发生中和反应的热效应为: H+(aq)+OH-(aq)===H2O(l) ΔH =-57.3kJ·mol-1。分别向1 L 0.5mol/L的NaOH溶液中加入①浓硫酸;②稀硫酸;③稀盐酸,恰好完全反应的热效应分别为ΔH1、ΔH2、ΔH3,下列关系正确的是( )
A.ΔH1>ΔH2>ΔH3 B.ΔH1<ΔH2<ΔH3 C.ΔH1=ΔH2<ΔH3 D.ΔH1<ΔH2=ΔH3
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
氧化还原反应与四种基本类型反应的关系如下图所示,则下列化学反应属于区域3的是( )
A.4Fe(0H)2+O2+2H2  4Fe(OH)3
4Fe(OH)3
B.2NaHCO3  Na2CO3+H2 O+CO2↑
Na2CO3+H2 O+CO2↑
C.4NH3+5O2  4NO+6H2O
4NO+6H2O
D.Zn+H2SO4 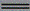 ZnSO4+H2 ↑
ZnSO4+H2 ↑
查看答案和解析>>
科目:高中化学 来源: 题型:
β-紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素 A1。
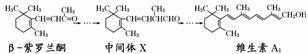
下列说法正确的是( )
A.β-紫罗兰酮可使酸性 KMnO4 溶液褪色
B.1 mol中间体 X最多能与3 mol H2发生加成反应
C.维生素 A1 易溶于NaOH 溶液
D.β-紫罗兰酮与中间体X互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
可降解聚合物P的合成路线如下:
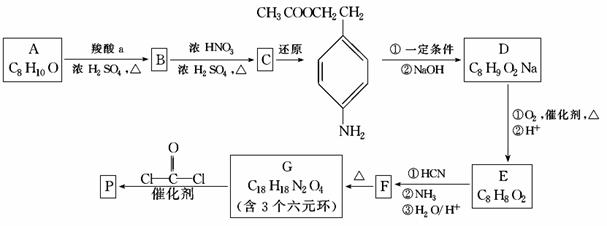
已知:

(1)A的含氧官能团名称是________。
(2)羧酸a的电离方程式是____________________________________。
(3)B→C的化学方程式是____________________________________。
(4)化合物D苯环上的一氯代物有2种,D的结构简式是____________________________________。
(5)E→F中反应①和②的反应类型分别是____________________________________。
(6)F的结构简式是____________________________________。
(7)聚合物P的结构简式是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
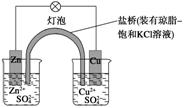
铜锌原电池(如图)工作时,下列叙述正确的是 ( )
A.正极反应为:Zn-2e-===Zn2+
B.电池反应为:Zn+Cu2+===Zn2++Cu
C.在外电路中,电子从正极流向负极
D.盐桥中的K+移向ZnSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知:H2(g)+O2(g) H2O(g),反应过程中能量变化如图所示,则:
H2O(g),反应过程中能量变化如图所示,则:

①试写出a、b、c分别代表的意义:
a ;
b ;
c 。
②该反应是 反应(填“吸热”或“放热”),ΔH 0(填“>”或“<”)。
(2)发射“天宫”一号的火箭使用的推进剂是液氢和液氧,这种推进剂的优点是 , 。(请写两条)
(3)已知:H2(g)+O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
H2(g)==H2(l) ΔH=-0.92 kJ·mol-1
O2(g)==O2(l) ΔH=-6.84 kJ·mol-1
H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
请写出液氢和液氧生成气态水的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
向某密闭容器中加入0.6 mol A、 0.2 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如甲图所示[其中t0~t1阶段c(B)未画出]。t2时刻后改变条件反应体系中反应速率随时间变化的情况如乙图所示,且四个阶段都各改变一种条件并且改变的条件均不相同。下列说法正确的是
0.2 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如甲图所示[其中t0~t1阶段c(B)未画出]。t2时刻后改变条件反应体系中反应速率随时间变化的情况如乙图所示,且四个阶段都各改变一种条件并且改变的条件均不相同。下列说法正确的是
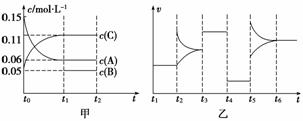
A.反应的方程式为3A(g)+B(g)  2C(g)
2C(g)
B.t3~t4,t4~t5,t5~t6各阶段可能改变的条件依次为:加催化剂,降低反应温度,增大压强
C.B的起始物质的量为0.08 mol
D.若t1=10 s,A在t0~t1时间段的反应速率为0.002 25 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO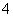 +H2C2O4+H+——Mn2++CO2↑+H2O(未配平)。用4 mL 0.001 mol·L-1KMnO4溶液与2 mL 0.01 mol·L-1H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+H2C2O4+H+——Mn2++CO2↑+H2O(未配平)。用4 mL 0.001 mol·L-1KMnO4溶液与2 mL 0.01 mol·L-1H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | |
| Ⅱ | 2 | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2 | 30 | |
| Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(1)该反应中氧化剂和还原剂的物质的量之比为________________________________________________________________________。
(2)如果研究催化剂对化学反应速率的影响,使用实验______和______(用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验______和______。
(3)对比实 验Ⅰ和Ⅳ,
验Ⅰ和Ⅳ, 可以研究________对化学反应速率的影响,实验Ⅳ中加入1 mL蒸馏水的目的是__________________________________________
可以研究________对化学反应速率的影响,实验Ⅳ中加入1 mL蒸馏水的目的是__________________________________________ ________________________。
________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸铵是一种常用的化肥,其工业生产流程如下图,请回答下列问题。
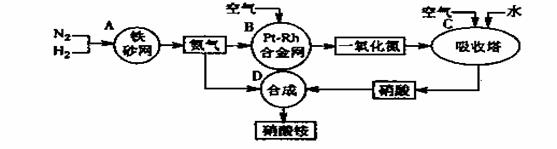
⑴写出反应容器B中发生反应的化学方程式: 。
⑵吸收塔C中通入空气的目的是 ;
A、B、C、D四个反应容器中发生的反应,属于氧化还原反应的是 (填反应容器代号)。
⑶浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因: 。
⑷金属铜与浓硝酸反应的离子方程式是 ,该反应中浓硝酸表现的性质是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com