
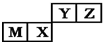
| A. | 原子半径:M>X>Y>Z | |
| B. | M的氯化物是弱电解质 | |
| C. | X的最简单气态氢化物的热稳定性比Z的小 | |
| D. | 简单离子的半径M小于Z |
分析 根据元素在周期表中的位置可知,这Y、Z处于第二周期,M、X处于第三周期,只有M为金属元素,可知M为Al元素,则X为Si元素、Y为氮元素、Z为氧元素,以此解答该题.
解答 解:根据元素在周期表中的位置可知,这Y、Z处于第二周期,M、X处于第三周期,只有M为金属元素,可知M为Al元素,则X为Si元素、Y为氮元素、Z为氧元素,
A.一般来说原子核外电子层数越多,原子半径越大,同周期元素从左到右原子半径逐渐减小,则原子半径M>X>Y>Z,故A正确;
B.M为Al元素,对应的氯化物在溶液中完全电离,为强电解质,故B错误;
C.非金属性O>Si,水的稳定性较强,故C正确;
D.M为Al、Z为O,铝离子与氧离子的电子层数相同,铝离子的核电荷数较大,则铝离子的离子半径较小,故D正确;
故选B.
点评 本题考查原子结构与元素周期律、元素周期表的关系,题目难度中等,推断元素是解题关键,注意对元素周期表的整体把握,注意对元素周期律的理解掌握,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | Cl2>Fe3+>Cu2+>PbO2 | B. | PbO2>Cl2>Fe3+>Cu2+ | ||
| C. | Fe3+>Cu2+>PbO2>Cl2 | D. | Cu2+>Fe3+>Cl2>PbO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
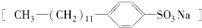 是常用洗涤剂的主要成分.其结构可用图形
是常用洗涤剂的主要成分.其结构可用图形 来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:
来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题: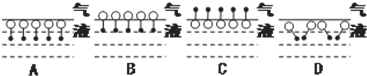
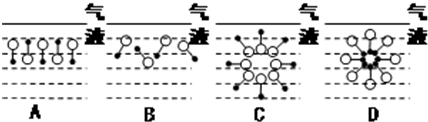
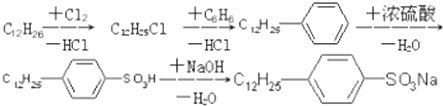
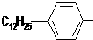 .
.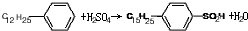 ,反应类型为取代反应.
,反应类型为取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不同元素的原子发生跃迁时,会释放不同的光 | |
| B. | 第一电离能与电负性的数值都是以气态中性基态原子为研究对象测得到 | |
| C. | 分子中的原子有固定的空间位置,组成完全相同的分子,由于原子位置的不同会表现出不同的性质 | |
| D. | 两个相同的原子的任意未成对电子的电子云在两个原子核间重叠,形成非极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
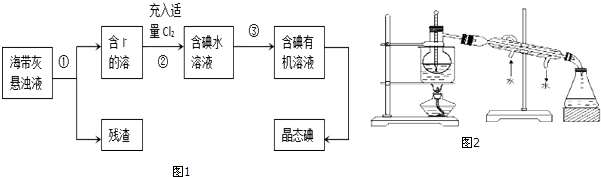
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
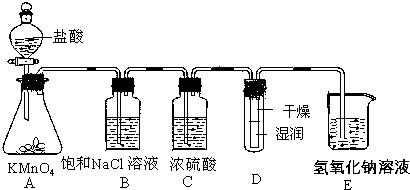
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
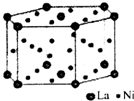 自然界存在的元素中,丰度最大的是非金属.80%以上的非金属在现代技术包括能源、功能材料等领域占有极为重要的地位.
自然界存在的元素中,丰度最大的是非金属.80%以上的非金属在现代技术包括能源、功能材料等领域占有极为重要的地位. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com