
| A、SO2能使品红溶液和酸性KMnO4溶液褪色,都是因为SO2具有漂白性 |
| B、硅单质是制造光电池、CPU和光导纤维的主要原料 |
| C、质量相等的碳酸钠和碳酸氢钠分别与足量盐酸反应,产生气体的质量相同 |
| D、FeSO4溶液存放在加有少量铁粉的试剂瓶中 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

| A、②③⑤⑧ | B、③⑤⑦⑧ |
| C、③④⑤⑧ | D、②③⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
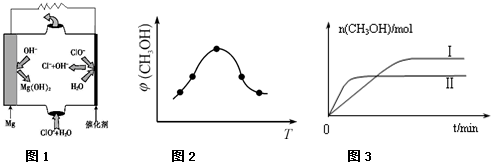
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2 3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 N2O5是一种新型硝化剂,其性质和制备受到人们的关注.一定温度下,在2L固定容积的密闭容器中发生反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示.下列说法中,正确的是( )
N2O5是一种新型硝化剂,其性质和制备受到人们的关注.一定温度下,在2L固定容积的密闭容器中发生反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示.下列说法中,正确的是( )| A、0~20 s内平均反应速率v(N2O5)=0.1 mol?(L?s)-1 |
| B、曲线a表示NO2的物质的量随反应时间的变化 |
| C、10 s时,正、逆反应速率相等,达到平衡 |
| D、20 s时,正反应速率大于逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18a L |
| B、24a L |
| C、96a L |
| D、144a L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②⑤⑥ | B、②⑥⑦ |
| C、①⑤ | D、③④⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com