


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、①③ | B、②③⑤ |
| C、③④⑤ | D、③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
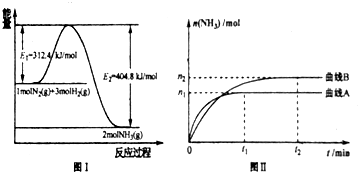
 合成氨反应过程中的能量变化如图所示,据图回答下列问题:
合成氨反应过程中的能量变化如图所示,据图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| n1 |
| 4t1 |
| 7 |
| 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某温度下,化学反应速率无论是用A、B、C何种物质来表示,其化学反应速率的数值相同 |
| B、在其他条件不变的情况下,降低温度,一般化学反应速率降低 |
| C、在其他条件不变的情况下,增大压强,单位体积内活化分子百分数一定增大,化学反应速率一定增大 |
| D、若增大或减少A物质的量,化学反应速率一定会发生明显的变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com