
����Ŀ�����ܱ�������Ͷ��һ������A��B������Ӧ��mA(g)��nB(g)![]() pC(g)��qD(g)��
pC(g)��qD(g)��
��1������ʼʱ����A����m mol����ʹA��B��ת������ȣ������B����________mol��
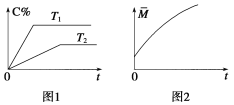
��2����ͬ��ѹǿ�£�����һ������A��B���ڲ�ͬ�¶���C�İٷֺ�����ʱ��Ĺ�ϵ��ͼ1��ʾ����T1(������������������������)______T2���÷�Ӧ����Ӧ�������H(������������������������)______0��
��3��һ�������£�������Ӧ��ʼ���ﵽ��ѧƽ��Ĺ����У���������ƽ����Է���������ʱ��ı仯��ͼ2��ʾ����ôﵽƽ��ʱA��B��C��D�����ʵ�����Ϊ1 mol��
�����ں��º��ݵ������£����ƽ����ϵ����ͨ��A��B��C��D��1 mol������ϵ�������ƽ����Է�������(����������������С������������������ȷ����)__________��
�������º�ѹ�������£���ԭƽ����ϵ����ͨ��A��B��C��D��1 mol������ϵ��������ܶ�(����������������С������������������ȷ����)__________��
���𰸡�n �� �� ���� ����
��������
(1)��Ӧ��������ϵ�и����ʵı仯���뷽��ʽ�и����ʵĻ�ѧ�����������ȡ���ʹA��B��ת������ͬ������Ҫ����ѧ����ʽ��A��B�ļ�����֮��Ͷ�ϣ��ʵ�����mmol Aʱ��Ӧ����nmol B��
(2)���ݡ��ȹ���ƽ����T1��T2��T1ʱC%����T2ʱC%���������¶ȣ�ƽ��������Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ����H��0��
(3)��ͼ2��֪�����ŷ�Ӧ�Ľ��У��������ƽ����Է��������������ڷ�Ӧ��ϵ�и����ʾ�Ϊ���壬��m��n��p��q��
���ں��º���ʱ�ټ���A��B��C��D��1 mol��ͬʱ����ϵ�и����ʵ�Ũ��ͬʱ����һ�������൱������ѹǿ��ƽ��������Ӧ�����ƶ���ƽ����Է�����������
���ں��º�ѹʱ���ټ���A��B��C��D��1 mol�������������һ����ѹǿ���䣬ƽ�ⲻ�ƶ����Ѳ��䡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƶ�֧������������������������Ϊ�й������Ĵ����������ڸ���������������ҵ����Ҫ����������(����)

A.Na��K�Ͻ�B.Cu��Sn�Ͻ�C.Sn��Pb�Ͻ�D.Mg��Al�Ͻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
�ٶ����������NaOH��Һ��Ӧ����˿���NaOH��Һ��̲�����
�� ��������ˮ��ˮ������Al(OH)3���壬��˿���������������ˮ����ɱ��������
�� ���������������������ӽ������ȶԺ�ˮ���е�����
�� �Ӻ�������ȡ��ֻ���õ�����ˮ��H2O2��Һ�����Ȼ�̼�����Լ���
�ݵع��Ϳ������Ʒ�������ȡ���ͻ�������������ͣ�
��ʯӢ������Na2O��CaO��6SiO2�����ۡ���ˮ�������������Ϊ��������������������ʡ�
A. �ۢݢ� B. �٢ܢ� C. �����ⶼ��ȷ D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������A��B��C��D�����л�����й���Ϣ��
A | ����ʹ������Ȼ�̼��Һ��ɫ���ڱ���ģ��Ϊ ������ˮ��һ�������·�Ӧ�����л���C |
B | ����C��H����Ԫ����ɣ������ģ��Ϊ |
C | ����C��H��O����Ԫ����ɣ�������Na��Ӧ����������NaOH��Һ��Ӧ������Cu�������Ҽ�������������O2��Ӧ |
D | ����C��H��O����Ԫ����ɣ������ģ��Ϊ ������C��Ӧ������Է�������Ϊ100���� |
�ش��������⣺
��1��A��������Ȼ�̼��Һ��Ӧ���������������___��
��2��B���������____(�����)��
����ɫ��ζҺ�� ���ж� �۲�����ˮ ���ܶȱ�ˮ�� ��������KMnO4��Һ����ˮ��Ӧ��ɫ ���κ������²���������Ӧ ������ˮ��Ϻ�Һ��ֲ����ϲ�ʳȺ�ɫ��
��3����B�Ʊ��������Ļ�ѧ����ʽ____��
��4��D��C��Ӧ��������Է�������Ϊ100�������÷�Ӧ�ķ�Ӧ����Ϊ___���仯ѧ����ʽΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¾ɶ���ת������֮һ������Դ�²��ϵ��ھ��Ӧ�á��Ҷ�������Ҫ�Ļ���ԭ�ϣ� ú���ϳ���(CO��H2)������Ҷ�������ת���ʸߡ������ʸߵ��ŵ㣬���ҹ�һ��ӵ������֪ʶ��Ȩ�������״��������Ʊ��������£�
��Ӧ I��4NO(g)+4CH3OH(g)+O2(g)![]() 4CH3ONO(g)+2H2O(g) ��H1 =akJ��mol-1
4CH3ONO(g)+2H2O(g) ��H1 =akJ��mol-1
��Ӧ II��2CO(g)+2CH3ONO(g)![]() CH3OOCCOOCH3(l)+2NO(g) ��H2=b kJ��mol-1
CH3OOCCOOCH3(l)+2NO(g) ��H2=b kJ��mol-1
��Ӧ III��CH3OOCCOOCH3(1)+4H2(g)![]() HOCH2CH2OH(1)+2CH3OH(g) ��H3=c kJ��mol-1
HOCH2CH2OH(1)+2CH3OH(g) ��H3=c kJ��mol-1
��1����д��ú���ϳ���[n(CO)��n(H2)= 1��2]��������Ӻϳ��Ҷ��������Ȼ�ѧ����ʽ��__���÷�Ӧ�ڽϵ������������Է����У�����H___0(������������������������)��
��2��һ���¶��£���2L���ܱ�������Ͷ�����ʵ�����Ϊ0.4mol��CO��CH3ONO������ӦII��10min�ﵽƽ��ʱCO�����������NO�����������ȡ�
������ѡ�����жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����____��
a.CO���������ٱ仯
b.���������ܶȲ��ٱ仯
c.��λʱ��������CO��NO�����ʵ������
d.CO��CH3ONO��Ũ�ȱȲ��ٱ仯
������ʱ����������ͨ��0.4molNO��һ��ʱ��ﵽ��ƽ��ʱNO�����������ԭƽ��ʱ���__(���������������������С����������ȷ����)��
�����÷�Ӧ��H��0���ں��ݵ��ܱ������У���Ӧ��ƽ��ı�ijһ����������ʾ��ͼ��ȷ����____������ĸ����
a.  b.
b. 
c.  d.
d. 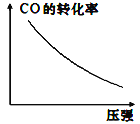
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1) 2016�й����ҹ�����ĸ����������8��052D������ˮ���ӿ����ҹ�������������ˮ�������IJ�����

����ͧ�ײ�Ϳ�к�Cu2O�ķ���ʴͿ�ϡ�Cu2O����________(����ĸ)��
a. ���ϲ��ϡ���������������
b. ���ǽ������ϡ���������
c. �л��߷��Ӳ���
���˶�����ĸ�У��ƼغϽ�(�����³�Һ̬)�����ڿ����ӷ�Ӧ�ѵ��ȼ������������ƼغϽ����ʵ�________(����ĸ)��
a. �۵�͡��е�ߡ�������b. �����Ժá�����������c. �ڿ��������ʲ��ȶ�
����ĸ�й�ˮ�ܵ������PE(����ϩ)���ϣ�����ϩ�Ļ�ѧʽΪ________________��
(2)������Ӫ���ḻ���������ʡ����ۡ���֬��Ҷ�ᡢά����C��Ҷ���أ�Ӫ���ɷ�λ��ͬ���߲�֮�ף�����Ϊ���߲˻ʹ�����

��ά����C����Ϊ________����һ֧ʢ��2 mL 2%������Һ���Թ��е���2�ε� ˮ����Һ����ɫ���ٵ���ά����C��ˮ��Һ����Һ��ɫ��Ϊ________����ʵ��˵��ά����C����________�ԡ�
����֬��������ˮ������ղ�����________(д����)���͡�
���������ɷ��п�����Ȼ��ɫ������________�������������________��
(3) 2016��9��4�գ�G20����ٿ���������ճ��ֳ��ɾ�����ɫ���Ʋ��������ɢ����գ��������������˳�������ˮ��������
��Ŀǰ�ҹ��������������ϵ������PM2.5��SO2��NO2��O3��CO��ָ�ꡣ����________����Ϊ����������������Ԫ�ף����������������������Ϊ________��
��NH3����ԭ����������ת��Ϊ����Ⱦ������ĿǰӦ����㷺�����������������ѳ�������д��NH3����ԭNO2��Ӧ�Ļ�ѧ����ʽ________________��
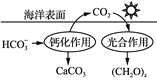
������CO2���ŷŶ��ڻ�������������Ҫ���塣�ں���̼ѭ���У���ͨ ����ͼ��ʾ��;����̼��д���ƻ����õ����ӷ���ʽ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
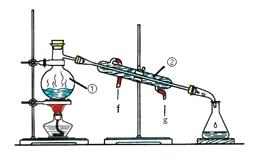
����Ŀ����ѧ��һ����ʵ��Ϊ������ѧ�ƣ���ѧ��ȡ�õķ�˶�ɹ�������ʵ�����Ҫ���÷ֲ����ġ��������ʵ��װ��ͼ�ش����⣺
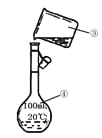
I II
��1��д������ͼ�����������ƣ���_______����______��
��2��������װ��I�������ᣨ�е�118�棩�������������е�77.1�棩�Ļ�����ȱ�ٵ�������__________��������������������е�ʵ�����������Ϊ_____��ʵ��ʱ����������ȴˮ�Ľ���Ϊ_______��ѡ����f������g������
��3����������250 mL 0.2 mol��L��1 NaCl��Һ��װ��II��ijͬѧת����Һ��ʾ��ͼ��ͼ������������ֱ���_______��_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������谷(�ṹ��ʽ��ͼ��ʾ)��һ����Ҫ�Ļ���ԭ�ϣ���������ȼ����ˮ���ˮ���߷��Ӻϳɵ�����һЩ��������ȴ��ţ���м��������谷�����������Ʒ�ĺ�����������˵����ȷ����
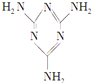
A. �����谷��һ�ֵ�����B. �����谷���Ǹ߷��ӻ�����
C. �����谷�����к���̼̼˫��D. �����谷�ķ���ʽΪC3H6N6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(ClO2)����������ˮ�������Դ���Ϊԭ������C1O2�Ĺ�����Ҫ�����������ξ��ƣ����������NaC1��Һ����C1O2����ȡ��������������ͼ��
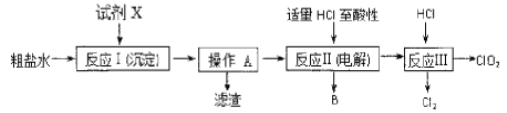
�ṩ���Լ�������Na2CO3��Һ������K2CO3��Һ��NaOH��Һ��BaCl2��Һ��Ba(NO3)2��Һ
��1����ʳ��ˮ�к���Ca2+��Mg2+��![]() �����ʡ����Ӳ���ʱ��������ˮ���ȼ���������Լ�X��ѡ���Լ�X���������Լ������μ�˳������Ϊ��__________________________(�ѧʽ)��
�����ʡ����Ӳ���ʱ��������ˮ���ȼ���������Լ�X��ѡ���Լ�X���������Լ������μ�˳������Ϊ��__________________________(�ѧʽ)��
��2�����������У���ʳ��ˮ���ض������µ��õ��������������ᷴӦ����C1O2����Ӧ���Ļ�ѧ����ʽΪ______________��
��3��ClO2�ܲ��ȶ������������ƣ�������ˮ���յõ�ClO2��Һ��Ϊ�ⶨ������Һ��ClO2�ĺ���������������ʵ�飺
����1��ȷ��ȡClO2��Һ10��00 mL��ϡ�ͳ�100 mL������
����2����ȡV1 mL�������뵽��ƿ�У�����������pH��2��0������������KI���壬ҡ�ȣ��ڰ�������30���ӡ�����֪ClO2+I��+H+==I2+Cl��+H2Oδ��ƽ��
����3���Ե�����Һ��ָʾ������c mol��L-1Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV2mL��(��֪��![]() )
)
��ȷ��ȡ10��00 mL ClO2��Һ�IJ���������__________________��
����������3�еζ��յ��������__________________________��
����ʵ����ʹ�õ�Na2S2O3����Һ�������������������ʣ���ʵ����_________(����ƫ��������ƫ����������Ӱ����)
�ܸ�����������ɼ����ԭC1O2��Һ��Ũ��Ϊ_________mol��L-1(�ú���ĸ�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com