
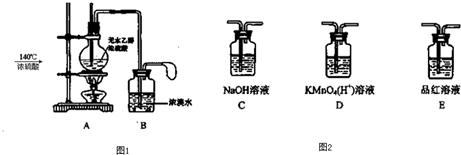
| 140℃ |
| 浓硫酸 |
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 颜色、状态 | 无色液体 | 无色液体 | 无色液体 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| 170℃ |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2、2 | B、2、4 |
| C、4、2 | D、4、5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 制取并收集干燥纯净的NH3 |
B、 除去NO2中的少量NO |
C、 将海带灼烧成灰 |
D、 分离乙酸乙酯和饱和碳酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
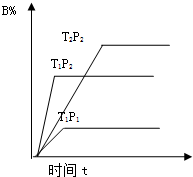 已知某可逆反应:mA(g)+nB(g)═pC(g)在密闭容器中进行,如图表示反应在不同时间t、温度T和压强P与反应物B在混合气体的体积分
已知某可逆反应:mA(g)+nB(g)═pC(g)在密闭容器中进行,如图表示反应在不同时间t、温度T和压强P与反应物B在混合气体的体积分| A、T1<T2 P1>P2m+n>p 正反应为吸热反应 |
| B、T1>T2 P2>P1 m+n<p 正反应为吸热反应 |
| C、T2>T1 P2>P1m+n<p 正反应为吸热反应 |
| D、T1>T2 P2>P1 m+n<p 正反应为放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com