
【题目】下列有关说法错误的是( )
A.![]() 为正极
为正极
B.①②中,捕获![]() 时碳元素的化合价未发生变化
时碳元素的化合价未发生变化
C.![]() 极电极反应式为
极电极反应式为![]()
D.由![]() 极反应
极反应![]()
![]() 可知,每转移
可知,每转移![]() 电子生成
电子生成![]()
【答案】D
【解析】
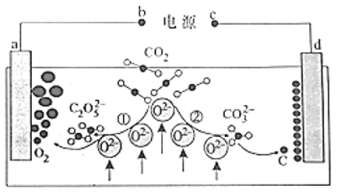
根据图片可知c极C2O52-→O2,发生氧化反应生成单质O2,所以a为阳极,d为阴极,阳极与电源正极相接、阴极与电源负极相接,即b极为电源正极、c极为电源负极,阳极反应式为2C2O52--4e-═4CO2↑+O2↑,阴极电极反应式为:CO32-+4e-═C+3O2-,以此解答该题。
A.根据上述分析,b极为电源正极,故A正确;
B.根据图示,①②中,CO2→C2O52或CO32时碳元素的化合价均为+4,没有变化,故B正确;
C.根据分析,d为阴极,阴极电极反应式为:CO32-+4e-═C+3O2-,故C正确;
D.根据分析,a为阳极,阳极反应式为2C2O52--4e-═4CO2↑+O2↑,转移1mol电子可捕获1molCO2,标准状况下体积为22.4L,题中未指明气体的状态条件,不能确定体积,故D错误;
答案选D。


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
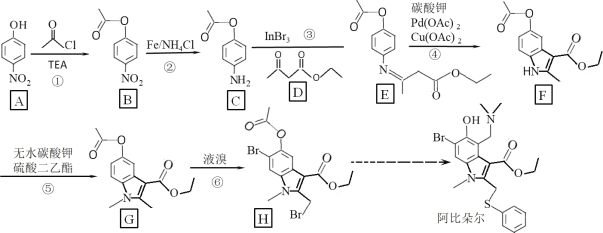
【题目】“阿比朵尔”是抗击新型冠状病毒潜在用药,其合成路线如图:
回答下列问题:
(1)有机物 A 含氧官能团名称_____;
(2)反应②、⑥反应类型分别是_____、_____;
(3)F 的分子式为_____;
(4)请写出反应③的化学反应方程式_____;
(5)M 是 B 的一种同分异构体,满足下列条件的同分异构体有_____种;其中核磁共振氢谱有 4 组峰,峰面积之比为 2:2:2:1 的结构简式_____;
①苯环上有 3 个取代基;
②能发生银镜反应;
③能发生水解反应,且 1 mol M 水解消耗4mol NaOH
(6)设计由甲苯和丙酮(![]() )为原料制备合成
)为原料制备合成![]() 路线_____。
路线_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个实验室制取氯气并以氯气为原料进行一系列反应的装置,回答下列问题。(已知:①MnO2+4HCl(浓) ![]() MnCl2+2H2O+Cl2↑,②Cl2+SO2+2H2O=2HCl+H2SO4,③ Ba(OH)2+CO2=BaCO3↓+H2O)
MnCl2+2H2O+Cl2↑,②Cl2+SO2+2H2O=2HCl+H2SO4,③ Ba(OH)2+CO2=BaCO3↓+H2O)

(1)写出a仪器的名称___;
(2)装置D产生白色沉淀现象的原因___________;
(3)E装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,其产物为CO2和HCl。试写出E中反应的化学方程式_______;
(4)F处的烧杯溶液中最终___(填“有”或“没有”)白色沉淀;
(5)F装置无法确认E处反应中有CO2产生,为了证明CO2的存在,要对F装置进行改造,下列装置符合要求的是___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中氧化剂是________(填化学式),过氧化钠(Na2O2)中氧元素化合价为_____。(填数字)
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:_________________。
②每生成1mol FeO42-转移___mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为_____mol。
(3)配平下面化学方程式,回答下列问题:____C +K2Cr2O7+H2SO4=K2SO4+CO2↑+Cr2(SO4)3+H2O。
①H2SO4在上述反应中表现出来的性质是(填选项编号)______。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
②若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为_____L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知还原性:Fe2+>Br-。向100mLFeBr2溶液中通入3.36L(标准状况)Cl2,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原溶液中FeBr2的物质的量浓度为( )
A. 2 mol·L-1 B. 1.5 mol·L-1 C. 1 mol·L-1 D. 0.75 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式____。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中P元素的化合价为___。
② 利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为__________(填化学式)。
③从分类来看,NaH2PO2属于______
a.正盐 b.酸式盐 c.钠盐 d.氧化物
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式_______Ba(H2PO2)2与H2SO4的离子方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向浓硫酸中分别加入下列三种固体,对实验现象的分析正确的是( )
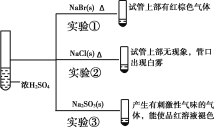
A.对比实验①和②可知还原性:Br->Cl-
B.对比实验①和③可知氧化性:Br2>SO2
C.对比实验②和③可知酸性:H2SO4>HCl>H2SO3
D.由实验可知浓硫酸具有强酸性、难挥发性、氧化性、脱水性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示实验回答下列问题:
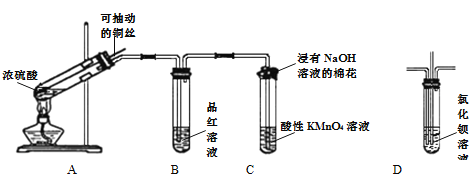
(1)装置A中试管内发生反应的化学方程式是_________________________________。
(2)根据装置B中的现象可以证明SO2具有__________性,反应一段时间后,将装置B中试管加热,可以观察到_______________________。
(3)装置C中试管口的棉花团上发生反应的离子方程式为________________________。
(4)如果将装置B换成装置D,并从直立导管中向氯化钡溶液中通入另一种气体,产生白色沉淀,则这种气体可能是_________________(填一种即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com