
【题目】化学反应过程中,不仅有物质的变化,同时还伴随有能量的变化。
(1)已知几种化学键的键能如表所示:
化学键 | Cl—Cl | F—F | Cl—F |
键能/ kJ·mol—1 | 242 | 159 | 172 |
则反应Cl2(g)+ 3F2(g)![]() 2ClF3(g) 的△H=_____________ kJ·mol—1 。
2ClF3(g) 的△H=_____________ kJ·mol—1 。
(2)如图是乙烷、二甲醚燃烧过程中的能量变化图。

请回答下列问题:
①乙烷的燃烧热ΔH=____kJ·mol-1。
②等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量__(填“多”或“少”)。
③根据题图写出二甲醚完全燃烧时的热化学方程式_____________。
(3)实验室用50mL 0.50mol·L﹣1HCl与50mL 0.55mol·L﹣1NaOH溶液测定中和热。
①若改用60mL HCl进行实验,与原实验相比,所放出的热量____(填“相等”或“不相等”,忽略实验本身误差,下同),所求中和热_____(填“相等”或“不相等”,)。
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所求中和热数值会___(填“偏大”“偏小”或“无影响”)。
【答案】 -313 -1 560 少 CH3OCH3(g)+3O2(g)![]() 2CO2(g)+3H2O(l) ΔH=-1 455 kJ/mol[或
2CO2(g)+3H2O(l) ΔH=-1 455 kJ/mol[或![]() CH3OCH3(g)+O2(g)
CH3OCH3(g)+O2(g)![]()
![]() CO2(g)+H2O(l) ΔH=-485 kJ/mol] 不相等 相等 偏小
CO2(g)+H2O(l) ΔH=-485 kJ/mol] 不相等 相等 偏小
【解析】(1)反应热的焓变△H=反应物总键能-生成物总键能,则反应Cl2(g)+ 3F2(g)![]() 2ClF3(g) △H=(242 kJ/mol)+(159 kJ/mol)×3-(172 kJ/mol)×6=-313kJ·mol—1,故答案为:-313;
2ClF3(g) △H=(242 kJ/mol)+(159 kJ/mol)×3-(172 kJ/mol)×6=-313kJ·mol—1,故答案为:-313;
(2)①依据原子守恒分析可知氢原子守恒,6a=2,a=![]() ,则根据图象分析可知,
,则根据图象分析可知, ![]() mol乙烷完全燃烧放热520kJ,所以1mol乙烷完全燃烧放热为520kJ×3=1560kJ,则乙烷的燃烧热△H=-1560kJ·mol-1,故答案为:-1560;
mol乙烷完全燃烧放热520kJ,所以1mol乙烷完全燃烧放热为520kJ×3=1560kJ,则乙烷的燃烧热△H=-1560kJ·mol-1,故答案为:-1560;
②因为液态乙烷转化为气态乙烷要吸热,所以等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物放出的热量少,故答案为:少;
③根据图象分析可知![]() mol二甲醚完全燃烧放热485kJ,则1mol二甲醚完全燃烧放热=485KJ×3=1455kJ,反应的热化学方程式为:CH3OCH3(g)+3O2(g)→2CO2(g)+ 3H2O(l) △H=-1455kJmol-1,故答案为:CH3OCH3(g)+3O2(g)→2CO2(g)+3H2O(l) △H=-1455kJmol-1;
mol二甲醚完全燃烧放热485kJ,则1mol二甲醚完全燃烧放热=485KJ×3=1455kJ,反应的热化学方程式为:CH3OCH3(g)+3O2(g)→2CO2(g)+ 3H2O(l) △H=-1455kJmol-1,故答案为:CH3OCH3(g)+3O2(g)→2CO2(g)+3H2O(l) △H=-1455kJmol-1;
(3)①中和反应中生成的水越多,放出的热量越多,若改用60mL HCl进行实验,与原实验相比,生成的水增大,所放出的热量与原来不相等,中和热是指生成1mol水放出的热量,因此所求中和热相等,故答案为:不相等;相等;
②氨水是弱碱,电离需要吸收热量,若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,放出的热量偏少,所求中和热数值偏小,故答案为:偏小。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】写出下列反应的热化学方程式:
(1)N2和H2反应生成34g NH3,放出92kJ热量____________________。
(2)1molCH4(g)在O2中完全燃烧生成CO2和H2O(g),放出890.3kJ热量________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列物质在水中的电离方程式
碳酸氢钠______________________________________________________________。
亚硫酸________________________________,______________________________。
(2)已知25 ℃时有关弱酸的电离平衡常数如下:HCN:4.9×10-10,H2CO3:K1=4.4×10-7 K2=4.7×10-11,向NaCN溶液中通入少量二氧化碳气体,写出发生反应的离子方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.合成硫酸的工业尾气可以直接排入大气
B.进入接触室的气体,必须先经净化、干燥
C.从沸腾炉中排出的炉渣可以作为肥料
D.在高温、高压下由SO2和O2合成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列用品的主要成分不正确的是
A | B | C | D | |
用品 | 水玻璃 | “84”消毒液 | 小苏打 | 光导纤维 |
主要成分 | Na2SiO3 | NaClO | NaHCO3 | Si |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列材料的主要成分为同主族元素形成的无机非金属材料的是( )
A.“玉兔二号”铁合金筛网轮B.医用聚乙烯无纺布防护服
C.酚醛树脂手柄D.大口径碳化硅反射镜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用海水可以提取溴和镁,提取过程如下。
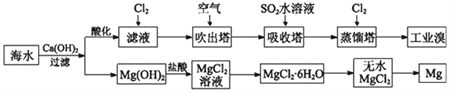
(1)提取溴的过程中,经过两次Br-→Br2转化的目的是_____________________,吸收塔中发生反应的离子方程式是___________________________________。用平衡移动原理解释通空气的主要目的是:____________________________。
(2)从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作是______、____、过滤、洗涤、干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com