
【题目】“84”消毒液在日常生活中使用广泛,该消毒液无色、有漂白作用,它的有效成分是( )
A.NaOHB.Na2O2C.NaClOD.KClO3
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】“低碳生活,绿色出行”已经成为很多人的生活理念。CO2的捕捉和利用也成为了科学家们积极探索的热门领域。回答下列问题:
(1)用CO2催化加氢可制取乙烯,其能量关系如图1,写出该反应的热化学方程式____________。

(2)以硫酸作电解质溶液,利用太阳能电池将CO2转化为乙烯的工作原理如图2。则A为电池的___极,N极的电极反应式为_________________________。
(3)用CO2催化加氢制取二甲醚的反应为:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
在恒容密闭容器中,均充入2mol.CO2和6molH2,分别以Ir和Ce作催化剂,反应进行相同的时间后测得的CO2的转化率a(CO2)随反应温度的变化情况如图3。

①用Ir和Ce作催化剂时,反应的活化能更低的是_______。
②a、b、c、d和e五种状态,反应一定达到平衡状态的是__________,反应的△H ___0(填“>”、“=”或“<”)。
③从状态a到c,CO2转化率不断增大的原因是________________________________。
④状态e时,a(CO2)= 50%,若保持容器容积为10L,则此时的平衡常数K=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式均为C5H10O2的两种有机物的结构简式如右图所示:
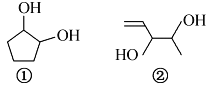
下列说法正确的是
A. 二者都能使Br2的CCl4溶液褪色
B. ①②分子中所有原子均可能处于同一平面
C. 等质量的①和②分别与足量钠反应生成等质量的H2
D. 与其互为同分异构体的酯有8种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O主要用于制造船底防污漆,它是一种鲜红色粉末,几乎不溶于水,在湿空气中逐渐氧化成黑色氧化铜。用含NaOH的Na2SO3溶液还原CuSO4制备Cu2O的工艺流程如下:

回答下列问题:
(1)流程中涉及的化学反应主要包括:
Ⅰ.Cu2++2OH-=Cu(OH)2↓;Ⅱ.生成CuOH;Ⅲ.2CuOH=Cu2O+H2O。
写出第Ⅱ步反应的离子方程式: ______________________________。
(2)其他反应条件相同时,测得反应时间和溶液的pH对Cu2O产率的影响如下图所示:
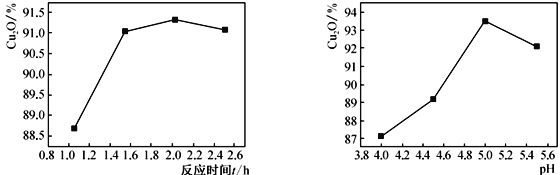
①反应时间超过2h时,Cu2O产率开始降低其原因是____________________________。
②pH<5时,Cu2O产率随pH减小而减小,产品中铜含量增加明显,其原因是______________________(用离子方程式说明)。
(3)为测定产品中Cu2O的含量,称取3.96 g产品于锥形瓶中,加入30mL硫酸酸化的Fe2(SO4)3溶液(足量),充分反应后用0.2000 mol·L-1标准KMnO4溶液滴定,至终点时消耗50mL标准液。
①滴定时应选用______(填“酸式”或“碱式”)滴定管,滴定终点的现象是______________________。
②产品与硫酸酸化的Fe2(SO4)3溶液反应的离子方程式为________________________________。
③假定杂质不参与反应,产品中Cu2O的质量分数为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)在25℃时,若100体积的某强酸溶液与1体积的某强碱溶液混合溶液中性,则混和前强酸pH1和强碱pH2应该满足的关系是pH1+pH2=
(2)某温度(t℃)时,水的离子积Kw=10﹣12 , 则该温度(填大于、小于或等于)25℃.将此温度下,将pH=2的硫酸溶液V1L与pH=11的氢氧化钠溶液V2L混合: ①若所得混合液为中性,则V1:V2= .
②若所得混合液的pH=10,则V1:V2= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质生产工艺的设计,必须牢牢抓住物质的性质,而推断化合物的化学性质,常从两个角度Ⅰ、物质的属类(如氧化物、酸、碱或盐等);Ⅱ、组成元素的化合价(是否处于最高价、中间价态或最低价)。请回答2
(1)已知SiO2是一种难溶于水的酸性氧化物,试写出一个化学方程式表示该物质具有的化学性质:__________________________________;
(2)已知,黄铜矿冶炼铜产生的炉渣含有Fe2O3、FeO、SiO2、Al2O3等多种氧化物,工业生产过程中可利用该炉渣制备Fe2O3。利用炉渣制备氧化铁的生产流程示意图如下:
![]()
①若盐酸浸泡后所得滤液用氯气处理,反应的离子方程式为______________________;经“足量的NaOH溶液”处理后,存在于炉渣中的铝元素最终以_____________形式被除去。
A.Al B.Al(OH)3 C.Al3+ D.[Al(OH)4]—
②现有a、稀硫酸 b、HNO3溶液 c、KSCN溶液 d、KMnO4溶液 e、NaOH溶液 f、碘水等试剂,为检验原炉渣中是否含有FeO,应该选择上述试剂中的_________________(填试剂对应的字母)。若存在FeO,将观察到的现象是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,充分燃烧一定量的丁烷放出热量Q kJ(Q>0),经测定完全吸收生成的CO2需消耗5 mol/L的KOH溶液100 mL,恰好生成正盐,则此条件下反应C4H10(g)+13/2O2(g)===4CO2(g)+5H2O(g)的ΔH为
A. +8Q kJ/mol B. +16Q kJ/mol
C. -8Q kJ/mol D. -16Q kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com