
(16分)化工工业中常用乙苯脱氢的方法制备苯乙烯。已知某温度下:
反应①:CO2(g)+H2(g) CO(g)+H2O(g),ΔH= +41.2 kJ/mol;
CO(g)+H2O(g),ΔH= +41.2 kJ/mol;
反应②: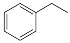 (g)
(g)
 (g)+H2(g),ΔH= +117.6 kJ/mol。
(g)+H2(g),ΔH= +117.6 kJ/mol。
①、②的化学反应平衡常数分别为K1、K2。
(1)请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式 。该反应的化学平衡常数K= (用K1、K2表示)。
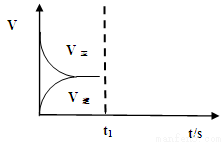
(2)恒温恒容条件下,反应①达到平衡后,t1时刻通入少量CO2。请
画出t1之后的正逆反应曲线,并作出标注。
(3)已知某温度下,Ag2SO4饱和溶液中c(Ag+)=0.04 mol/L,则该温度
下Ksp(Ag2SO4)= 。(保留两位有效数字)
(4)电解法制备高铁酸钠(Na2FeO4),总反应式为:Fe+2H2O+2OH-=FeO42-+3H2↑,电解质溶液选用NaOH溶液。该电解池阳极材料是 (写化学式);阳极的电极反应式为__ _________。
(1)CO2(g)+ (g)
(g) 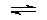
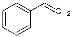 (g)+CO(g)+H2O(g),ΔH=+158.8 kJ/mol(4分;K= K1·K2(2分)
(g)+CO(g)+H2O(g),ΔH=+158.8 kJ/mol(4分;K= K1·K2(2分)
(2)(3分,曲线趋势正确2分,标示正确1分)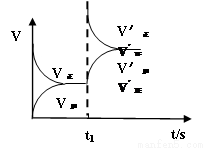
(3)3.2 x 10-5(3分)
(4)Fe(2分);Fe-6e+8OH- =FeO42-+4H2O(2分)
【解析】
试题分析:(1)①+②整理可得二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式是
CO2(g)+ (g)
(g) 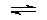
 (g)+CO(g)+H2O(g),ΔH=+158.8 kJ/mol;K1=
(g)+CO(g)+H2O(g),ΔH=+158.8 kJ/mol;K1=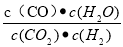 ;K2=
;K2=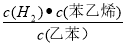 ;K=
;K=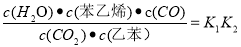 ;(2)恒温恒容条件下,反应①达到平衡后,t1时刻通入少量CO2,在此时刻,反应物的浓度突然增大,而生成物的浓度不变,所以V正增大,V逆不变,由于V正>V逆,所以平衡正向移动,经过一段时间,当V正=V逆时,反应达到新的平衡,则在t1之后的正逆反应曲线图为:
;(2)恒温恒容条件下,反应①达到平衡后,t1时刻通入少量CO2,在此时刻,反应物的浓度突然增大,而生成物的浓度不变,所以V正增大,V逆不变,由于V正>V逆,所以平衡正向移动,经过一段时间,当V正=V逆时,反应达到新的平衡,则在t1之后的正逆反应曲线图为: ;(3)已知某温度下,Ag2SO4饱和溶液中c(Ag+)=0.04 mol/L,c(SO42-)=0.02mol/L则该温度下Ksp(Ag2SO4)= c2(Ag+)·c(SO42-)=0.042×0.02=3.2 ×10-5. (4)电解法制备高铁酸钠(Na2FeO4),总反应式为:Fe+2H2O+2OH-=FeO42-+3H2↑,电解质溶液选用NaOH溶液。由于Fe失去电子变为FeO42-,所以该电解池阳极材料是Fe;阳极的电极反应式为Fe-6e+8OH- =FeO42-+4H2O。
;(3)已知某温度下,Ag2SO4饱和溶液中c(Ag+)=0.04 mol/L,c(SO42-)=0.02mol/L则该温度下Ksp(Ag2SO4)= c2(Ag+)·c(SO42-)=0.042×0.02=3.2 ×10-5. (4)电解法制备高铁酸钠(Na2FeO4),总反应式为:Fe+2H2O+2OH-=FeO42-+3H2↑,电解质溶液选用NaOH溶液。由于Fe失去电子变为FeO42-,所以该电解池阳极材料是Fe;阳极的电极反应式为Fe-6e+8OH- =FeO42-+4H2O。
考点:考查热化学方程式的书写、化学平衡常数的表达式及关系、沉淀溶解平衡、电解池反应原理的知识。


科目:高中化学 来源:2015届江苏省高三上学期摸底考试化学试卷(解析版) 题型:选择题
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g) 2XY3(g) △H=-92.6kJ·mol-1
2XY3(g) △H=-92.6kJ·mol-1
起始时各物质物质的量如下表所示:
容器 编号 | 起始时各物质物质的量/mol | ||
X2 | Y2 | XY3 | |
① | 1 | 3 | 0 |
② | 0.6 | 1.8 | 0.8 |
达到平衡后,①容器中XY3的物质的量为0.5mol。下列叙述正确的是
A.容器①、②中反应的平衡常数不相等
B.达平衡时,容器②中XY3的物质的量浓度为2mol·L—1
C.容器①中反应达到平衡时放出的热量为23.15 kJ
D.容器②中反应达到平衡时放出热量
查看答案和解析>>
科目:高中化学 来源:2015届广西桂林市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A、温度相同、体积相同的O2(g)和N2(g)分子数相同
B、等温等压下,SO2气体与CO2气体的密度之比等于16∶11
C、温度和容积相同的两气罐中分别盛有5mol O2(g)和2 mol N2(g),两容积中的压强之比等于5∶2
D、等温等压条件下, 5 molO2(g)和2 molH2 (g)的体积之比等于5∶2
查看答案和解析>>
科目:高中化学 来源:2015届广东肇庆中学高三8月考理综化学试卷(解析版) 题型:实验题
(16分)“向海洋进军”,已成为世界许多国家发展的战略口号,海水中通常含有较多的Ca2+、Mg2+、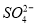 等杂质离子,以海盐为原料的氯碱厂电解饱和食盐水制取NaOH的工艺流程如下:
等杂质离子,以海盐为原料的氯碱厂电解饱和食盐水制取NaOH的工艺流程如下:
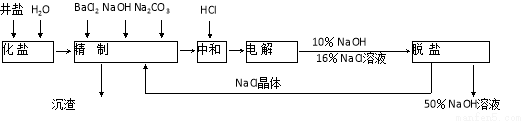
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极的电极反应式为 ;
(2)电解过程的总反应的化学方程式_________________________________________。
(3)电解槽阳极产物可用于_____________________________(至少写出两种用途)。
(4)工业食盐含Ca2+、Mg2+等杂质,精制过程中除去这2种离子所发生反应的离子方程式为: 。
(5)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(6)为了有效除去Ca2+、Mg2+、SO42-加入试剂的合理顺序为
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(7)已知NaOH、NaCl在水中的溶解度数据如下表:
温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
NaOH /g | 109 | 118 | 129 | 146 | 177 | 300 | 313 | 318 | 337 |
NaCl/ g | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
根据上述数据,脱盐工序中利用通过 、 (填操作名称)除去NaCl。
查看答案和解析>>
科目:高中化学 来源:2015届广东肇庆中学高三8月考理综化学试卷(解析版) 题型:选择题
下列陈述Ⅰ、Ⅱ都正确并且有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 非金属性:Cl>S | 酸性:HClO> H2SO3 |
B | SO2有氧化性 | SO2能使酸性KMnO4溶液褪色 |
C | NH3.H2O为一元弱碱 | 含有NH4+的水溶液均显弱碱性 |
D | 锌的金属性比铁强 | 海轮外壳上装锌块可减缓腐蚀 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省韶关市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
下列有关物质的性质和该性质的应用均正确的是
A.氯气具有酸性,可与烧碱或石灰乳反应制备含氯消毒剂
B.浓硫酸具有强氧化性,常温下可用铝罐盛装
C.氢氟酸具有弱酸性,可用氢氟酸雕刻玻璃
D.过氧化钠具有强氧化性,可用作潜水艇中氧气的来源
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三8月月考化学试卷(解析版) 题型:填空题
(16分)甲醇是一种可再生燃料。在容积为2L的密闭容 器中进行反应:CO(g)+2H2(g) CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示。
CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示。

(1)该反应的△H 0 (填>、<或=)
(2)300℃时,0-t1 min内 CH3OH的平均生成速率为
(3)若要提高甲醇的产率,可采取的措施有_______ 。(填字母)
A 缩小容器体积B 降低温度
C 升高温度 D 使用合适的催化剂
E.甲醇从混合体系中分离出来
(4)300℃时,CO、H2的起始物质的量分别为2mol和3mol,若图中n1数据为0.5mol,试计算300℃下,该反应的平衡常数(写出计算过程,保留两位有效数字)
(5)工业上也可以用CO2和H2反应制得甲醇。在2×105Pa、300℃的条件下,若有440g CO2与H2恰好完全反应生成甲醇和水,放出495kJ的热量,试写出该反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省深圳市高三上学期第一次五校联考理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值。下列说法正确的是(用到的相对原子质量:H 1 O16 Al27)
A.18g 2H2O含有10NA个电子
B.1mol苯含有6NA个C-H键
C.常温常压下,22. 4L NH3约含有NA个NH3分子
D.27 g铝片投入足量浓H2SO4中生成1.5NA个SO2分子
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高三九月份化学月考试卷(解析版) 题型:填空题
(12分)水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为_____ _____;
(2)写出与H2O分子互为等电子体的微粒__ ________(填2种)。
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是_ ____
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是__ ___(请用相应的编号填写)
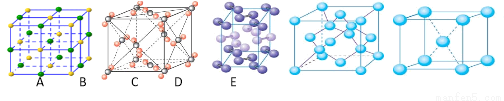
(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能” 是_________kJ/mol;
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com