
【题目】氢能是一种极具发展潜力的清洁能源.以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法.其反应过程如图所示:
完成下列填空
(1)反应Ⅰ的化学方程式是 . 反应Ⅰ得到的产物用I2进行分离.该产物的溶液在过量I2的存在下会分成两层﹣﹣含低浓度I2的H2SO4层和高浓度的I2的HI层.
(2)根据上述事实,下列说法正确的是(选填序号).a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
(3)辨别两层溶液的方法: ,
(4)经检测,H2SO4层中c(H+):c(SO ![]() )=2.06:1.其比值大于2的原因是 . 反应Ⅱ:2H2SO4(l)→2SO2(g)+O2(g)+2H2O(g)﹣1100kJ 它由两步反应组成:
)=2.06:1.其比值大于2的原因是 . 反应Ⅱ:2H2SO4(l)→2SO2(g)+O2(g)+2H2O(g)﹣1100kJ 它由两步反应组成:
i.H2SO4(l)→SO3(g)+H2O(g)﹣177kJ ii.SO3(g)分解.
L(L1、L2),X可分别代表压强或温度.图2表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系.
(5)X代表的物理量是 , 推断的依据是 .
(6)判断L1和L2的大小,并简述理由 .
【答案】
(1)SO2+2H2O+I2=H2SO4+2HI
(2)ac
(3)观察颜色|颜色深的为HI层,颜色浅的为硫酸层
(4)硫酸层中含少量的HI,且HI电离出氢离子
(5)压强;增大压强平衡逆向进行,三氧化硫转化率减小
(6)L1<L2 , 分解反应为吸热反应,温度高,三氧化硫转化率大
【解析】解:(1)由图可知,反应I为二氧化硫与碘发生氧化还原反应生成硫酸和HI,该反应为SO2+2H2O+I2=H2SO4+2HI,所以答案是:SO2+2H2O+I2=H2SO4+2HI;(2)a.两层溶液的密度存在差,才出现上下层,故a正确;b.加I2前,H2SO4溶液和HI溶液互溶,与分层无关,故b错误;c.I2在HI溶液中比在H2SO4溶液中易溶,则碘在不同溶剂中溶解性不同,类似萃取,与分层有关,故c正确;所以答案是:ac;(3)辨别两层溶液的方法是观察颜色,颜色深的为HI层,颜色浅的为硫酸层,所以答案是:观察颜色,颜色深的为HI层,颜色浅的为硫酸层;(4)H2SO4层中c(H+):c(SO42﹣)=2.06:1.其比值大于2的原因是硫酸层中含少量的HI,且HI电离出氢离子,所以答案是:硫酸层中含少量的HI,且HI电离出氢离子;(5)由图可知,X越大,三氧化硫转化率越低,升高温度转化率增大不符合,增大压强平衡逆向进行,三氧化硫转化率减小,图象符合X表示压强,所以答案是:压强,增大压强平衡逆向进行,三氧化硫转化率减小;(6)由2SO3(g)=2SO2(g)+O2(g)△H>0,温度高,转化率大,图中等压强时L2对应的转化率大,则L1<L2 , 所以答案是:L1<L2 , 分解反应为吸热反应,温度高,三氧化硫转化率大.
【考点精析】掌握化学平衡状态本质及特征是解答本题的根本,需要知道化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


科目:高中化学 来源: 题型:
【题目】25°C时,某溶液中由水电离出的c(OH﹣)=1×10﹣13mol/L,该溶液中一定不能大量共存的离子组是( )
A.NH ![]() 、Fe3+、SO
、Fe3+、SO ![]() 、Cl﹣
、Cl﹣
B.CO ![]() 、PO
、PO ![]() 、K+、Na+
、K+、Na+
C.Na+、SO ![]() 、NO
、NO ![]() 、Cl﹣
、Cl﹣
D.HPO ![]() 、Na+、HSO
、Na+、HSO ![]() 、K+
、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质转化关系中, 必须加入适当氧化剂才能实现的是( )
A. PCl3→PCl5 B. MnO4—→Mn2+ C. SO42—→SO32— D. CO2→CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】广东正在建设成为海洋强省。下列说法不正确的是( )
A.从海带中提取碘单质的过程涉及氧化还原反应
B.往淡水中加入NaCl等配成人造海水,可用于海产品的长途运输
C.赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的
D.海洋经济专属区的资源开发可获得Fe、Co、K Au、Mg、B等金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚芳酯(PAR)是分子主链上带有苯环和酯基的特种工程塑料,在航空航天等领域具有广泛应用.如图是利用乙酰丙酸 ![]() 合成聚芳酯E的路线:
合成聚芳酯E的路线: 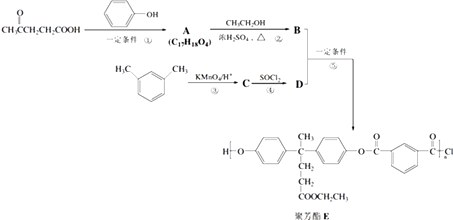
已知: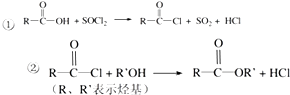
(1)乙酰丙酸中含有的官能团是羰基和(填官能团名称).
(2)D的结构简式为 .
(3)下列关于有机物B的说法错误的是a.能发生取代反应 b.能与浓溴水反应c.能发生消去反应 d.能与H2发生加成反应
(4)A→B的化学方程式为 .
(5)C的分子式为 , F是符合下列条件的C的同分异构体①能发生银镜反应 ②能与NaHCO3溶液反应
③分子中有四种化学环境不同的氢原子 ④苯环上只有2个取代基,无 ![]() 结构
结构
写出其中任一种与足量NaOH溶液共热反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银锌电池是一种常见化学电源,其反应原理:Zn+Ag2O+H2O===Zn(OH)2+2Ag,其工作示意图如下。下列说法不正确的
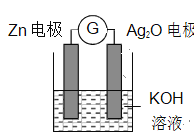
A. K+向正极移动
B. Ag2O 电极发生还原反应
C. Zn 电极的电极反应式:Zn-2eˉ+2OHˉ===Zn(OH)2
D. 放电前后电解质溶液的碱性保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的是( ) 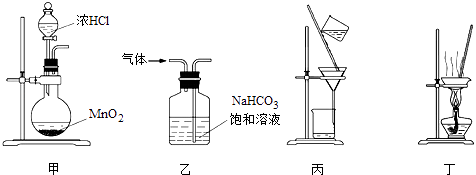
A.用装置甲制取氯气
B.用装置乙除去氯气中混有的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl24H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L0.3mol/L的NaOH溶液中,通入4.48LCO2(标准状况),反应后所得溶液中离子的浓度之间有一些等量关系,例如:.c(Na+)+c(H+)=c(HCO3﹣)+2c(CO32﹣)+c(OH﹣),另外对此溶液中存在的离子按浓度由大到小排序为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com