
下图表示反应X(g) 4Y(g)+Z(g),ΔH<0,在某温度时X的浓度随时间变化的曲线:
4Y(g)+Z(g),ΔH<0,在某温度时X的浓度随时间变化的曲线:
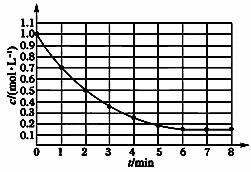
下列有关该反应的描述正确的是( )
A.第6min后,反应就终止了
B.X的平衡转化率为85%
C.若升高温度,X的平衡转化率将大于85%
D.若降低温度,v正和v逆将以同样倍数减小
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
在密闭容器中进行反应:2A+3B 2C。开始时C的浓度为amol·L-1,2min后C的浓度变为2amol·L-1,A和B的物质的量浓度均变为原来的1/2,则下列说法中不正确的是
2C。开始时C的浓度为amol·L-1,2min后C的浓度变为2amol·L-1,A和B的物质的量浓度均变为原来的1/2,则下列说法中不正确的是
A.用B表示的反应速率是0.75a mol/(L·min)
B.反应开始时,c(B)=3amol·L-1
C.反应2min后,c(A)=0.5amol·L-1
D.反应2min后,c(B)=1.5amol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应X+Y===M+N为放热反应,对该反应的下列说法中正确的是( )
A.X的焓一定高于M
B.Y的焓一定高于N
C X和Y的总焓一定高于M和N的总焓
D.因为该反应为放热反应,故不必加热反应就可发生
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中发生下列反应aA(g ) cC(g)+d D(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
) cC(g)+d D(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
A.A的转化率变大 B.平衡向正反应方向移动
C.a <c+d D.D的体积分数变大
查看答案和解析>>
科目:高中化学 来源: 题型:
降低大气中CO2的含量及有效地开发利用 CO2,目前工业上有一种方法是用CO2来生产甲醇燃料。为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH =-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH =-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)从反应开始到平衡,氢气的平均反应速率v(H2)=________mol/(L·min);
(2)氢气的转化率=________;
(3)该反应的平衡常数为________(保留小数点后2位);
(4)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是________。
A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出去
D.再充入1mol H2
(5)当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2,则c1________c2的关系(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于ⅦA族元素的叙述正确的是 ( )
A.ⅦA族元素是同周期中原子半径最大的元素
B.ⅦA族元素是同周期中非金属性最弱的元素
C.ⅦA族元素的最高正价都是+7价
D.ⅦA族元素其简单阴离子的核外电子层数等于该元素所在的周期数
查看答案和解析>>
科目:高中化学 来源: 题型:
有机化合物有不同的分类方法,下列说法正确的是( )
①从组成元素分:烃,烃的衍生物
②从分子中碳骨架形状分:链状有机化合物,环状有机化合物
③从官能团分:烯烃、炔烃、卤代烃、醇、酚、醛、酮、羧酸、酯等
A.①③ B.①② C.①②③ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)甲烷通常用来作燃料,其燃烧反应的化学方程式是 。
(2) 若用甲烷—氧气构成燃料电池,电解质溶液为KOH溶液,试写出该电池的
正极的电极反应式 ;
负极的电极反应式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com