
【题目】(一)有以下微粒:①N2H4 ②P4 ③H2O ④N2 ⑤H3O+ ⑥NH4+ ⑦CO2 ⑧H2O2
(填编号)
(1)既有极性键又有非极性键的是 ;(2)既有σ键又有π键的是 ;
(3)微粒中不含孤电子对的是____________;(4)立体构型呈正四面体的是____________;
(5)⑤和⑧的电子式分别为 和 ;
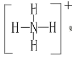
(6)⑥和⑦的结构式分别为 和 ;
(二)以下反应均为放热反应,根据热化学方程式,比较 △H1 和 △H2 的大小
① I2(g)+ H2(g)=2HI(g) △H1;I2(s)+ H2(g)=2HI(g) △H2,则△H1 △H2
② H2(g)+Cl2(g)=2HCl(g) △H1;H2(g)+Br2(g)=2HBr(g) △H2,则△H1 △H2
【答案】(一)(1)①⑧(2)④⑦ (3)⑥ (4)②⑥
(5)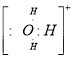
![]() (6)
(6) 、
、![]()
(二)① < ②<
【解析】
试题分析:(1)同种元素的原子间形成非极性键、不同元素的原子形成极性键,既有极性键又有非极性键的是①⑧;
(2)单键是σ键,双键含有1个σ键和1个π键,三键含有1个σ键和2个π键;既有σ键又有π键的是④⑦;
(3)根据价层电子对互斥理论可知,N2H4中中心原子N原子含有的孤电子对数是(5-3×1)÷2=1;P4中心原子P原子含有的孤电子对数是(5-3×1)÷2=1;水中中心原子氧原子含有的孤电子对数是(6-2×1)÷2=2;N2每个N原子含有1对孤对电子;H3O+中心原子氧原子含有的孤电子对数是(6+3-1)÷2-3=1;NH4+中心原子氧原子含有的孤电子对数是(5+4-1)÷2-4=0;CO2中心原子氧原子含有的孤电子对数是0;H2O2中心原子氧原子含有的孤电子对,微粒中不含孤电子对的是⑥;
(4)立体构型呈正四面体的是②⑥;
(5)⑤和⑧的电子式分别为![]() 和
和![]() ;
;
(6)⑥和⑦的结构式分别为![]() 和
和![]()
(二)① 碘蒸汽的能量大于固体碘,气态碘放出的能量大,所以△H1 <△H2 ②氯化氢的键能大于溴化氢,所以△H1 <△H2。


科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。下列关于某些化学过程的描述中:
①1mol 金刚石中含有的共价键数为4NA ; ②在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA ; ③密闭容器中2mol NO与1molO2充分反应,最终产物的分子数为2NA ; ④将0.1 mol CO2通入足量NaOH溶液中,则反应后溶液中阴离子数目为0.1NA ;⑤含NA个Na+的Na2O2溶于1L水中,Na+物质的量浓度为1mol·L-1,错误的是( )
A.①③④ B.②③⑤ C.②④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是
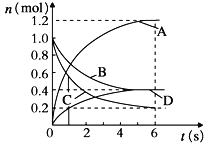
A.该反应的化学方程式为3B+4D![]() 6A+2C
6A+2C
B.反应进行到1 s时,v(A)=v(D)
C.反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D.反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于海水资源综合利用的说法中,不正确的是( )
A.从海水中富集镁元素可用Ca(OH)2沉淀法
B.海水淡化的方法主要有蒸馏法、离子交换法、电渗析法
C.从海水中提取溴单质的过程中用氯气做还原剂
D.从海水中获得粗盐可用蒸发结晶法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蛋白质的性质在生活中有许多实际应用.请在下表“性质”一栏中表述的蛋白质性质填空.
实例 | 性质 |
(1)紫外线消毒 | 变性 |
(2)蛋白质遇浓硝酸变黄 | |
(3)误食了重金属离子,可以立即喝大量的牛奶来缓解毒性 | |
(4)鸡蛋清溶液中加入少量饱和的硫酸铵溶液出现沉淀 | |
(5))常用酒精清洗伤口 | |
(6)蒸煮鸡蛋食用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

(1)写出下列仪器的名称:①____________,②____________,④____________。
(2)仪器①~④中,使用时必须检查是否漏水的是________________(填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器____________,将仪器补充完整后进行的实验操作的名称为____________;②的进水口是____________(填“f”或“g”)。
(4)现需配制250mL、0.2 mol·L-1NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误操作:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”的核心是在化学反应过程中或化工生产中,尽量减少使用或彻底消除有害物质,下列做法中,符合“绿色化学”理念的是 ( )
A.生产和使用剧毒农药 B.化工厂产生的废气向高空排放
C.利用氢气作高能燃料 D.造纸厂用二氧化硫进行纸浆漂白
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列说法正确的是
A.在标准状况下,22.4LCCl4中含5 NA 个原子
B.0.1mol铁与足量的盐酸完全反应,铁失去的电子数为0.1 NA
C.1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1 NA
D.将100mL0.1mol/L的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.01 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH标准溶液的配制和标定时,需经过NaOH溶液的配制、基准物质H2C2O4·2H2O的称量以及用NaOH溶液滴定等操作。下列操作正确的是( )
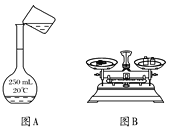
A. 用图A所示的方法转移NaOH溶液到容量瓶中
B. 用图B所示的装置准确称得0.15 g H2C2O4·2H2O
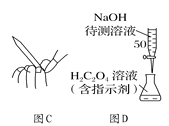
C. 用图C所示的操作排除碱式滴定管中的气泡
D. 用图D所示的装置,用NaOH待测液滴定H2C2O4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com