
【题目】NA表示阿伏加德罗常数的值。下列关于某些化学过程的描述中:
①1mol 金刚石中含有的共价键数为4NA ; ②在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA ; ③密闭容器中2mol NO与1molO2充分反应,最终产物的分子数为2NA ; ④将0.1 mol CO2通入足量NaOH溶液中,则反应后溶液中阴离子数目为0.1NA ;⑤含NA个Na+的Na2O2溶于1L水中,Na+物质的量浓度为1mol·L-1,错误的是( )
A.①③④ B.②③⑤ C.②④⑤ D.全部
【答案】D
【解析】
试题分析:①金刚石中C有4个共价键,因此根据均摊法,1个碳原子真正有2个共价键,因此1mol金刚石含有共价键的物质的量为2mol,故错误;②2Na2O2+2H2O=4NaOH+O2↑,生成1molO2转移电子2mol,因此生成0.1molO2转移电子的物质的量为0.2mol,故错误;③发生的反应 有2NO+O2=2NO2,2NO2![]() N2O4,因此产物的分子的物质的量小于2mol,故错误;④CO2通入足量的NaOH溶液中产物是Na2CO3,CO32-发生水解,阴离子物质的量小于0.1mol,故错误;⑤物质的量浓度是单位体积的溶液中含有溶质的物质的量,因此体积为溶液的体积,题目中1L是水的体积,不是溶液体积,故错误;综上所述,选项D正确。
N2O4,因此产物的分子的物质的量小于2mol,故错误;④CO2通入足量的NaOH溶液中产物是Na2CO3,CO32-发生水解,阴离子物质的量小于0.1mol,故错误;⑤物质的量浓度是单位体积的溶液中含有溶质的物质的量,因此体积为溶液的体积,题目中1L是水的体积,不是溶液体积,故错误;综上所述,选项D正确。


科目:高中化学 来源: 题型:
【题目】已知:①N2(g)+O2(g)=2NO(g) △H1=+180kJ·mol-1
②N2(g)+3H2(g)![]() 2NH3(g) △H2=-92.4 kJ·mol-1
2NH3(g) △H2=-92.4 kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) △H3=-483.6 kJ·mol-1

下列说法正确的是
A.反应②中的能量变化如图所示,则△H2=E1-E3
B.N2的燃烧热为180 kJ·mol-1
C.由反应②知在温度一定的条件下,在一恒容密闭容器中通入1molN2和3molH2,反应后放出的热量为Q1kJ,则Q1=92.4
D.氨的催化氧化反应为4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-906 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是( )
被提纯物质 | 除杂试剂 | 分离方法 | |
A | 淀粉(NaCl) | H2O | 渗析 |
B | Al2O3(SiO2) | NaOH溶液 | 过滤 |
C | CO2(CO) | O2 | 点燃 |
D | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1mol/L
B. 从1L2mol/L的H2SO4溶液中取出0.5L,该溶液溶质物质的量浓度为1mol/L
C. 0.5L2mol·L-1的BaCl2溶液中,Ba2+和Cl-的总数为3×6.02×1023
D. 10g98%的硫酸(密度为1.84g·cm-3)与10mL18.4mol·L-1的硫酸的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中c (OH-)之比为( )
A.大于10 B.小于10 C.等于10 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A可以作水果的催熟剂,D是食醋的主要成分。相关的转化关系如下:
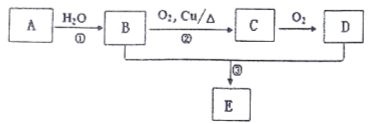
请回答下列问题:
(1)A的结构简式为 ,反应①的反应类型是 。
(2)C的名称是 。
(3)反应③的化学方程式为 ,该反应类型是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.稀硫酸滴在银片上:2Ag+2H+===2Ag++H2↑
B.稀硫酸与氢氧化钡溶液混合:SO![]() +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C.稀硝酸滴在大理石上:CaCO3+2H+===Ca2++H2CO3
D.氧化铁与稀盐酸混合:Fe2O3+6H+===2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】细胞的结构和生命活动的物质基础是构成细胞的各种化合物,下列有关这些化合物功能的叙述,正确的是
A. 生命活动都由蛋白质调节
B. 干种子因缺乏自由水不能萌发
C. 多糖是植物细胞的能源物质
D. 生物的遗传物质是DNA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)有以下微粒:①N2H4 ②P4 ③H2O ④N2 ⑤H3O+ ⑥NH4+ ⑦CO2 ⑧H2O2
(填编号)
(1)既有极性键又有非极性键的是 ;(2)既有σ键又有π键的是 ;
(3)微粒中不含孤电子对的是____________;(4)立体构型呈正四面体的是____________;
(5)⑤和⑧的电子式分别为 和 ;
(6)⑥和⑦的结构式分别为 和 ;
(二)以下反应均为放热反应,根据热化学方程式,比较 △H1 和 △H2 的大小
① I2(g)+ H2(g)=2HI(g) △H1;I2(s)+ H2(g)=2HI(g) △H2,则△H1 △H2
② H2(g)+Cl2(g)=2HCl(g) △H1;H2(g)+Br2(g)=2HBr(g) △H2,则△H1 △H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com