
【题目】一定温度下,水溶液中H+的浓度变化曲线如图所示,下列说法正确的是( )
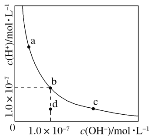
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl3可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
【答案】C
【解析】
A.温度升高,水的离子积常数增大,水溶液中,氢离子和氢氧根离子浓度都增大,将不在曲线上,A选项错误;
B.b点c(H+)=c(OH-)=1.0×10-7,故Kw=c(H+)·c(OH-)=1.0×10-7×1.0×10-7=1.0×10-14,B选项错误;
C.加入FeCl3,由于氯化铁为强酸弱碱盐,在溶液中Fe3+水解结合水电离出的OH-,促进水的电离平衡右移,最终使溶液中氢离子浓度增大,氢氧根离子浓度减小,可以由b到a点,符合图象变化趋势,C选项正确;
D.由c点到d点,水的离子积常数减小,温度不变,Kw不变,故不能利用稀释使其形成此变化,D选项错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】某二次电池充、放电的化学方程式为:2K2S2+KI3![]() K2S4+3KI,与其它设备连接的电路如图示。当闭合开关K时,X附近溶液先变红.则下列说法正确的是
K2S4+3KI,与其它设备连接的电路如图示。当闭合开关K时,X附近溶液先变红.则下列说法正确的是
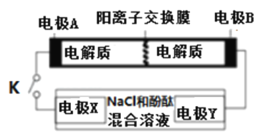
A.K+从右到左通过阳离子交换膜
B.A的电极反应式为:3I﹣﹣2e﹣=I3﹣
C.当有0.1molK+通过离子交换膜,X电极上产生标准状况的气体1.12L
D.电池充电时,B电极要与外电源的正极相连,电极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KI用于分析试剂、感光材料制药和食品添加剂等。
制备原理如下:反应① 3I2+6 KOH =a KIO3+5KI+3H2O
反应② 3H2S+KIO3=3S↓+KI+3H2O

按照下列实验过程,请回答有关问题。
(1)启普发生器中发生的化学方程式为______________________,用该装置还可以制备___________(填一种气体化学式)。
(2)关闭启普发生器活塞,打开滴液漏斗的活塞,滴入30%的KOH溶液,待观察到______________________(填现象),停止滴人KOH溶液;然后______________________(填操作),待KIO3混合液和NaOH溶液气泡速率接近相同时停止通气。
(3)滴人硫酸溶液,并对KI混合液水浴加热,其目的是______________________。
(4)把KI混合液倒入烧杯,加入碳酸钡,在过滤器中过滤,过滤得到的沉淀中除含有过量碳酸钡外,还有硫酸钡和___________,其中加入碳酸钡的作用是______________________。合并滤液和洗液,蒸发至析出结晶,滤出经于燥得成品。
(5)如果得到3.2g硫单质,则理论上制得的KI为___________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,NaCN溶液中CN-、HCN浓度所占分数(δ)随pH变化的关系如下图甲所示。向10 mL 0.01 mol·L-1 NaCN溶液中逐滴加入0.01 mol·L-1的盐酸,其pH变化曲线如下图乙所示。
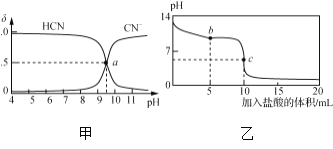
下列溶液中微粒的物质的量浓度关系一定正确的是( )
A. 图甲中pH=7的溶液:c(Cl-)=c(HCN)
B. 图甲中a点的溶液:c(CN-)<c(Cl-)
C. 图乙中b点的溶液:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+)
D. 图乙中c点的溶液:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-)
查看答案和解析>>
科目:高中化学 来源: 题型:
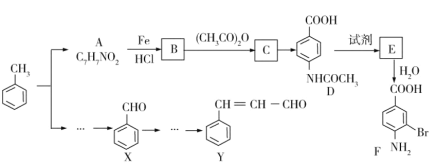
【题目】两种重要的有机化工合成中间体F和Y可用甲苯为主要原料采用路线制得:
已知:①![]()
![]()
![]()
②2CH3CHO![]() CH3CH(OH)CH2CHO
CH3CH(OH)CH2CHO![]() CH3CH=CHCHO
CH3CH=CHCHO
③![]() 高温、高压可以与NaOH发生取代反应
高温、高压可以与NaOH发生取代反应
请回答下列问题:
(1)写出X的名称:__________________。
(2)写出![]() →A的化学方程式:_______________________________________。
→A的化学方程式:_______________________________________。
(3)D→E的试剂为:______________________。
(4)写出1molF在高温、高压下与NaOH的反应:____________________________________。
(5)写出符合下列条件A的同分异构体的一种结构简式:________________。
①苯环上只有两种不同化学环境的氢原子②能发生银镜反应
(6)根据题中所给信息,设计由有机物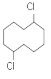 合成
合成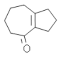 流程图其他无机试剂任选。_______________
流程图其他无机试剂任选。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度T1时,Ag2SO4在水中的沉淀溶解曲线如图实线所示。下列说法正确的是( )

A. T1时,Ag2SO4的溶度积常数(Ksp)为1×10-3
B. T1时,0.02 mol/L的AgNO3溶液与0.2 mol/L的Na2SO4溶液等体积混合不会生成沉淀
C. b点表示T1时Ag2SO4的饱和溶液,稀释时可以使溶液由b点变到a点
D. 仅通过降温的方法,可以使T2时的饱和溶液从c点变到T1时b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:图甲是由某温度下![]() 、
、![]() 分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化图.图乙是常温下向100mL
分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化图.图乙是常温下向100mL![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液,混合溶液的pH变化图.如图所示与推测的结论相符的是
溶液,混合溶液的pH变化图.如图所示与推测的结论相符的是
图甲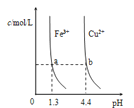 图乙
图乙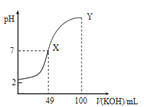
A.由图甲知:![]()
B.由图甲知:a、b点溶液中![]() ,b点的大
,b点的大
C.由图乙知:HA为强酸
D.由图乙知:Y点对应的溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范并能达到实验目的是
选项 | 实验操作 | 实验目的 |
A | 在一定条件下,向混有少量乙烯的乙烷中通入氢气 | 除去乙烷中的乙烯 |
B | 用玻璃棒蘸取待测液,点在干燥的pH试纸中部,片刻后与标准比色卡比较并读数 | 粗略测定NaClO溶液的pH |
C | 将0.1mol/LMgSO4溶液滴入到2mLNaOH溶液中至不再有沉淀生成,再滴入0.1mol/LCuSO4溶液 | 比较Mg(OH)2和Cu(OH)2的Ksp大小 |
D | 向亚硫酸钠溶液中滴加硝酸钡和稀硝酸 | 检验亚硫酸钠溶液是否变质 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com