
【题目】某温度T1时,Ag2SO4在水中的沉淀溶解曲线如图实线所示。下列说法正确的是( )

A. T1时,Ag2SO4的溶度积常数(Ksp)为1×10-3
B. T1时,0.02 mol/L的AgNO3溶液与0.2 mol/L的Na2SO4溶液等体积混合不会生成沉淀
C. b点表示T1时Ag2SO4的饱和溶液,稀释时可以使溶液由b点变到a点
D. 仅通过降温的方法,可以使T2时的饱和溶液从c点变到T1时b点
科目:高中化学 来源: 题型:
【题目】一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知: pM=-lgc(M),pc(CO32-)=-lgc(CO32-)。下列说法正确的是
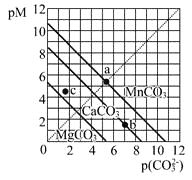
A. MgCO3、CaCO3、MnCO3的Ksp依次增大
B. a点可表示MnCO3的饱和溶液,且c(Mn2+)> c(CO32-)
C. b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-)
D. c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/( mol·L1) | 0.1 | 0.2 | 0 |
平衡浓度/( mol·L1) | 0.05 | 0.05 | 0.1 |
下列说法正确的是
A.反应达到平衡时,X和Y的转化率相等
B.增大压强使平衡向生成Z的方向移动,平衡常数增大
C.反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
D.若该反应的正反应方向为放热反应,升高温度,化学反应速率增大,反应的平衡常数也增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)是人体健康必需的一种微量元素。已知Se的原子结构示意图为: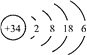 。下列说法不正确的是( )
。下列说法不正确的是( )
A. 该元素处于第四周期第ⅥA族 B. SeO2既有氧化性又有还原性
C. 该原子的质量数为34 D. 酸性:HBrO4 > H2SeO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法处理酸性含铬废水(主要含有Cr2O![]() )时,以铁板作阴、阳极,处理过程中存在反应Cr2O
)时,以铁板作阴、阳极,处理过程中存在反应Cr2O![]() +6Fe2++14H+===2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是( )
+6Fe2++14H+===2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是( )
A. 阳极反应为Fe-2e-===Fe2+
B. 电解过程中溶液pH不会变化
C. 处理过程中有Fe(OH)3沉淀生成
D. 每转移12 mol电子,有1 mol Cr2O![]() 被还原
被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)广泛应用于农药、医药和其它化工生产中。
(1)氧和硫元素位于同一主族,其原子结构的共同点是______;羰基硫中含有的化学键类型是______。
(2)CO和H2S混合加热生成羰基硫的反应是CO(g) + H2S(g) ![]() COS(g) + H2(g),
COS(g) + H2(g),
请回答下列问题。
①某温度下,在1L恒容密闭容器中,加入10mol CO和10mol H2S,平衡时测得CO转化率为40%,则该温度下反应的平衡常数K=______。
②由下图分析该反应是_______反应(填“吸热”或“放热”)。
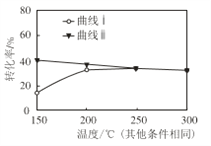

③请解释上图250℃以前, 曲线 ⅰ 变化的可能原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是元素周期表的一部分:
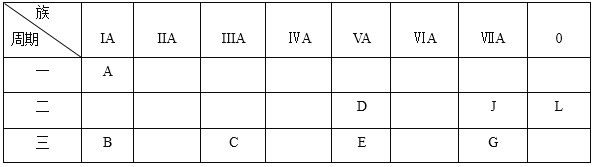
根据以上元素在周期表中的位置,用化学式填写空白。
(1)非金属性最强的元素是_________;化学性质最不活泼的是_________;除L外,原子半径最大的是_________;A与D形成的10电子离子是_________。
(2)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、D、E四种元素的最高价氧化物对应水化物的化学式排列成序是__________________;
(3)B元素可以形成两种氧化物,分别写出两种氧化物的电子式_________,_________。
(4)B、C、G、J四种元素的简单离子的半径由大到小的顺序为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是

A. 向苦卤中通入Cl2是为了提取溴
B. 粗盐可采用除杂和重结晶等过程提纯
C. 工业生产中常选用NaOH作为沉淀剂
D. 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com