
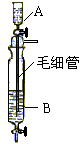
| A.A中装浓硫酸,B中装浓盐酸 |
| B.A中装浓盐酸,B中装浓硫酸 |
| C.A中装氢氧化钠浓溶液,B中装浓氨水 |
| D.A中装浓氨水,B中装氢氧化钠浓溶液 |
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源:不详 题型:单选题
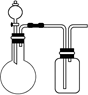
| A.实验室制取并收集少量NO2 |
| B.实验室制取并收集少量NH3 |
| C.验证非金属性:C>Si |
| D.验证氧化性:Cl2>I2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
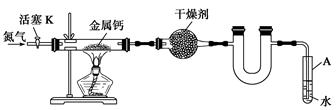
| 空硬质管质 量m0/g | 硬质管与钙的 质量m1/g | 硬质管与产物 的质量m2/g |
| 14.80 | 15.08 | 15.15 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
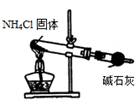
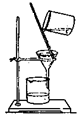


| A.用①装置制取干燥的氨气 | B.用②装置除去淀粉溶液中的NaCl |
| C.③装置可用于氨气的收集、检验 | D.④装置可用排空气法收集氢气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
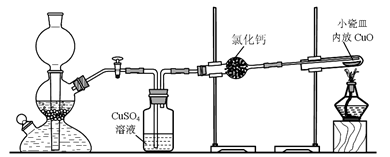

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
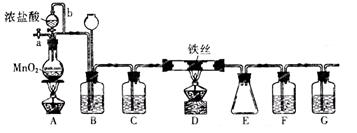
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com