
【题目】Na2CO3溶液呈性,原因是(用离子方程式表示) . KHSO4溶液呈性,原因是(用离子方程式表示) .
科目:高中化学 来源: 题型:
【题目】将1mol两种气态烃组成的混合气体完全燃烧后,将得到产物依次通入浓硫酸和石灰水中,其中浓硫酸质量增加了36g,并生成了150g沉淀.下列说法正确的是( )
A.一定有乙烷
B.一定有甲烷
C.一定没有甲烷
D.不一定有甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe2+和Fe3+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是( )
A. 2∶3 B. 3∶2
C. 1∶2 D. 1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素铬及其化合物工业用途广泛,但含+6价铬的污水会损害环境,必须进行处理。某工厂的处理工艺流程如下:
![]()
(1)N2H4的电子式为___________。
(2)下列溶液中,可以代替上述流程中N2H4的是___________。(填选项序号)
A.FeSO4溶液 B.浓HNO3溶液 C.酸性KMnO4溶液 D.Na2SO3溶液
(3)已知加入N2H4的流程中,N2H4转化为无污染的物质,则该反应中氧化剂与还原剂的物质的量之比为___________。
(4)在实际的含铬废水处理中,还可采用直接沉淀的方法,处理成本较低。
①已知含铬酸性废水中存在着Cr2O72-和CrO42-相互转化的平衡,请用离子方程式表示它们之间的转化反应___________;
②在实际工业生产中,加入沉淀剂BaCl2溶液之前还要加入一定量的NaOH,这样有利于沉淀的生成,则生成的沉淀为____________写化学式)。
(5)工业上可用电解法来处理含Cr2O![]() 的酸性废水。具体方法是首先通过电解制得还原剂,然后还原剂将Cr2O
的酸性废水。具体方法是首先通过电解制得还原剂,然后还原剂将Cr2O![]() 还原为Cr3+,最终转化成Cr(OH)3沉淀而除去。如图为电解装置示意图(电极材料分别为铁和石墨)。
还原为Cr3+,最终转化成Cr(OH)3沉淀而除去。如图为电解装置示意图(电极材料分别为铁和石墨)。

①装置中b电极的材料是________(填“铁”或“石墨”)。
②上述处理过程中,Cr2O![]() 被还原成Cr3+的离子方程式为_______________________。
被还原成Cr3+的离子方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。五种元素均位于短周期,X、W的质子数之和为23。下列说法正确的是
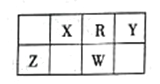
A. Y元素的最高价氧化物对应的水化物是含氧酸中酸性最强的
B. W和R只能形成一种化合物WR3,且为酸性氧化物
C. Z的气态氢化物稳定性强于W的气态氢化物
D. Z与R形成的化合物ZR2是生产光纤制品的基本原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.阅读下面短文。
原子核究竟是什么形状的呢?你也许会说,原子核应该是球形的吧。没错,对于大多数的原子而言,它们的原子核都是球形(如图1)或者比较接近球形的椭球形,就像橄榄球一样(如图2)。但是,科学家也发现极少数的原子核中的质子和中子会聚集成罕见的梨形(如图3)。

要想验证原子核是否为梨形,最直接的方法就是寻找不同核状态间的八极形变(octupole transition),这是梨形结构原子核特有的现象。利用这一手段,研究人员先后确认了224Ra、226Ra及其他一些重原子核均为梨形,但一直没有发现质量数小于200的梨形原子核。
近日,来自美国、英国和法国的一组科研团队制备了144Ba原子束,使其与铅箔发生碰撞并进入激发态。通过分析原子核产生的伽马射线光谱,研究人员发现几次八极形变的强度是核结构模型中预测数值的两倍多。由此,确认了144Ba的原子核也是梨形。
请回答下列问题:
(1)224Ra原子核的形状是_____________,224Ra和226Ra互称为____________。
(2)科学家确认144Ba的原子核是梨形,其根据是_____________(填字母)。
a.直接观察了144Ba原子核的形状 b.由核结构模型做出的理论计算 c.发现了八极形变现象
II.氧元素和硫元索组成的两种物质发生化学反应的微观示意图如图所示,其中●表示硫原子,O表示氧原子。

请回答下列问题:
(3)该反应的化学方程式是__________________________________。
(4)反应过程中,O2的浓度在5min内由5mol/L变成了1mol/L,用O2表示的化学反应速率是____________ mol·L-1·min-1。
(5)在等温等容条件下,该反应达到化学平衡状态的依据是___________(填字母)。
a.同一物质的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体中c(O2)不再改变 d.c(SO2)=c(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的CH3COOH和NaOH溶液混合后,溶液中c(CH3COO﹣)=c(Na+),则醋酸体积氢氧化钠溶液体积(填“>”或“=”或“<”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温下乙醛的沸点为20.8℃,且与水互溶.用HgSO4做催化剂,在75℃左右,乙炔可水化为乙醛,但HgSO4遇到某些特定物质常会发生催化剂中毒而失去催化作用,H2S就是其中一种:现用乙炔水化法,只用块状电石、浓硫酸、水、NaOH溶液、HgO粉末五种物质制取乙醛,装置如图所示,请回答下列问题; 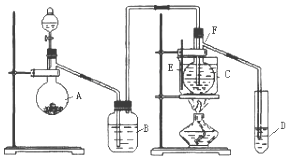
(1)实验开始时,仪器A中盛放电石,B中装NaOH溶液,其作用是 .
(2)仪器D中盛放水,其作用是吸收蒸气.
(3)蒸馏烧瓶F中应加入HgO和浓硫酸、水两种试剂,若将三者分别直接加入,请按加入的先后顺序写出包括HgO在内的各试剂的名称:氧化汞→→ .
(4)装置图中,加热F的方法叫 , 所选用温度计F的量程表示正确的是(填代号). A.0℃~50℃B.0℃~100℃C.0℃~200℃D. 0℃~360℃
(5)检验乙醛已制出的操作及现象是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com