
| 实验步骤 | 预期现象与结论 |
| 步骤1:取2mL FeSO4溶液和2mL KI溶液混合于试管中,再滴加1~2滴氯水. | 现象:溶液变成黄色. 结论: |
| 步骤2: | 现象: 结论: |
| 实验步骤 | 预期现象与结论 |
| 步骤1:取2mL FeSO4溶液和2mL KI溶液混合于试管中,再滴加1~2滴氯水. | 现象:溶液变成黄色. 结论:可能是生成了Fe3+、也可能是生成了I2 |
| 步骤2:向试管中继续滴加几滴2%KSCN溶液 | 现象:溶液不变血红色; 结论:证明I-的还原性强于Fe2+ |


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
| A、c(HCO3-)<c(CO32-) |
| B、c(HCO3-)>c(HSO3-) |
| C、c(CO32-)+c(HCO3-)═c(SO32-)+c(HSO3-) |
| D、两溶液都能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 一定条件下,溶液的酸碱性对TiO2光催化燃料R降解反应的影响如图所示.请回答下列问题:
一定条件下,溶液的酸碱性对TiO2光催化燃料R降解反应的影响如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
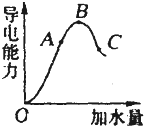 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如图所示.请回答:
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如图所示.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| 事实 | 结论 |
| A.完全燃烧产物是CO2和H2O的物质 | 一定只含C、H元素 |
| B.灼烧棉织品、羊毛衫和涤纶衣物 | 有烧焦羽毛气味的是羊毛衫 |
| C.在淀粉溶液中加入市售的加碘食盐不出现蓝色 | 不能说明此盐不含碘 |
| D.甲乙两种物质,相对分子质量相同,结构不同 | 甲和乙一定是同分异构体 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com