
【题目】根据下面的反应路线及所给信息填空。
(1)A的名称是________.
(2)③的反应类型是________,④的反应类型是________.
(3)反应②的化学方程式是________
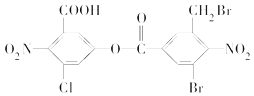
(4)某有机物的结构简式如图所示.1mol该有机物与足量的NaOH溶液共热,充分反应后质的量为________ mol.
【答案】环己烷 加成反应 消去反应 ![]() +NaOH
+NaOH![]()
![]() +NaCl+H2O 8.
+NaCl+H2O 8.
【解析】
由反应路线可知,A为![]() ,反应①为取代反应,反应②为
,反应①为取代反应,反应②为![]() + NaOH
+ NaOH![]()
![]() +NaCl+H2O,属于消去反应,反应③为C=C的加成反应,B为
+NaCl+H2O,属于消去反应,反应③为C=C的加成反应,B为 ,④为消去反应,反应④的化学方程式是
,④为消去反应,反应④的化学方程式是 +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O,以此解答(1)~(3);
+2NaBr+2H2O,以此解答(1)~(3);
(4)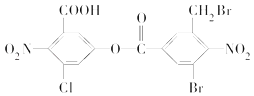 中,-Cl、-COOH、2个Br、-1个-COOC-及水解生成的3个酚-OH均与NaOH以1:1反应
中,-Cl、-COOH、2个Br、-1个-COOC-及水解生成的3个酚-OH均与NaOH以1:1反应
(1)由上述分析可知A为![]() ,名称为环己烷,故答案为:环己烷;
,名称为环己烷,故答案为:环己烷;
(2)反应③为C=C的加成反应,B为 ,④为消去反应,生成二烯烃,
,④为消去反应,生成二烯烃,
故答案为:加成反应;消去反应;
(3)反应②的化学方程式为![]() +NaOH
+NaOH![]()
![]() +NaCl+H2O
+NaCl+H2O
故答案为:![]() +NaOH
+NaOH ![]()
![]() +NaCl+H2O
+NaCl+H2O
(4)  中,Cl、COOH、2个Br、1个COOC及水解生成的3个酚OH均与NaOH反应,则1mol该有机物与足量的NaOH溶液共热,充分反应后最多可消耗NaOH的物质的量为8mol,
中,Cl、COOH、2个Br、1个COOC及水解生成的3个酚OH均与NaOH反应,则1mol该有机物与足量的NaOH溶液共热,充分反应后最多可消耗NaOH的物质的量为8mol,
故答案为:8.


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)若电解食盐水时消耗NaCl的质量为234 g,则在理论上最多可得氯气的体积为________升(标准状况)。
(2)若将2 mol的氯气通入足量石灰乳中,理论上可得到次氯酸钙________克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲氧基甲烷[CH2(OCH3)2]水溶性好、含氧量高、燃烧完全、烟气排放量低,被认为是一种极具应用前景的柴油添加剂。工业生产CH2(OCH3)2一般是在催化剂作用下,将37%的甲醛(HCHO)水溶液和甲醇(CH3OH)混合共热,反应原理如下:HCHO+2CH3OH![]() CH2(OCH3)2+H2O
CH2(OCH3)2+H2O
(1)某次研究反应时间对产率的影响的实验中,CH2(OCH3)2的浓度随反应时间变化如表:
时间(min) | 20 | 25 | 30 | 40 | 50 | 60 |
CH2(OCH3)2 (mol/L) | 9.02 | 9.10 | 9.18 | 9.23 | 9.30 | 9.32 |
计算25~50min中CH2(OCH3)2的平均生成速率为___。
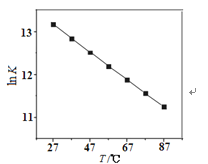
(2)研究反应的化学平衡常数(记作lnK)与温度(T)的关系如图所示,判断该反应的△H___0(填“>”、“<”、“=”)。
(3)假设在密闭容器中发生上述反应:
①达到平衡时下列措施能提高HCHO转化率的是___。
A.及时从反应体系中分离出CH2(OCH3)2
B.升高反应体系的温度
C.再添加适量甲醇
D.再添加一定量甲醛
②下图是催化剂作用下甲醇转化率随时间变化的趋势曲线图。请在图中用虚线画出相同条件下,不使用催化剂时转化率随时间变化的曲线。___
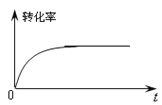
(4)进一步研究发现:甲醛的滴加速率、反应时间、催化剂的量和搅拌速率等对CH2(OCH3)2的工业实际产率(不完全是平衡状态下得出的)也会产生一定影响。欲分别研究甲醛的滴加速率、搅拌速率对产率的影响,某同学设计了三组实验如表:
影响因素 实验号 | 甲醛的滴加速率(g/min) | 反应时间(min) | 催化剂的量(g) | 搅拌速率(r/min) |
1 | ___ | 70 | 2.5 | 30 |
2 | 1.0 | ___ | ___ | ___ |
3 | 2.5 | ___ | ___ | 80 |
①请在上表空格中填入剩余的实验条件数据。
②在研究过程中发现,甲醛(HCHO)的滴加速率过慢或过快均会使CH2(OCH3)2产率降低。请结合该反应的合成机理:HCHO![]() HOCH2OCH3
HOCH2OCH3![]() CH2(OCH3)2,试分析甲醛的滴加速率过快时,导致产率较低的原因可能是___。
CH2(OCH3)2,试分析甲醛的滴加速率过快时,导致产率较低的原因可能是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BASF高压法制备醋酸,所采用钴碘催化循环过程如图所示,则下列观点错误的是( )
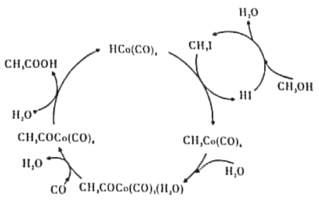
A.CH3OH转化为CH3I的有机反应类型属于取代反应
B.从总反应看,循环过程中需不断补充CH3OH、H2O、CO等
C.与乙酸乙酯互为同分异构体且与CH3COOH互为同系物的物质有2种结构
D.工业上以淀粉为原料也可以制备醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前我国研制的稀土催化剂催化转化汽车尾气示意图如图:
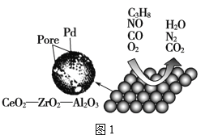
(1)Zr原子序数为40,价电子排布式为___。图1中属于非极性的气体分子是___。
(2)①氟化硼(BF3)是石油化工的重要催化剂。BF3中B-F比BF![]() 中B—F的键长短,原因是___。
中B—F的键长短,原因是___。
②乙硼烷(B2H6)是用作火箭和导弹的高能燃料,氨硼烷(H3NBH3)是最具潜力的储氢材料之一。
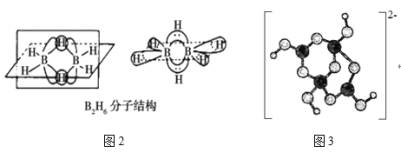
B2H6的分子结构如图2所示,其中B原子的杂化方式为___。
③H3NBH3的相对分子质量与B2H6相差不大,但是H3NBH3的沸点却比B2H6高得多,原因是__。
④硼酸盐是重要的防火材料。图3是硼酸钠晶体中阴离子(含B、O、H三种元素)的结构,该晶体中含有的化学键有__。
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键
(3)CO与Ni可生成羰基镍[Ni(CO)4],已知其中镍的化合价为0,[Ni(CO)4]的配体中配位原子是___。
(4)为了节省贵金属并降低成本,也常用钙钛矿型复合氧化物作为催化剂。一种复合氧化物结构如图4所示,则与每个Sr2+紧邻的O2-有___个。
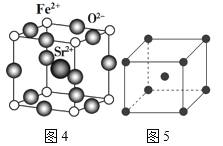
(5)与Zr相邻的41号元素Nb金属的晶格类型为体心立方晶格(如图5所示),原子半径为apm,相对原子质量为b,阿伏加德罗常数为NA,试计算晶体铌的密度为___g·cm-3(用来a、b、NA表示计算结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在做原电池原理的实验时,有如下实验步骤:
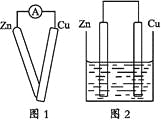
①用导线将灵敏电流计的两端分别与纯净的锌片和铜片相连接(如图1);
②把一块纯净的锌片插入盛有稀硫酸的烧杯中;
③把一块纯净的铜片插入盛有稀硫酸的烧杯中;
④用导线把锌片和铜片连接起来后,再平行地插入盛有稀硫酸的烧杯中(如图2)。
回答下列问题:
(1)实验步骤①中应观察到的现象是_______________________。
(2)实验步骤②中应观察到的现象是_______________________。
(3)实验步骤③中应观察到的现象是_______________________。
(4)实验步骤④中应观察到的现象是_______________________。
(5)通过实验步骤④该同学头脑中有了一个猜想(或假设),该猜想是_______。
(6)为了证实该猜想,该同学又设计了第⑤步实验,请简要画出第⑤步实验的装置示意图。______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明反应: A(s)+3B(g)![]() 2C(g)+D(g)已达平衡状态的是
2C(g)+D(g)已达平衡状态的是
A. 混合气体的压强B. 混合气体的密度
C. 3v逆(C)=2v正(B)D. 气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了9种元素在元素周期表中的位置示意。
周期 | ⅠA 1 | 0 18 | ||||||
1 | ⅡA 2 | ⅢA 13 | ⅣA 14 | ⅤA 15 | ⅥA 16 | ⅦA 17 | ||
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | |||||
4 | ⑨ | |||||||
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_____
(2)画出元素⑧形成的简单离子的结构示意图_________________
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_________
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是__________________
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是_______(填化学式),写出元素⑥的单质与水反应的离子反应方程式___________________,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是( )
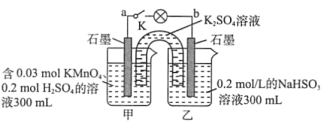
A.电池工作时,甲烧杯发生的反应为MnO4-被还原生成MnO2
B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a
C.乙中电极反应为HSO3--2e-+H2O=SO42-+3H+
D.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的H+浓度约为0.1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com