
| m |
| M |
| n |
| V |
| 49g |
| 98g/mol |
| 0.5mol |
| 0.5L |


科目:高中化学 来源: 题型:
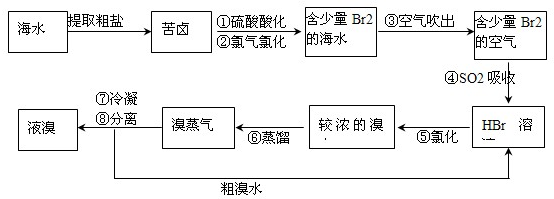
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | Fe2+具有还原性 | |
| ② | 在FeCl2溶液中加入锌片 | Zn+Fe2+→Zn2++Fe | Fe2+具有氧化性 | |
| ③ | 在FeCl3溶液中加入足量铁粉 | 溶液由棕黄色变为浅绿色 | Fe+2Fe3+→3Fe2+ | Fe3+具有氧化性 |
| ④ | 在FeCl3溶液中加入铜片 | Fe3+具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、少量的浓硫酸沾到皮肤上时,直接用大量的水冲洗,再涂上小苏打 |
| B、取用化学药品时,应特别注意观察药品包装容器上的安全警示标志 |
| C、凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
| D、闻任何化学药品的气味都不能使鼻子凑近药品 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com