
【题目】草酸是一种二元弱酸,可用作还原剂、沉淀剂等。某校课外小组的同学设计利用C2H2气体制取H2C2O4·2H2O。回答下列问题:
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。
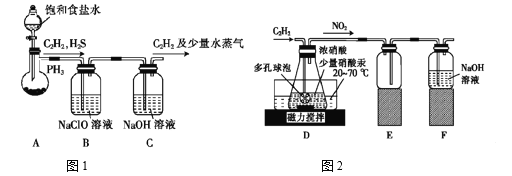
①电石与水反应很快,为了减缓反应速率,装置A中除用饱和食盐水代替水之外,还可以采取的措施是__________(写一种即可)。
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为______。该过程中,可能产生新的杂质气体Cl2,其原因是: _____________(用离子方程式回答)。
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是______________________。
②装置D中生成H2C2O4的化学方程式为____________________________。
③从装置D中得到产品,还需经过_____________(填操作名称)、过滤、洗涤及干燥。
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是______________________。
②滴定过程中发现褪色速率开始很慢后逐渐加快,分析可能的原因是_______________。
③产品中H2C2O4·2H2O的质量分数为_______________(列出含 m、c、V 的表达式)。
【答案】将烧瓶底部置于冰水浴中、控制分液漏斗活塞减缓滴加速度、将电石变为更大的块状 PH3+4ClO-=H3PO4+4Cl- Cl-+ ClO-+2H+ =Cl2↑+H2O 增大气体和溶液的接触面积,加快反应速率,使反应充分进行 C2H2+8HNO3(浓) ![]() H2C2O4+8NO2+4H2O 蒸发浓缩、冷却结晶 当加入最后一滴标准液后,溶液由无色变为浅红色,且半分钟内不恢复原来的颜色 生成的 Mn2+是该反应的催化剂
H2C2O4+8NO2+4H2O 蒸发浓缩、冷却结晶 当加入最后一滴标准液后,溶液由无色变为浅红色,且半分钟内不恢复原来的颜色 生成的 Mn2+是该反应的催化剂 ![]()
【解析】
(1)①碳化钙和水反应十分剧烈,可用饱和食盐水或利用分液漏斗控制滴加液体速度来控制反应速率;
②装置B用NaClO将H2S氧化为磷酸,将PH3氧化为H3PO4,硫、磷元素化合价升高,则氯元素化合价降低,生成氯离子;酸性条件下,ClO-也能氧化Cl-,生成氯气;
(2)D中,Hg(NO3)2作催化剂,浓硝酸氧化乙炔制取H2C2O42H2O,反应为:C2H2+8HNO3![]() H2C2O4+8NO2+4H2O,多孔球泡增大乙炔气体与硝酸的接触面,充分反应,E装置防止倒吸,F装置吸收生成的二氧化氮气体,将反应后的D浓缩结晶、过滤、洗涤、干燥得产品,据此分析解答;
H2C2O4+8NO2+4H2O,多孔球泡增大乙炔气体与硝酸的接触面,充分反应,E装置防止倒吸,F装置吸收生成的二氧化氮气体,将反应后的D浓缩结晶、过滤、洗涤、干燥得产品,据此分析解答;
(3)①滴定终点时,继续滴加高锰酸钾溶液,紫色不褪去;
②H2C2O4与KMnO4反应生成锰离子和二氧化碳,反应放热,生成的锰离子作催化剂;
③根据2MnO4-~5H2C2O4,由高锰酸钾的消耗可得H2C2O4的量,据此计算H2C2O42H2O的质量分数。
(1)①碳化钙和水反应十分剧烈,用饱和食盐水代替水来控制反应速率,也可以利用分液漏斗控制滴加液体速度,来控制反应速率;
②NaClO将PH3氧化为磷酸,根据电子守恒、电荷守恒、原子守恒,可得反应的离子反应为:PH3+4ClO-=H3PO4+4Cl-;在酸性条件下, ClO-也可以将Cl-氧化为Cl2,反应的离子方程式为:Cl-+ClO-+2H+=Cl2↑+H2O
(2)①装置D多孔球泡的作用是增大乙炔气体与硝酸的接触面,充分反应;
②根据装置图,D中,Hg(NO3)2作催化剂,浓硝酸氧化乙炔反应生成H2C2O4和二氧化氮,反应为:C2H2+8HNO3![]() H2C2O4+8NO2+4H2O;
H2C2O4+8NO2+4H2O;
③将反应后的D溶液加热浓缩、冷却结晶、过滤、洗涤、干燥得产品;
(3)①滴定过程中,当溶液呈浅红色且30 s内不褪色时达到滴定终点;
②H2C2O4与KMnO4反应生成Mn2+和CO2,反应可能放热,溶液温度升高,另外生成的Mn2+是该反应的催化剂,故滴定过程中发现褪色速率先慢后逐渐加快;
③根据氧化还原反应过程中电子转移数目相等,可得关系式
2MnO4-~5H2C2O4,则n(H2C2O42H2O)=n(H2C2O4)=![]() n(MnO4-)=
n(MnO4-)=![]() ×cV×10-3mol,产品中H2C2O42H2O的质量分数为
×cV×10-3mol,产品中H2C2O42H2O的质量分数为![]() =
=![]() 。
。


科目:高中化学 来源: 题型:
【题目】25℃时,在20 mL 0.1 mol·L-1一元弱酸HA溶液中滴加0. 1 mol· L-1 NaOH溶液,溶液中1g[c(A-)/c(HA)]与pH关系如图所示。下列说法正确的是

A. A点对应溶液中:c(Na+)>c(A-)>c(H+)>c(OH-)
B. 25℃时,HA酸的电离常数为1. 0× 10-5.3
C. B点对应的NaOH溶液体积为10 mL
D. 对C点溶液加热(不考虑挥发),则c(A-)/[c(HA)c(OH-)]一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海带中提取碘的工业生产过程如下:
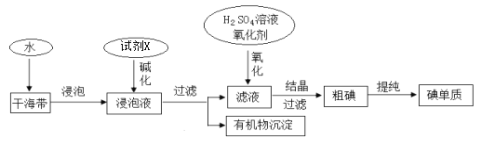
下列说法不正确的是
A.试剂X可以为NaOH溶液,其作用是使浸泡液中的可溶性有机物形成沉淀
B.氧化剂X可以用H2O2或适量的Cl2
C.干海带浸泡液中的碘离子可用淀粉溶液检验
D.氧化后的滤液在实验室也可采用四氯化碳萃取、分液、蒸馏的方法得到粗碘,蒸馏后得到的粗碘在蒸馏烧瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X元素是地壳中含量最多的元素,Y元素是空气中含量最多的元素,A元素与Y同主族,且是该主族中原子序数最大的非金属元素,D元素位于周期表中第三周期,其最高氧化态可与A形成D3A2。下列说法错误的是
A. 对应酸的酸性:A2X5<A2X3B. 简单离子半径:A>Y>X>D
C. A元素的原子结构示意图: D. 非金属性:X>Y
D. 非金属性:X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的结构简式如图,下列说法不正确的是

A. X分子式为C10H20O,它是环己醇的同系物
B. X的一氯取代物有6种
C. X能使酸性高锰酸钾溶液褪色
D. 在一定条件下,X能发生消去反应生成2种烯烃(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B均为钾盐的水溶液,A呈中性,B有氧化性,E的溶质中有一种含+5价元素的含氧酸盐M。现有下图所示转化:
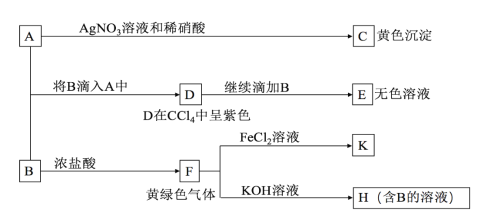
请回答:
(1)C的化学式为_________,检验气体F常用的试纸是______________
(2)写出物质M在生活中的常见用途______________
(3)写出F→H的化学方程式:______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
A.Fe+CuSO4=FeSO4+Cu
B.AgNO3+NaCl=AgCl↓+NaNO3
C.Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
D.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积恒定的密闭容器中发生反应N2O4(g)![]() 2NO2(g) ΔH>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g) ΔH>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是

A. A、C两点的反应速率:A>C
B. A、C两点气体的颜色:A深,C浅
C. 由状态B到状态A,可以用加热的方法
D. A、C两点气体的平均相对分子质量:A>C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com