
【题目】(题文)高聚物I和J在生产、生活中有广泛应用,其合成路线如图:

芳香烃R的分子式为C9H10,其苯环上只有一个取代基,R与H21:1加成后产物的核磁共振氢谱中有5组峰,峰面积之比为1:2:2:1:6。
已知:R'CH=CH2![]() R'CH2CH2Br
R'CH2CH2Br
回答下列问题:
(1)芳香烃R分子的官能团是_________(填官能团符号),R的最简单同系物是_____(填化学名称)。
(2)反应②的化学方程式为__________________。
(3)③和⑦的反应类型分别属于____________、______________________。
(4)高聚物J的结构简式为________________________。
(5)反应⑥的反应条件是______________________。
(6)H与T互为同分异构体,符合下列性质特征的H分子共有________种。
①能发生银镜反应②和氯化铁溶液反应显紫色③能使溴的四氧化碳溶液褪色
(7)仿照上述合成路线,设计一条以R为主要原料制备 的合成路线(无机试剂任选):____________________________________________________。
的合成路线(无机试剂任选):____________________________________________________。
【答案】 ![]() 苯乙烯
苯乙烯 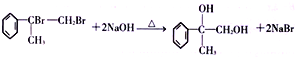 氧化区应 酯化反应或取代反应
氧化区应 酯化反应或取代反应 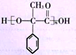 浓硫酸、加热 16
浓硫酸、加热 16 ![]()
【解析】试题分析:芳香烃R的分子式为C9H10,其苯环上只有一个取代基,R与H21:1加成后产物的核磁共振氢谱中有5组峰,峰面积之比为1:2:2:1:6,R的结构简式是![]() ;
;![]() 与溴的四氯化碳溶液发生加成反应生成X,X是
与溴的四氯化碳溶液发生加成反应生成X,X是![]() ,
,![]() 在氢氧化钠的水溶液中水解为Y,Y是
在氢氧化钠的水溶液中水解为Y,Y是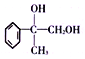 ,
, 催化氧化为Z,Z是
催化氧化为Z,Z是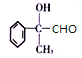 ;
; 被银氨溶液氧化为W,W是
被银氨溶液氧化为W,W是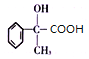 ;
; 发生缩聚反应生成J,则J是
发生缩聚反应生成J,则J是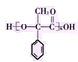 ;
; 在浓硫酸作用下发生消去反应生成T,T是
在浓硫酸作用下发生消去反应生成T,T是![]() ;
;![]() 与乙醇发生酯化反应生成M,M是
与乙醇发生酯化反应生成M,M是![]() ;
;![]() 一定条件下发生加聚反应生成I,I是
一定条件下发生加聚反应生成I,I是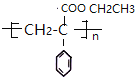 ;
;
解析:根据以上分析,(1)芳香烃R是![]() ,含的官能团是
,含的官能团是![]() ,R的最简单同系物含有1个苯环和1个碳碳双键,名称是苯乙烯。
,R的最简单同系物含有1个苯环和1个碳碳双键,名称是苯乙烯。
(2) ![]() 在氢氧化钠的水溶液中水解为
在氢氧化钠的水溶液中水解为 的化学方程式为
的化学方程式为 。
。
(3)  生成
生成 是氧化反应,
是氧化反应,![]() 与乙醇生成的
与乙醇生成的![]() 反应类型是酯化反应。
反应类型是酯化反应。
(4)  发生缩聚反应生成高聚物J,J的结构简式为
发生缩聚反应生成高聚物J,J的结构简式为 。
。
(5)  在浓硫酸作用下、加热,发生消去反应生成
在浓硫酸作用下、加热,发生消去反应生成![]() 。
。
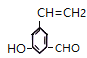
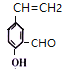
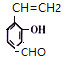
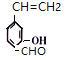
(6)①能发生银镜反应,说明含有醛基;②和氯化铁溶液反应显紫色,说明含有酚羟基;③能使溴的四氧化碳溶液褪色,说明含有碳碳双键,符合条件的![]() 的同分异构体有
的同分异构体有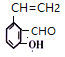 、
、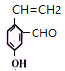 、
、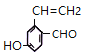 、
、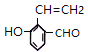 、
、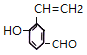 、
、 、
、 、
、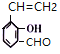 、
、 、
、 、
、![]() 、
、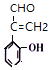 、
、![]() 、
、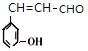 、
、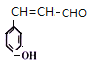 、
、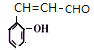 ,共16种。
,共16种。
(7) 根据R'CH=CH2![]() R'CH2CH2Br,
R'CH2CH2Br, ![]()
![]()
![]()
,![]() 在氢氧化钠的水溶液中水解为
在氢氧化钠的水溶液中水解为![]() ,
,![]() 催化氧化为
催化氧化为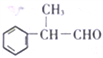 ,以
,以![]() 为主要原料制备
为主要原料制备 的合成路线是:
的合成路线是:![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知常温:Ksp(PbI2)=4×10-6,Ksp(PbS)=8×10-28。取适量黄色PbI2固体配制成100mL溶液,配制过程中溶液的离子浓度与时间的变化关系如图所示。下列说法中正确的是

A. A点处可表示PbI2的不饱和溶液
B. T时刻有可能向该PbI2溶液中加人了KI固体
C. 常温下PbI2饱和溶液中的c(I-)=10-2mol/L
D. 向A点处的PbI2溶液中加入100mL 2×10-3mol/L的Na2S溶液,平衡后溶液中的c(Pb2+)<4×10-3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是原子序数依次递增的前四周期元素,A元素的正化合价与负化合价的代数和为零;B元素原子的价电子结构为nsnnpn;C元素基态原子s能级的电子总数比p能级的电子总数多1;D元素原子的M能层全满,最外层只有一个电子。请回答:
(1)A元素的单质为A2,不能形成A3或A4,这体现了共价键的___性;B元素单质的一种空间网状结构的晶体熔点>3550℃,该单质的晶体类型属于________;基态D原子共有___种不同运动状态的电子。
(2)A与C形成的最简单分子的中心原子杂化方式是___________,该分子与D2+、H2O以2:1:2的配比结合形成的配离子是_________(填化学式),此配离子中的两种配体的不同之处为_____(填标号)。
①中心原子的价层电子对数 ②中心原子的孤电子对的对数 ③中心原子的化学键类型 ④VSEPR模型
(3)1molBC—中含有的π键数目为______;写出与BC-互为等电子体的分子和离子各一种______、______。
(4)D2+的硫酸盐晶体的熔点比D2+的硝酸盐晶体的熔点高,其原因是______。
(5)D3C具有良好的电学和光学性能,其晶体的晶胞结构如图所示,D+和C3—半径分别为apm、bpm,D+和C3—都是紧密接触的刚性小球,则C3—的配位数为_____,晶体的密度为____g·cm-3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于吸热反应的是( )
A. C6H12O6(葡萄糖aq)+6O2![]() 6CO2+6H2O
6CO2+6H2O
B. 氢氧化钠溶液与盐酸的中和反应
C. 反应物的总能量大于生成物的总能量
D. 破坏反应物全部化学键所需能量大于破坏生成物全部化学键所需能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芒硝化学式为Na2SO410H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物.该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念. 
(1)该电解槽的阳极反应式为 . 此时通过阴离子交换膜的离子数(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数.
(2)制得的氢氧化钠溶液从出口(填“A”、“B”、“C”或“D”)导出.
(3)通电开始后,阴极附近溶液pH会增大,请简述原因: .
(4)若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为 . 已知H2的燃烧热为285.8kJmol﹣1 , 则该燃料电池工作产生36g H2O时,理论上有 kJ的能量转化为电能.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量的说法正确的是
A. 原电池将化学能转变为电能
B. 原电池将电能转变为化学能
C. 中和反应放热说明中和反应前后能量不守恒
D. 吸热反应中生成物的总能量低于反应物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示为石蜡油分解的实验装置。在试管①中加入石蜡油和氧化铝;试管②放在冷水中;试管③中加入酸性高锰酸钾溶液;试管④中加入溴水。分析实验完成下列各题:

分析实验回答下列问题:
(1)试管①中加入氧化铝的作用是____________________________________________。
(2)试管②内看到的实验现象是______________________________________________。
(3)试管③中看到的实验现象为_______________________________________________,发生________反应(填反应类型)。
(4)试管④中看到的实验现象为_______________________________________________,发生________反应(填反应类型)。
(5)通过本实验说明______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,可逆反应A(g)+3B(g)![]() 2C(g)达到平衡的标志是( )
2C(g)达到平衡的标志是( )
A. C生成的速率是A反应速率的2倍
B. A、B、C的浓度不再变化
C. 单位时间内生成nmol A,同时生成3nmol B
D. A、B、C的分子数之比为1∶3∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com