
【题目】关于明矾的下列说法错误的是( )
A.明矾的化学式为KAl(SO4)2
B.明矾是纯净物
C.明矾可用于净水
D.明矾中存在K+和Al3+两种阳离子
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】纯铁的熔点为1 535 ℃,在高炉中炼铁时,生铁(含碳量较高的合金)在1 200 ℃左右就熔化了,这是因为( )
A.铁的纯度越高熔点越低
B.合金的熔点比其成分物质的熔点高
C.合金的熔点比其成分物质的熔点低
D.在高炉中熔化的过程中发生了化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“4.14玉树地震”后,消毒尤为重要,其中常用的消毒剂为“84”消毒液,市场上销售的“84”消毒液,其商品标识上有如下叙述: ①本品为无色溶液,呈碱性 ②使用时加水稀释 ③可对餐具、衣物进行消毒,可漂白浅色衣服 则其有效成份可能是
A.Cl2 B.SO2 C.NaClO D.KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料.某AlN样品仅含有Al2O3杂质,为侧定AlN的含量.设计如下三种实验方案。
己知:AlN+NaOH+H2O═NaAlO2+NH3↑
【方案1】取一定量母的样品,用图1装置测量样品中AlN的纯度(夹持装置已略去)。

(1)如图C装置中球形干燥管的作用是__________________。
(2)完成以下实验步骤:组装好实验装置,首先__________,再加入实验药品.接下来的实验操作是__________,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体.打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是__________。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见__________。
【方案2】用如图2装置测定mg样品中A1N的纯度(部分夹持装置已略去)。
(4)导管a的主要作用是__________。
(5)为测定生成气体的体积,量气装置中的X液体可以是__________(填选项序号)。
a.CCl4 b.H2O c.NH4Cl溶液 d.![]()
(6)若mg样品完全反应,测得生成气体的体积为VmL(已转换为标准状况),则AlN的质量分数是__________(用含m、V的数学表达式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对四种无色溶液进行离子检验,实验结果如下,其中明显错误的是
A. K+、Na+、Cl-、NO3- B. Na+、NO3-、OH-、CO32-
C. Na+、OH-、Cl-、NO3- D. MnO4-、K+、S2-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
①质子数相同的粒子一定属于同种元素;
②同位素的性质几乎完全相同;
③质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子;
④电子数相同的粒子不一定是同一种元素;
⑤一种元素只能有一种质量数;
⑥某种元素的相对原子质量取整数,就是其质量数
⑦元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑧核外电子排布相同的微粒化学性质不一定相同
⑨![]() 与
与![]() 得电子能力相同
得电子能力相同
A. ①②④⑤ B. ③④⑤⑥ C. ②③⑤⑥ D. ①②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修物质结构与性质】主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
(1)在基态14C原子中,核外存在 对自旋相反的电子,基态氮原子的价层电子排布图为_________________________。
(2)将F2通入稀NaOH溶液中可生成OF2,OF2分子构型为 ,其中氧原子的杂化方式为 。
(3)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n= 。CO与N2结构相似,CO分子内σ键与π键个数之比为 。
(4)CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜,该反应的化学方程式是 。
(5)H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释H2SeO4比H2SeO3酸性强的原因: ;
(6)已知Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
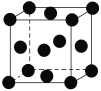
(7)用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如右图),已知该晶体的密度为9.00 g·cm-3,Cu的原子半径为________cm(阿伏加德罗常数为NA,只要求列式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com