
| A、用酸性高锰酸钾溶液鉴别乙烯和甲苯 |
| B、用醋、石灰水验证蛋壳中含有碳酸盐 |
| C、用碘酒检验汽油中是否含有不饱和烃 |
| D、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、多肽、油脂、纤维素、淀粉、蔗糖和葡萄糖在一定条件都能发生水解反应 |
| B、棉、麻、蚕丝、羊毛及合成纤维完全燃烧都只生成CO2和H2O |
| C、蛋白质是结构复杂的高分子化合物,蛋白质分子中都含有C、H、O、N四种元素 |
| D、根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、用惰性电极电解MgCl2溶液时只发生:2Cl-+2H2O
| ||||
| B、在含有nmolFeBr2溶液中通入nmolCl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+2Cl- | ||||
| C、在Ca(HCO3)2溶液中加入含等物质的量的NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O | ||||
| D、金属铝溶于NaOH溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④ | B、②④ | C、①④ | D、①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、减小、增大、减小 |
| B、增大、减小、减小 |
| C、减小、增大、增大 |
| D、增大、减小、增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
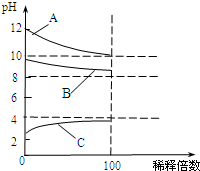 现有常温时浓度相同的五种电解质溶液:
现有常温时浓度相同的五种电解质溶液:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量①与②分别与少量的锌(大小相同)反应时,开始时刻速率相同,反应中速率:①<② |
| B、将②、③两种溶液混合后,若呈中性,则消耗溶液的体积:②>③ |
| C、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| D、将③稀释a倍,将④稀释b倍,两溶液pH相等,则a<b倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若混合气体中各成分的浓度不再变化,则该反应已达平衡状态 |
| B、将1 mol N2和3 mol H2充入容器反应达到平衡时,放出的热量等于93.4 kJ |
| C、催化剂能缩短该反应达到平衡所需的时间,从而提高N2的转化率 |
| D、缩小容器的体积,v(正)增大、v(逆)减小,平衡向右移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com