
【题目】下列过程或现象与盐类水解无关的是( )
A. 纯碱溶液去油污 B. 铁在潮湿的环境下生锈
C. 加热氯化铁溶液颜色变深 D. 浓硫化钠溶液有臭味
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,其中W的原子核中只有6个质子;X可与W形成两种常见的气体WX和WX2;Y是短周期元素中原子半径最大的元素;Z与Y形成的化合物的水溶液呈中性。下列叙述正确的是( )
A. Y位于第3周期ⅦA族 B. 单质沸点:W>Y
C. 气体氢化物稳定性:W>Z D. 离子半径:X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有X(g)+Y(g)2Z(g),正反应放热,从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据如图回答:从t2→t3的曲线变化是由哪种条件引起的( )
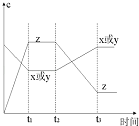
A.增大X或Y的浓度 B.增大压强
C.增大Z的浓度 D.升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】飘尘是物质燃烧时产生的粒状漂浮物,颗粒很小,不易沉降,它与空气中的SO2和O2接触时,SO2会部分转化为SO3,使空气的酸度增加,飘尘所起的作用可能是( )
A.氧化剂 B.还原剂 C.催化剂 D.载体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200℃时,11.6gCO2和水蒸气的混合气体与过量的Na2O2充分反应后,固体质量增加了3.6g,再将反应后剩余固体冷却后加入含有Na+、HCO3-、SO42-、CO32-等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是( )
A.原混合气体的平均摩尔质量为23.2g/mol
B.混合气体与Na2O2反应过程中电子转移的物质的量为0.25mol
C.溶液中SO42-的物质的量浓度基本保持不变
D.溶液中HCO3-的物质的量浓度减小,CO32-的物质的量浓度增大,但是HCO3-和CO32-的物质的量浓度之和基本保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸钙广泛用于食品、化工、石油等工业生产上,300~400℃左右分解.
Ⅰ、实验室制取的方法之一是:Ca(OH)2+2HCHO+H2O2=Ca(HCOO)2+2H2O+H2↑.
实验室制取时,将工业用氢氧化钙和甲醛依次加入到质量分数为30-70%的过氧化氢溶液中(投料物质的量之比依次为1:2:1.2),最终可得到质量分数98%以上且重金属含量极低的优质产品.
(1)过氧化氢比理论用量稍多,其目的是____________。
(2)反应温度最好控制在30-70℃之间,温度不宜过高,其主要原因是____________。
(3)制备时在混合溶液中要加入微量硼酸钠抑制甲醛发生副反应外,还要加入少量的Na2S溶液,加硫化钠的目的是____________。
(4)实验时需强力搅拌45min,其目的是____________;结束后需调节溶液的pH 7~8,其目的是____________,最后经结晶分离、干燥得产品.
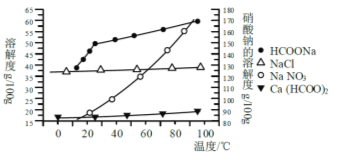
Ⅱ、某研究性学习小组用工业碳酸钙(主要成分为CaCO3;杂质为:Al2O3、FeCO3) 为原料,先制备无机钙盐,再与甲酸钠溶液混合制取甲酸钙.结合下图几种物质的溶解度曲线及表中相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0molL-1计算)。
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
请补充完整由碳酸钙制备甲酸钙的实验方案:
步骤一:称取13.6g甲酸钠溶于约20mL水,配成溶液待用,并称取研细的碳酸钙样品10g待用;
步骤二:____________;
步骤三:____________;
步骤四:过滤后,将滤液与甲酸钠溶液混合,调节溶液pH7-8,充分搅拌,所得溶液经过 、 、洗涤、60℃干燥得甲酸钙晶体。
提供的试剂有:a.甲酸钠,b.5molL-1硝酸,c.5molL-1盐酸,d.5molL-1硫酸,e.3%H2O2溶液,f.澄清石灰水。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国晋代《抱朴子》中描述了大量的化学反应,其中有:①“丹砂(HgS)烧之成水银,积变又还成丹砂”; ②“以曾青涂铁,铁赤色如铜”。下列有关叙述正确的是
A.①中水银“积变又还成丹砂”说明水银发生了还原反应
B.②中反应的离子方程式为:2Fe+3Cu2+=2Fe3++3Cu
C.根据①可知温度计打破后可以用硫粉覆盖水银,防止中毒
D.水银能跟曾青发生置换反应生成单质铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可利用下图所示电解装置吸收和转化SO2(A、B均为惰性电极)。下列说法正确的是
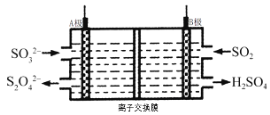
A.A电极接电源的正极
B.A极区溶液的碱性逐渐增强
C.本装置中使用的是阴离子交换膜
D.B极的电极反应式为SO2+2e-+2H2O = SO42-+4H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com