
| A�������½�pH=3�Ĵ�����Һϡ�͵�ԭ�����10������Һ��pH=4 |
| B��δȷ��ij��H2A��ǿ�ỹ�����ᣬ�ɲ�NaHA��Һ��pH����pH��7����H2A�����pH��7��H2A��ǿ�� |
| C����֪����HF��CH3COOH�����ʵ���Ũ����ȵ�NaF��CH3COOK��Һ�У�[c��Na+��-c��F-��]��[c��K+��-c��CH3COO-��] |
| D����ͬ�¶��£��������Ȼ�������ֱ������ͬ����Ģ�����ˮ ��0.1mol/L���� ��0.1mol/L�Ȼ�þ��Һ ��0.1mol/L��������Һ�У�Ag+Ũ�ȣ��٣���=�ڣ��� |
| 1 |
| 10 |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A���ų�������ϵ��a��b��196 |
| B�����������ڷ�Ӧ��ƽ�ⳣ�����ۣ��٣��� |
| C����ƽ��ʱSO3������������ۣ��� |
| D��SO2��ת���ʣ��ڣ��٣��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ʵĵ��뷽��ʽΪNaHCO3��Na++H++CO32- |
| B��25��ʱ����ˮϡ�ͺ�n��H+����n��OH-���ij˻���� |
| C������Ũ�ȹ�ϵ��c��Na+��+c��H+��=c��OH-��+c��HCO3-��+c��CO32-�� |
| D���¶����ߣ�c��HCO3-������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Һ�мӵμӼ���Ũ���ᣬc��NH4+������ |
| B������Һ�м�������CH3COONa���壬c��NH4+������ |
| C����Һ������Ũ�ȹ�ϵΪ��c��Cl-����c��NH4+����c��H+����c��OH-�� |
| D������Һ�м�������ˮʹ���Һ��pH=7�����Һ��c��NH4+����c��Cl-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��AgCl��ͬŨ�ȵ�CaCl2��NaCl��Һ�е��ܽ����ͬ | ||
| B��pH=4.5�ķ���֭��c��H+����pH=6.5��ţ����c��H+����100�� | ||
| C��ij��Һ����ˮ���������c��H+����c��OH-���ij˻�Ϊ1��10-24������Һ��һ�����Դ�������K+��Na+��[Al��OH��4]-��SO42- | ||
D��������0.1 mol?L-1HA��Һ��pH��1��0.1 mol?L-1BOH��Һ��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 50-80�� |
| 180-200�� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A���÷�Ӧ�Ļ�ѧ����ʽ��3X+2Y=2Z |
| B�������������ﵽƽ��ʱ�������������V��I����V��II����������II�ﵽƽ������ʱ��С��t0 |
| C�����������о��ﵽƽ��ʱ����������Z�����ʵ���������ͬ����YΪ��̬��Һ̬ |
| D������ƽ��������II�����¶�ʹ���������˵��Z�����ķ�ӦΪ���ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�� ���� | Ԫ��ԭ�ӽṹ |
X | ԭ�ӽṹʾ��ͼΪ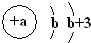 |
| Y | �����������Ǵ�����������2�� |
Z | ԭ�Ӻ��ں���12�����ӣ��������ӵĽṹʾ��ͼΪ  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com