
ЎҫМвДҝЎҝ·ҙУҰ4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)Ј¬H=-akJmol-1Ј¬ФЪ5LГЬұХИЭЖчН¶Ил1molNH3әН1molөДO2Ј¬2·ЦЦУәуNOөДОпЦКөДБҝФцјУБЛ0.4molЈ¬ПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
4NO(g)+6H2O(g)Ј¬H=-akJmol-1Ј¬ФЪ5LГЬұХИЭЖчН¶Ил1molNH3әН1molөДO2Ј¬2·ЦЦУәуNOөДОпЦКөДБҝФцјУБЛ0.4molЈ¬ПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
A.2·ЦЦУ·ҙУҰ·ЕіцөДИИБҝЦөРЎУЪ0.1akJ
B.УГСхЖшұнКҫ0Ў«2minөД·ҙУҰЛЩВКЈәv(O2)=0.05molЎӨL-1ЎӨmin-1
C.2·ЦЦУДЪNH3өДЧӘ»ҜВККЗ50%
D.2·ЦЦУД©c(H2O)=0.6mol/L
Ўҫҙр°ёЎҝB
ЎҫҪвОцЎҝ
ФЪ5LГЬұХИЭЖчН¶Ил1molNH3әН1molO2Ј¬2·ЦЦУәуNOөДОпЦКөДБҝФцјУБЛ0.4molЈ¬ФтЈә
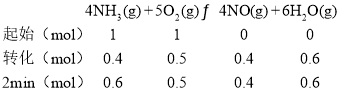
AЈ®УЙИИ»ҜС§·ҪіМКҪҝЙЦӘЙъіЙ4molNOЈ¬Фт·ЕіцakJИИБҝЈ¬ФтЙъіЙ0.4molNOЈ¬ФтИИБҝЦөОӘ0.1akJЈ¬№КAҙнОуЈ»
BЈ®УГСхЖшұнКҫ2·ЦЦУөД·ҙУҰЛЩВКЈәv(O2)= =0.05molLmin-1Ј¬№КBХэИ·Ј»
=0.05molLmin-1Ј¬№КBХэИ·Ј»
CЈ®2·ЦЦУДЪNH3өДЧӘ»ҜВККЗ![]() ЎБ100%=40%Ј¬№КCҙнОуЈ»
ЎБ100%=40%Ј¬№КCҙнОуЈ»
DЈ®2·ЦЦУД©c(H2O)=![]() =0.12mol/LЈ¬№КDҙнОуЈ»
=0.12mol/LЈ¬№КDҙнОуЈ»
№Кҙр°ёОӘBЎЈ


 МмМмПтЙПТ»ұҫәГҫнПөБРҙр°ё
МмМмПтЙПТ»ұҫәГҫнПөБРҙр°ё РЎС§Йъ10·ЦЦУУҰУГМвПөБРҙр°ё
РЎС§Йъ10·ЦЦУУҰУГМвПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝФЪДіОВ¶ИКұЈ¬Ҫ«n mol/LөД°ұЛ®өОИл10 mL1.0 mol/LСОЛбЦРЈ¬ИЬТәpHәНОВ¶ИЛжјУИл°ұЛ®Ме»эұд»ҜЗъПЯИзНјЛщКҫЈ¬ПВБРУР№ШЛө·ЁХэИ·өДКЗ

A. aөгKW=1.0ЎБ10Јӯ14
B. Л®өДөзАліМ¶ИЈәb©ғa©ғc©ғd
C. bөгЈәc(NH4+)©ғc(Cl-)©ғc(H+)©ғc(OH-)
D. 25ЎжКұNH4ClЛ®ҪвЖҪәвіЈКэОӘ(nЈӯ1)ЎБ10-7ЈЁУГnұнКҫЈ©
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝФЪ2 LГЬұХИЭЖчЦРЈ¬800 ЎжКұЈ¬·ҙУҰ2NOЈ«O2![]() 2NO2МеПөЦРЈ¬n(NO)ЛжКұјдөДұд»ҜИзПВұнЈә
2NO2МеПөЦРЈ¬n(NO)ЛжКұјдөДұд»ҜИзПВұнЈә
Кұјд(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)ИзНјұнКҫёчОпЦКЕЁ¶ИөДұд»ҜЗъПЯЈ¬
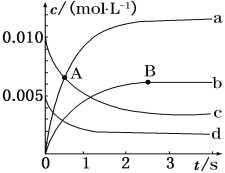
AөгҙҰЈ¬v(Хэ)___________v(Дж)Ј¬ AөгХэ·ҙУҰЛЩВК_________BөгХэ·ҙУҰЛЩВКЎЈ (УГЎ°ҙуУЪЎұЎўЎ°РЎУЪЎұ»тЎ°өИУЪЎұМоҝХ)
(2)НјЦРұнКҫO2ұд»ҜөДЗъПЯКЗ___________ЎЈУГNO2ұнКҫҙУ0Ў«2 sДЪёГ·ҙУҰөДЖҪҫщЛЩВКvЈҪ____________________________ЎЈ
(3) ДЬК№ёГ·ҙУҰөД·ҙУҰЛЩВКФцҙуөДКЗ____________ЎЈ
AЈ®ј°Кұ·ЦАліцNO2ЖшМе BЈ®ЙэёЯОВ¶И
CЈ®јхРЎO2өДЕЁ¶И DЈ®СЎФсёЯР§өДҙЯ»ҜјБ
(4) ДЬЛөГчёГ·ҙУҰТСҫӯҙпөҪЖҪәвЧҙМ¬өДКЗ___________ЎЈ
AЈ®ИЭЖчДЪС№ЗҝұЈіЦІ»ұдЎЎЎЎ BЈ®v(NO)ЈҪ2v(O2)
CЈ®ИЭЖчДЪөДГЬ¶ИұЈіЦІ»ұд DЈ®vДж(NO2)ЈҪ2vХэ(O2)
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝИзНјЛщКҫAҙҰНЁИліұКӘөДCl2Ј¬№ШұХ»оИыBКұDЦРёЙФпөДәмЙ«ІјМхСХЙ«ОЮұд»ҜЈ»ҙтҝӘ»оИыBКұDҙҰёЙФпөДәмЙ«ІјМхНКЙ«Ј¬ФтCЦРөДКФјБЈЁЧгБҝЈ©І»ҝЙДЬКЗ
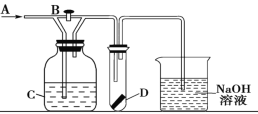
A.ұҘәНВИ»ҜДЖИЬТәB.ЗвСх»ҜёЖРьЧЗТәC.ұҘәНМјЛбДЖИЬТәD.ЕЁБтЛб
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР·ҪіМКҪКйРҙХэИ·өДКЗ(ЎЎЎЎ)
A. NaHSO4ФЪЛ®ИЬТәЦРөДөзАл·ҪіМКҪЈәNaHSO4===NaЈ«Ј«HSO4-
B. HFУлNaOHИЬТә·ҙУҰЈәHЈ«(aq)Ј«OHЈӯ(aq) = H2O(l)ЎЎҰӨHЈҪЈӯ57.3 kJ/mol
C. 1g H2ИјЙХЙъіЙТәМ¬Л®·Еіц142Ј®9 kJөДИИБҝЈ¬ЖдИИ»ҜС§·ҪіМКҪЈә2H2(g)+ O 2(g) = 2H2O (l) ҰӨH = ЎӘ142Ј®9ЎЎkJЎӨmol-1
D. CaCO3іБөнИЬҪвЖҪәв·ҪіМКҪЈәCaCO3(s) ![]() Ca2Ј«(aq)Ј«CO32-(aq)
Ca2Ј«(aq)Ј«CO32-(aq)
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝФЪБтЛбНӯҫ§МеҪбҫ§Л®ә¬БҝІв¶ЁөДКөСйЦРЈ¬»бФміЙКөСйҪб№ыЖ«өНөДКЗЈЁ Ј©
A. јУИИКұјд№эіӨЈ¬№ММеІҝ·ЦұдәЪB. ЫбЫцДЪёҪУРІ»»У·ўФУЦК
C. ҫ§МеІ»ҙҝЈ¬ә¬УРІ»»У·ўФУЦКD. јУИИ№эіМЦРУРЙЩБҝҫ§МеҪҰіц
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіёцМеРЎГәҝуФш·ўЙъНЯЛ№ұ¬ХЁКВ№К,ФміЙИЛФұЙЛНцЎЈФЪГәҝуҝуҫ®Ап,ұШРлІЙИЎ°ІИ«ҙлК©,ИзНЁ·зЎўСПҪыСМ»рөИ,¶шЗТТӘЛжКұјмІйНЯЛ№өДМе»э·ЦКэ,Из№ыҝХЖшЦРә¬јЧНйөДМе»э·ЦКэОӘ5%~15.4%,УцөҪГч»р»б·ўЙъұ¬ХЁЎЈ·ўЙъЧоЗҝБТұ¬ХЁКұҝХЖшЦРјЧНйЛщХјөДМе»э·ЦКэФјКЗ
A. 5% B. 9.1% C. 10.5% D. 15%
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВұнОӘФӘЛШЦЬЖЪұнөДТ»Іҝ·ЦЈ¬ЗлІОХХФӘЛШўЩЈӯўбФЪұнЦРөДО»ЦГЈ¬УГ»ҜС§УГУп»ШҙрПВБРОКМвЈә
Че ЦЬЖЪ | IA | 0 | ||||||
1 | ўЩ | ўтA | ўуA | ўфA | ўхA | ўцA | ўчA | |
2 | ўЪ | ўЫ | ўЬ | ўЭ | ||||
3 | ўЮ | ўЯ | ўа | ўб | ||||
(1)ФӯЧУ°лҫ¶ЧоРЎөДФӘЛШКЗ____ЈЁМоФӘЛШГыіЖЈ©Ј¬РҙіцўаөДФӯЧУҪб№№КҫТвНј______ЎЈ
(2)ЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОпЦРЈ¬јоРФЧоЗҝөДКЗ___ЈЁУГ»ҜС§КҪ»ШҙрЈ¬ПВН¬Ј©Ј¬ЛбРФЧоЗҝөДКЗ___ЎЈ
(3)ўЩУлўЭРОіЙөД»ҜәПОпЦРЈ¬»ҜС§јьАаРНОӘ_____ЎЈ
(4)ўЯУлўбРОіЙөД»ҜәПОпөДөзЧУКҪОӘ___Ј¬ўЪУлўЬРОіЙөДФӯЧУёцКэұИОӘ1:2өД»ҜәПОпөДҪб№№КҪОӘ____ЎЈ
(5)ўЫЎўўЬЎўўЮөДФӯЧУ°лҫ¶УЙҙуөҪРЎөДЛіРтОӘ_____ЈЁУГФӘЛШ·ыәЕ»ШҙрЈ©ЎЈ
(6)ОӘМҪҫҝФӘЛШўЪәНўаөД·ЗҪрКфРФЗҝИхЈ¬ДіН¬С§ЙијЖБЛИзНјЛщКҫөДЧ°ЦГҪшРРКөСйЈЁјРіЦТЗЖчТСВФИҘЈ¬Ч°ЦГЖшГЬРФБјәГЈ©ЎЈЗл»ШҙрЈә

a.ИЬТәBөДЧчУГКЗ_______
b.ИфҝҙөҪ____ПЦПуЈ¬јҙҝЙЦӨГчЛбРФ_______ЈЁУГ»ҜС§КҪ»ШҙрЈ©Ј¬Фт·ЗҪрКфРФ_______ЈЁУГФӘЛШ·ыәЕ»ШҙрЈ©ЎЈ
c.ЙПКцКөСйЦРЈ¬ДЬЛөГчўЪәНўа·ЗҪрКфРФЗҝИхөД»ҜС§·ҪіМКҪКЗ_____________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝЙиNAұнКҫ°ў·ьјУөВВЮіЈКэөДЦөЎЈПВБРЛө·ЁХэИ·өДКЗ
A.15g 14COУл15N2өД»мәПЖшМеЛщә¬ЦКЧУКэОӘ7.5NA
B.11.2L Cl2УлNaOHИЬТә·ҙУҰЈ¬ЧӘТЖөзЧУКэОӘ0.5NA
C.2mol SO2Ул1mol O2·ҙУҰЙъіЙSO3өД·ЦЧУКэОӘ2NA
D.6g MgSO4УлNaHSO4өД»мәПОпЛщә¬СхФӯЧУКэОӘ0.2NA
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com