
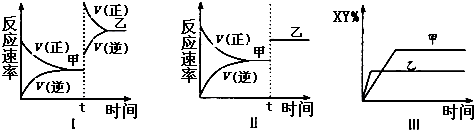
| A、图I中,甲、乙的平衡常数分别为K1、K2,则K1<K2 |
| B、图Ⅱ中,平衡状态甲与乙相比,平衡状态甲的反应物转化率低 |
| C、图Ⅱ中,t时间是增大了压强 |
| D、图Ⅲ是反应分别在甲、乙条件下达到平衡,说明乙温度高于甲 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯水中的次氯酸具有杀菌消毒作用 |
| B、陶瓷的主要成分是碳酸钙 |
| C、硅是制造太阳能电池的常用材料 |
| D、漂白粉的有效成分是次氯酸钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
| B、用PH试纸测得氯水的PH约为3 |
| C、纯净的H2在Cl2中安静的燃烧,发出苍白色的火焰,集气瓶口有白烟生成 |
| D、氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
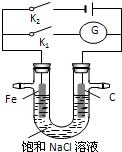
| A、K1闭合,铁棒上发生的反应为2H++2e-→H2↑ |
| B、K1闭合,石墨棒周围溶液pH逐渐升高 |
| C、K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 |
| D、K2闭合,电路中通过0.4NA个电子时,两极共产生标况下4.48L气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuSO4溶液与Ba(OH)2溶液混合:Ba2++SO42-=BaSO4↓ |
| B、澄清石灰水与稀盐酸反应:OH-+H+=H2O |
| C、NaHSO3溶液与NaHSO4溶液混合:SO32-+2H+=H2O+SO2↑ |
| D、铁钉放入硫酸铜溶液中:Fe+3Cu2+=2Fe3++3Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com