
【题目】下列气体不能用排空气法收集的是( )
A.SO2
B.NH3
C.NO
D.NO2
科目:高中化学 来源: 题型:
【题目】已知W、X、Y、Z为短周期元素,原子序数依次增大。W、Z同主族,X、Y、Z
同周期,其中只有X为金属元素。下列说法一定正确的是
A.原子半径:X>Y>Z>W
B.W的含氧酸的酸性比Z的含氧酸的酸性强
C.W的气态氢化物的稳定性小于Y的气态氢化物的稳定性
D.若W与X原子序数差为5,则形成化合物的化学式为X3W2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生活、环境保护密切相关,下列现象或事实与解释一致的是
编号 | 现象或事实 | 解释 |
A | SiO2+Na2CO3 | 酸性:H2SiO3>H2CO3 |
B | 2Mg+CO2 | 还原性:Mg>C |
C | 漂白粉因在空气中放置时间过久而变质 | 漂白粉中的CaCl2与空气中的CO2反应生成碳酸钙 |
D | 利用氯化铁溶液可以制作铜质印刷线路板 | FeCl3溶液置换出铜单质 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g)。经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(g)。经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol·L-1。其中正确的是
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期元素,且原子序数依次增大;A的主族序数、周期数、原子序数均相同;B为非金属元素,其单质有多种同素异形体,其中一种可作电极材料;C是植物生长所需的主要元素之一;D和A可形成A2D和A2D2,A2D是最常见的溶剂;E原子次外层电子电子数等于其它层电子数之和。则
(1)E在周期表中的位置是______________,B、C、D、E与A形成的化合物中稳定性最强的是_______(该化学式)。
(2)C、D、E的离子半径由大至小顺序______________。
(3)写出B与由A、C、D组成的化合物的浓溶液在加热条件下的反应方程式:_________。
(4)A-E五种元素中,含同一元素的各类物质能实现下列转化的有______(填元素符号)。
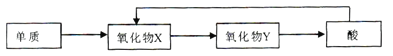
(5)A2D2与FeSO4溶于稀硫酸,反应的离子方程式为_________。
(6)由A、B、C、D四种元素组成的化合物A,其原子个致比为7: 2 : l : 2,则A为(名称)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制适合的条件,将反应2Fe3++2I-![]() 2Fe2++I2设计成如图所示的原电池。下列判断不正确的是( )
2Fe2++I2设计成如图所示的原电池。下列判断不正确的是( )
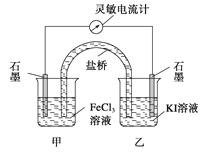
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上的Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中的石墨电极为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 高纯度的晶体硅可以制备晶体管等半导体、电脑芯片和光导纤维
B. PM 2.5是指大气中直径接近2.5×10-6 m的颗粒物,它分散在空气中形成胶体
C. 受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗,并视情况作进一步处理
D. NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是( )
A. 与NaOH反应的氯气一定为0.3 mol
B. n(Na+):n(Cl-)可能为7:3
C. 若反应中转移的电子为n mol,则0.15<n<0.25
D. n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com