
【题目】常温下,下列离子在指定溶液中一定能大量共存的是
A.0.1mol·L-1NaHCO3溶液:K+、Al3+、NO3-、SO42-
B.![]() 10-12的溶液中:Na+、K+、ClO-、CO32-
10-12的溶液中:Na+、K+、ClO-、CO32-
C.能使红色石蕊试纸变蓝的溶液:NH4+、K+、Cl-、NO3-
D.水电离的c(H+)=10—11mol·L-1的溶液中:Na+、Ca2+、HCO3-、Cl-
科目:高中化学 来源: 题型:
【题目】常温下,向20mL![]()
![]() 溶液中滴加
溶液中滴加![]() NaOH溶液.有关微粒的物质的量变化如图,下列说法正确的是
NaOH溶液.有关微粒的物质的量变化如图,下列说法正确的是
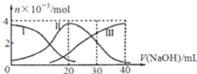
A.滴加过程中当溶液呈中性时,![]()
B.当![]() 时,则有:
时,则有:![]()
C.H![]() 在水中的电离方程式是:H
在水中的电离方程式是:H![]() ;
;![]()
D.当![]() 时,则有:
时,则有:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型储氢材料是开发利用氢能的重要研究方向。
(1)元素N的价电子数排布式为3d24s2,其氯化物NCl4和LiBH4反应可制得储氢材料N(BH4)3。
①元素N在周期表中的位置为__,该原子具有__种运动状态不同的电子。
②化合物LiBH4中含有的化学键有__,BH4-的立体构型是_,B原子的杂化轨道类型是__,B原子轨道表达式为__。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+__H-(填“>”“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:M的最高正价是__。
I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
(3)NaH具有NaCl型晶体结构,Na+的配位数为__,晶体的堆积方式为__,已知NaH晶体的晶胞参数a=488pm,Na+半径为102pm,H-的半径为pm,NaH的理论密度是__g·cm-3。(仅写表达式,不计算)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F代表原子序数依次增大的前四周期元素。其中A是空气中含量最高的元素;B是同周期中原子半径最大的元素;C原子的最外层电子数与核外电子层数相等;D、E元素的基态原子3p能级上都有两个未成对电子;F原子的外围电子排布为(n-1)d10ns1。根据以上信息,回答下列问题:
(1)A元素基态原子核外电子的轨道表达式为________________;在同周期元素中第一电离能介于C、E之间的元素是______(用化学式表示)。
(2)将以下三种物质:①A与硼元素按原子个数比为1∶1形成的空间网状结构化合物,②B的氯化物, ③D的氯化物。按熔点由高到低的顺序排列:______________(用化学式表示)。
(3)A的最简单氢化物易液化,其原因是_______________,E的次高价含氧酸根离子的VSEPR模型名称是_________,该离子的空间构型为__________。
(4)F单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
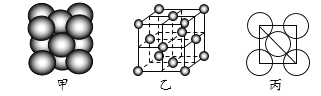

若已知F晶胞参数为a pm,F相对原子质量为M,NA代表阿伏加德罗常数,请回答:
①晶胞中F原子的配位数为_______;F单质晶体中原子的堆积方式是_________堆积。
②F原子半径r =________pm,F单质晶体密度计算式为:______________ g·cm-3。
(5)A与F形成的某种化合物晶胞结构如图丁所示,该晶体的化学式为___________。该化合物能与稀盐酸剧烈反应,生成一种白色沉淀和一种全部由非金属元素组成的离子化合物,该反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
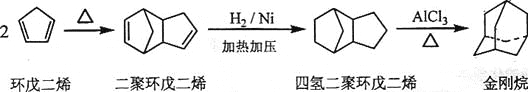
请回答下列问题:
(1)环戊二烯分子中最多有___个原子共平面;
(2)金刚烷的分子式为___________,其分子中的CH2基团有______个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
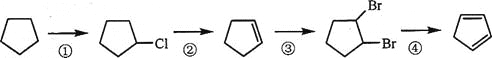
其中,反应①的产物名称是__________,反应②的反应试剂和反应条件是__________,反应③的反应类型是__________;
(4)已知烯烃能发生如下反应:
![]()
请写出下列反应产物的结构简式: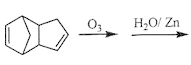 __________;
__________;
(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环上的烷基(-CH3,-CH2R,-CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基],写出A所有可能的结构简式(不考虑立体异构):_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能被视为21世纪最具发展潜力的清洁能源。根据下列图示有关说法正确的是
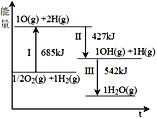
A.断开非极性键和生成极性键的能量相同
B.反应II比反应III生成的O-H键更牢固
C.1/2O2(g) +H2(g) → OH(g) + H(g) ΔH1>0
D.H2O(g)→ 1/2O2(g) +H2(g) ΔH2<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡为ⅣA族元素,四碘化锡是常用的有机合成试剂(SnI4,熔点144.5℃,沸点364.5℃,易水解)。实验室以过量锡箔为原料通过反应Sn+2I2![]() SnI4制备SnI4。下列说法错误的是
SnI4制备SnI4。下列说法错误的是
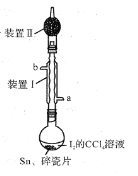
A.装置Ⅱ的主要作用是吸收挥发的I2
B.SnI4可溶于CCl4中
C.装置Ⅰ中a为冷凝水进水口
D.加入碎瓷片的目的是防止暴沸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10mL1mol·L-1的HCOOH溶液中不断滴加1mol·L-1的NaOH溶液,并一直保持常温,所加碱的体积与-lgc水(H+)的关系如图所示。c水(H+)为溶液中水电离的c(H+)。下列说法不正确的是( )
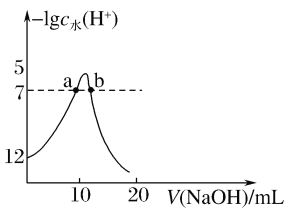
A.常温下,Ka(HCOOH)的数量级为10-4
B.a、b两点pH均为7
C.从a点到b点,水的电离程度先增大后减小
D.混合溶液的导电性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四组物质,用横线上所给的试剂常温下就能鉴别出来的是( )
A.FeO、FeS、CuO、CuS、稀硫酸
B.苯、四氯化碳、无水乙醇、己烯 溴水
C.甲酸、乙酸、乙醛、乙醇 新制氢氧化铜悬浊液
D.苯酚钠溶液、甲苯、乙酸乙酯、乙酸 饱和碳酸钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com