
ЁОЬтФПЁПЫФбѕЛЏШ§УЬЃЈMn3O4ЃЉЙуЗКгІгУгкЩњВњШэДХВФСЯЁЂДпЛЏВФСЯжЦБИСьгђЁЃвЛжжвдЕЭЦЗЮЛУЬПѓЃЈКЌMnCO3ЁЂMn2O3ЁЂMnOOHМАЩйСПFe2O3ЁЂAl2O3ЁЂSiO2ЃЉЮЊдСЯЩњВњMn3O4ЕФЙЄвеСїГЬШчЭМЃК

вбжЊЃК(NH4)2SO4![]() NH3Ёќ+NH4HSO4
NH3Ёќ+NH4HSO4
ЛиД№ЯТСаЮЪЬтЃК
(1)MnOOHжаMnЕФЛЏКЯМлЮЊ___ЁЃ
(2) ЁАШмНўЁБжаH2O2ЕФзїгУЪЧ___ЁЃ
(3) ЁАТЫдќ2ЁБЕФжївЊГЩЗжга___ЁЃ
(4) ЁАФИвКЁБШмжЪЕФжївЊГЩЗжЪЧ___ЃЌбЛЗРћгУИУЮяжЪЕФЗНАИЪЧ___ЁЃ
(5)бѕЛЏЁБЪБЃЌНЋЙЬЬхМгШыЫЎжаЃЌ70ЁцЫЎдЁМгШШЃЌЭЈПеЦјбѕЛЏЃЌНЋЙЬЬхШЋВПзЊЛЏЮЊMn3O4ЁЃMn(OH)2ЩњГЩMn3O4ЕФЛЏбЇЗНГЬЪНЮЊ___ЁЃЗДгІКѓШмвКpH___ЃЈЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБЃЉЁЃ
ЁОД№АИЁП+3 НЋ+3МлMnдЊЫиЛЙдГЩMn2+ Fe(OH)3ЁЂAl(OH)3 (NH4)2SO4 МгШШЕН213~308ЁцЗжНтЩњГЩАБЦјКЭNH4HSO4ЃЌЗжБ№бЛЗЕНГСУЬКЭШмНўжаЃЌЛђМгH2SO4ЩњГЩNH4HSO4бЛЗЕНШмНўжа 6Mn(OH)2+O2![]() 2Mn3O4+6H2O МѕаЁ
2Mn3O4+6H2O МѕаЁ
ЁОНтЮіЁП
УЬПѓЗл(КЌMnCO3ЁЂMn2O3ЁЂMnOOHМАЩйСПFe2O3ЁЂAl2O3ЁЂSiO2)МгNH4HSO4ЁЂH2O2ШмНўЃЌMnCO3ЁЂMn2O3ЁЂMnOOHзЊЛЏЮЊMn2+ЃЌFe2O3ЁЂAl2O3зЊЛЏЮЊFe2+ЁЂAl3+ЃЌSiO2ВЛШмЖјГЩТЫдќ1ЃЛМгШыMn(OH)2ЕїpH=5ЃЌДЫЪБFe3+ЁЂAl3+зЊЛЏЮЊFe(OH)3ЁЂAl(OH)3ЃЌГЩЮЊТЫдќ2ЕФГЩЗжЃЛМгШыАБЫЎГСУЬЃЌДЫЪБУЬзЊЛЏЮЊMn(OH)2ЁЂMn2(OH)2SO4ЃЌЭЈПеЦјбѕЛЏЃЌ70ЁцЫЎдЁМгШШЃЌМДЕУMn3O4ЁЃ
(1)MnOOHжаOЯд-2МлЃЌHЯд+1МлЃЌвРОнЛЏКЯМлЕФДњЪ§ЮЊ0ЃЌПЩЧѓГіMnЕФЛЏКЯМлЮЊ+3ЁЃД№АИЮЊЃК+3ЃЛ
(2) ЁАШмНўЁБжаЃЌгавЛВПЗжMnгЩ+3МлНЕЮЊ+2МлЃЌЫљвдH2O2ЕФзїгУЪЧНЋ+3МлMnдЊЫиЛЙдГЩMn2+ЁЃД№АИЮЊЃКНЋ+3МлMnдЊЫиЛЙдГЩMn2+ЃЛ
(3) гЩвдЩЯЗжЮіжЊЃЌЁАТЫдќ2ЁБЕФжївЊГЩЗжгаFe(OH)3ЁЂAl(OH)3ЁЃД№АИЮЊЃКFe(OH)3ЁЂAl(OH)3ЃЛ
(4) гЩвдЩЯЗжЮіжЊЃЌЁАФИвКЁБШмжЪЕФжївЊГЩЗжЪЧ(NH4)2SO4ЃЌбЛЗРћгУИУЮяжЪЕФЗНАИЪЧМгШШЕН213~308ЁцЗжНтЩњГЩАБЦјКЭNH4HSO4ЃЌЗжБ№бЛЗЕНГСУЬКЭШмНўжаЃЌЛђМгH2SO4ЩњГЩNH4HSO4бЛЗЕНШмНўжаЁЃД№АИЮЊЃК(NH4)2SO4ЃЛМгШШЕН213~308ЁцЗжНтЩњГЩАБЦјКЭNH4HSO4ЃЌЗжБ№бЛЗЕНГСУЬКЭШмНўжаЃЌЛђМгH2SO4ЩњГЩNH4HSO4бЛЗЕНШмНўжаЃЛ
(5)бѕЛЏЁБЪБЃЌMn(OH)2РћгУ70ЁцЫЎдЁМгШШЃЌЭЈПеЦјбѕЛЏЃЌЩњГЩMn3O4ЃЌЛЏбЇЗНГЬЪНЮЊ6Mn(OH)2+O2![]() 2Mn3O4+6H2OЁЃMn(OH)2ГЪМюадЃЌMn3O4ФбШмгкЫЎЃЌЫљвдЗДгІКѓШмвКpHМѕаЁЁЃД№АИЮЊЃК6Mn(OH)2+O2
2Mn3O4+6H2OЁЃMn(OH)2ГЪМюадЃЌMn3O4ФбШмгкЫЎЃЌЫљвдЗДгІКѓШмвКpHМѕаЁЁЃД№АИЮЊЃК6Mn(OH)2+O2![]() 2Mn3O4+6H2OЃЛМѕаЁЁЃ
2Mn3O4+6H2OЃЛМѕаЁЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПБНЕФНсЙЙМђЪНПЩгУ![]() РДБэЪОЃЌЯТСаЙигкБНЕФа№Ъіжае§ШЗЕФЪЧ
РДБэЪОЃЌЯТСаЙигкБНЕФа№Ъіжае§ШЗЕФЪЧ
A. БНжївЊЪЧвдЪЏгЭЮЊдСЯЖјЛёЕУЕФвЛжжживЊЛЏЙЄдСЯ
B. БНжаКЌгаЬМЬМЫЋМќЃЌЫљвдБНЪєгкЯЉЬў
C. БНЗжзгжа6ИіЬМЬМЛЏбЇМќЭъШЋЯрЭЌ
D. БНПЩвдгыфхЫЎЁЂИпУЬЫсМиШмвКЗДгІЖјЪЙЫќУЧЭЪЩЋ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМюадаПУЬЕчГиБШЦеЭЈЕФаПУЬИЩЕчГиадФмгХдНЃЌФмЬсЙЉНЯДѓЕФЕчСїВЂСЌајЗХЕчЃЌЦфЙЙдьШчЭМЫљЪОЁЃЕчГиЗДгІЗНГЬЪНЮЊ 2MnO2+Zn+2H2O=2MnO (OH)+Zn (OH)2ЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
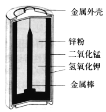
A.ЕчГиЪЙгУЙ§ГЬжаЃЌЕчНтжЪЕФМюаддіЧП
B.аПЗлЪЧИУЕчГиЕФИКМЋ
C.MnO2 ЕчМЋЕФЕчМЋЗДгІЪНЃКMnO2+eЁЅЃЋH2O=MnO(OH)+OHЁЅ
D.ЕБЕчГиЪЙгУЪБЃЌOHЁЅвЦЯђЕчГиЕФе§МЋ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП5ЉЖўМзбѕЛљБНЗгЪЧживЊЕФгаЛњКЯГЩжаМфЬхЃЌПЩгУгкЬьШЛЮяжЪАзФћУЪЫиЕФКЯГЩЃЌвЛжжвдМфБНШ§ЗгЮЊдСЯЕФКЯГЩЗДгІШчЯТЃК

МзДМЁЂввУбКЭ3ЃЌ5ЉЖўМзбѕЛљБНЗгЕФВПЗжЮяРэаджЪМћЯТБэЃК
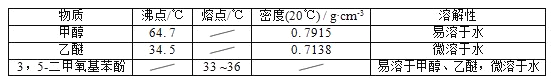
ЃЈ1ЃЉЗДгІНсЪјКѓЃЌЯШЗжРыГіМзДМЃЌдйМгШыввУбНјаанЭШЁЃЌЂйЗжРыГіМзДМЕФВйзїЪЧЕФ______ЃЛЂкнЭШЁгУЕНЕФЗжвКТЉЖЗЪЙгУЧАаш__________________ВЂЯДОЛЃЌЗжвКЪБгаЛњВудкЗжвКТЉЖЗЕФ________ЬюЃЈЁАЩЯЁБЛђЁАЯТЁБЃЉВуЃЛ
ЃЈ2ЃЉЗжРыЕУЕНЕФгаЛњВувРДЮгУБЅКЭNaHCO3ШмвКЁЂБЅКЭЪГбЮЫЎЁЂЩйСПеєСѓЫЎНјааЯДЕгЃЎгУБЅКЭNaHCO3ШмвКЯДЕгЕФФПЕФЪЧ__ЃЌгУБЅКЭЪГбЮЫЎЯДЕгЕФФПЕФЪЧ______ЃЛ
ЃЈ3ЃЉЯДЕгЭъГЩКѓЃЌЭЈЙ§вдЯТВйзїЗжРыЁЂЬсДПВњЮяЃЌе§ШЗЕФВйзїЫГађЪЧ__ЃЈЬюзжФИЃЉЃЛ
aЃЎеєСѓГ§ШЅввУб bЃЎжиНсОЇ cЃЎЙ§ТЫГ§ШЅИЩдяМС dЃЎМгШыЮоЫЎCaCl2ИЩдя
ЃЈ4ЃЉЙЬвКЗжРыГЃВЩгУМѕбЙЙ§ТЫЃЎЮЊСЫЗРжЙЕЙЮќЃЌМѕбЙЙ§ТЫЭъГЩКѓгІЯШ________________ЃЌдй______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪнШтОЋЃЌбЇУћбЮЫсПЫТзЬиТоЃЌИУвЉЮяМШВЛЪЧЪовЉЃЌвВВЛЪЧЫЧСЯЬэМгМСЃЌЖјЪЧЩіЩЯЯйРрЩёОаЫЗмМСЃЌПЩвддіМгЖЏЮяЕФЪнШтСП.МѕЩйЫЧСЯЪЙгУ.ЪЙШтЦЗЬсдчЩЯЪаЃЌНЕЕЭГЩБОЃЌЕЋЖдШЫЬхЛсВњЩњИБзїгУЃЌбЮЫсПЫТзЬиТоЗжзгНсЙЙМђЪНШчЯТЭМЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
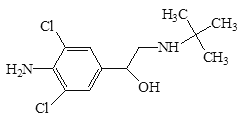
AЃЎЪнШтОЋЕФЗжзгЪНЪЧC11H18ON2Cl2
BЃЎЮяжЪФмЗЂЩњШЁДњЗДгІЁЂбѕЛЏЗДгІЁЂМгГЩЗДгІКЭЫЎНтЗДгІ
CЃЎ1molбЮЫсПЫТзЬиТозюЖрФмгы4molNaOHЗДгІ
DЃЎбЮЫсПЫТзЬиТоЗжзгжажСЩйга7ИіЬМдзгЙВУц
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГбЇЯАаЁзщЖдШЫНЬАцНЬВФЪЕбщЁАдк200mLЩеБжаЗХШы20gесЬЧЃЈC12H22O11ЃЉЃЌМгШыЪЪСПЫЎЃЌНСАшОљдШЃЌШЛКѓдйМгШы15mLжЪСПЗжЪ§ЮЊ98%ХЈСђЫсЃЌбИЫйНСАшЁБНјааШчЯТЬНОПЃЛ
ЃЈ1ЃЉЙлВьЯжЯѓЃКесЬЧЯШБфЛЦЃЌдйж№НЅБфКкЃЌЬхЛ§ХђеЭЃЌаЮГЩЪшЫЩЖрПзЕФКЃУрзДКкЩЋЮяжЪЃЌЭЌЪБЮХЕНДЬМЄадЦјЮЖЃЌАДбЙДЫКкЩЋЮяжЪЪБЃЌИаОѕНЯгВЃЌЗХдкЫЎжаГЪЦЏИЁзДЬЌЃЌЭЌбЇУЧгЩЩЯЪіЯжЯѓЭЦВтГіЯТСаНсТлЃК
ЂйХЈСђЫсОпгаЧПбѕЛЏад ЂкХЈСђЫсОпгаЮќЫЎад ЂлХЈСђЫсОпгаЭбЫЎадЂмХЈСђЫсОпгаЫсад ЂнКкЩЋЮяжЪОпгаЧПЮќИНад
ЦфжавРОнВЛГфЗжЕФЪЧ_________ЃЈЬюађКХЃЉЃЛ
ЃЈ2ЃЉЮЊСЫбщжЄесЬЧгыХЈСђЫсЗДгІЩњГЩЕФЦјЬЌВњЮяЃЌЭЌбЇУЧЩшМЦСЫШчЯТзАжУЃК

ЪдЛиД№ЯТСаЮЪЬтЃК
ЂйЭМ1ЕФAжазюКУбЁгУЯТСазАжУ_________ЃЈЬюБрКХЃЉЃЛ
ЂкЭМ1ЕФ BзАжУЫљзАЪдМСЪЧ_________ЃЛDзАжУжаЪдМСЕФзїгУЪЧ_________ЃЛEзАжУжаЗЂЩњЕФЯжЯѓЪЧ_________ЃЛ
ЂлЭМ1ЕФAзАжУжаЪЙесЬЧЯШБфКкЕФЛЏбЇЗДгІЗНГЬЪНЮЊ_________ЃЌКѓЬхЛ§ХђеЭЕФЛЏбЇЗНГЬЪНЮЊЃК_________ЃЛ
ЂмФГбЇЩњАДЭМ2НјааЪЕбщЪБЃЌЗЂЯжDЦПЦЗКьВЛЭЪЩЋЃЌEзАжУжагаЦјЬхвнГіЃЌFзАжУжаЫсадИпУЬЫсМиШмвКбеЩЋБфЧГЃЌЭЦВтFзАжУжаЫсадИпУЬЫсМиШмвКбеЩЋБфЧГЕФдвђ_________ЃЌЦфЗДгІЕФРызгЗНГЬЪНЪЧ_________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПКЯГЩАБЪЧФПЧАзюгааЇЙЄвЕЙЬЕЊЕФЗНЗЈЃЌНтОіЪ§вкШЫПкЩњДцЮЪЬтЁЃЛиД№ЯТСаЮЪЬтЃК
(1)ПЦбЇМвбаОПРћгУЬњДЅУНДпЛЏКЯГЩАБЕФЗДгІРњГЬШчЭМЫљЪОЃЌЦфжаЮќИНдкДпЛЏМСБэУцЕФЮяжжгУЁАadЁББэЪОЁЃ

гЩЭМПЩжЊКЯГЩАБЗДгІ![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g)ЕФH=___ kJЁЄmol-1ЁЃИУРњГЬжаЗДгІЫйТЪзюТ§ЕФВНжшЕФЛЏбЇЗНГЬЪНЮЊ___ЁЃ
NH3(g)ЕФH=___ kJЁЄmol-1ЁЃИУРњГЬжаЗДгІЫйТЪзюТ§ЕФВНжшЕФЛЏбЇЗНГЬЪНЮЊ___ЁЃ
(2)ЙЄвЕКЯГЩАБЗДгІЮЊЃКN2(g)+3H2(g)![]() 2NH3(g)ЃЌЕБНјСЯЬхЛ§БШV(N2)ЃКV(H2)=1ЃК3ЪБЦНКтЦјЬхжаNH3ЕФЮяжЪЕФСПЗжЪ§ЫцЮТЖШКЭбЙЧПБфЛЏЕФЙиЯЕШчЭМЫљЪОЃК
2NH3(g)ЃЌЕБНјСЯЬхЛ§БШV(N2)ЃКV(H2)=1ЃК3ЪБЦНКтЦјЬхжаNH3ЕФЮяжЪЕФСПЗжЪ§ЫцЮТЖШКЭбЙЧПБфЛЏЕФЙиЯЕШчЭМЫљЪОЃК

Ђй500ЁцЪБЃЌЗДгІЦНКтГЃЪ§Kp(30MPa)___ Kp(100MPa)ЁЃЃЈЬюЁА<ЁБЁЂЁА=ЁБЁЂЁА>ЁБЃЉ
Ђк500ЁцЁЂ30MPaЪБЃЌЧтЦјЕФЦНКтзЊЛЏТЪЮЊ___ЃЈБЃСє2ЮЛгааЇЪ§зжЃЉЃЌKp=___(MPa)-2ЃЈСаГіМЦЫуЪНЃЉЁЃ
(3)ПЦбЇМвРћгУЕчНтЗЈдкГЃЮТГЃбЙЯТЪЕЯжКЯГЩАБЃЌЙЄзїЪБвѕМЋЧјЕФЮЂЙлЪОвтШчЭМЃЌЦфжаЕчНтвКЮЊШмНтгаШ§ЗњМзЛЧЫсяЎКЭввДМЕФЖшадгаЛњШмМСЁЃ

ЂйвѕМЋЧјЩњГЩNH3ЕФЕчМЋЗНГЬЪНЮЊ___ЁЃ
ЂкЯТСаЫЕЗЈе§ШЗЕФЪЧ___ЃЈЬюБъКХЃЉЁЃ
AЃЎШ§ЗњМзЛЧЫсяЎЕФзїгУЪЧдіЧПЕМЕчад
BЃЎИУзАжУгУН№(Au)зїДпЛЏМСФПЕФЪЧНЕЕЭN2ЕФМќФм
CЃЎбЁдёадЭИЙ§ФЄПЩдЪаэN2КЭNH3ЭЈЙ§ЃЌЗРжЙH2OНјШызАжУ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУ50mL0.50mol/LбЮЫсгы50mL0.55mol/LNaOHШмвКдкШчЭМЫљЪОЕФзАжУжаНјаажаКЭЗДгІЁЃЭЈЙ§ВтЖЈЗДгІЙ§ГЬжаЫљЗХГіЕФШШСППЩМЦЫужаКЭШШЁЃЛиД№ЯТСаЮЪЬтЃК
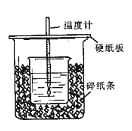
ЃЈ1ЃЉДгЪЕбщзАжУЩЯПДЃЌЭМжаЩаШБЩйЕФвЛжжВЃСЇвЧЦїЪЧ ЁЃ
ЃЈ2ЃЉЩеБМфЬюТњЫщжНЬѕЕФзїгУЪЧ ЁЃ
ЃЈ3ЃЉДѓЩеБЩЯШчВЛИЧгВжНАхЃЌЧѓЕУЕФжаКЭШШЪ§жЕ (ЬюЁАЦЋДѓЁЂЦЋаЁЁЂЮогАЯьЁБ)
ЃЈ4ЃЉШчЙћгУ60mL0.50mol/LбЮЫсгы50mL0.55mol/LNaOHШмвКНјааЗДгІЃЌгыЩЯЪіЪЕбщЯрБШЃЌЫљЗХГіЕФШШСП (ЬюЁАЯрЕШЁЂВЛЯрЕШЁБ)ЃЌЫљЧѓжаКЭШШ (ЬюЁАЯрЕШЁЂВЛЯрЕШЁБ)ЃЌМђЪіРэгЩ
ЃЈ5ЃЉгУЯрЭЌХЈЖШКЭЬхЛ§ЕФАБЫЎ(NH3ЁЄH2O)ДњЬцNaOHШмвКНјааЩЯЪіЪЕбщЃЌВтЕУЕФжаКЭШШЕФЪ§жЕЛс ЃЛЃЈЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЁЂЁАЮогАЯьЁБЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПввЯЉЁЂБНввЯЉОљЪЧживЊЕФЛЏЙЄдСЯЁЃ
![]() ЙЄвЕЩЯПЩгУввБНДпЛЏЭбЧтЗНЗЈжЦБИБНввЯЉ
ЙЄвЕЩЯПЩгУввБНДпЛЏЭбЧтЗНЗЈжЦБИБНввЯЉ
ЂйвбжЊВПЗжЛЏбЇМќЕФМќФмШчЯТЃК
ЛЏбЇМќ | C-H | C-C |
| H-H |
МќФм/(kJ/mol) | 412 | 348 | 612 | 436 |
дђ![]() +H2(g)ЕФ
+H2(g)ЕФ![]() ________kJ/molЁЃ
________kJ/molЁЃ
ЂкЪЕМЪЩњВњжаГЃдкКубЙЬѕМўЯТВєШыИпЮТЫЎеєЦјзїЮЊЗДгІЬхЯЕЕФЯЁЪЭМС![]() ЫЎеєЦјВЛВЮМгЗДгІ
ЫЎеєЦјВЛВЮМгЗДгІ![]() ЁЃдквЛЖЈбЙЧПЁЂ900 KЕФЬѕМўЯТЃЌввБНЕФЦНКтзЊЛЏТЪЫцзХ
ЁЃдквЛЖЈбЙЧПЁЂ900 KЕФЬѕМўЯТЃЌввБНЕФЦНКтзЊЛЏТЪЫцзХ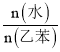 ЕФдіДѓЖј________
ЕФдіДѓЖј________![]() ЬюЁАдіДѓЁБЁАМѕаЁЁБЛђЁАВЛБфЁБ
ЬюЁАдіДѓЁБЁАМѕаЁЁБЛђЁАВЛБфЁБ![]() ЁЃЫцзХЗДгІЕФНјааЃЌЩйСПЛ§ЬМЛсЪЙДпЛЏМСЛюадМѕШѕЃЌЫЎеєЦјЛЙгаРћгкЛжИДДпЛЏМСЛюадЃЌдвђЪЧ____________
ЁЃЫцзХЗДгІЕФНјааЃЌЩйСПЛ§ЬМЛсЪЙДпЛЏМСЛюадМѕШѕЃЌЫЎеєЦјЛЙгаРћгкЛжИДДпЛЏМСЛюадЃЌдвђЪЧ____________![]() гУЛЏбЇЗНГЬЪНБэЪО
гУЛЏбЇЗНГЬЪНБэЪО![]() ЁЃ
ЁЃ
![]() БНввЯЉПЩгЩввБНКЭ
БНввЯЉПЩгЩввБНКЭ![]() ДпЛЏЭбЧтжЦЕУЁЃЦфЗДгІРњГЬШчЯТЃК
ДпЛЏЭбЧтжЦЕУЁЃЦфЗДгІРњГЬШчЯТЃК
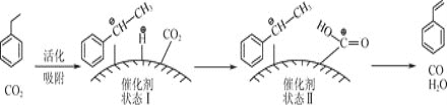
ввБНЦНКтзЊЛЏТЪгы![]() ЕФЙиЯЕШчЭМЫљЪОЃЌЕБP(CO2)< 15 kPaЪБЃЌввБНЦНКтзЊЛЏТЪЫцзХ
ЕФЙиЯЕШчЭМЫљЪОЃЌЕБP(CO2)< 15 kPaЪБЃЌввБНЦНКтзЊЛЏТЪЫцзХ![]() діДѓЖјдіДѓЃЌЦфдвђЪЧ__________ЃЌЕБP(CO2)> 15 kPaЪБЃЌввБНЦНКтзЊЛЏТЪЫцзХ
діДѓЖјдіДѓЃЌЦфдвђЪЧ__________ЃЌЕБP(CO2)> 15 kPaЪБЃЌввБНЦНКтзЊЛЏТЪЫцзХ![]() діДѓЗДЖјМѕаЁЃЌЦфдвђЪЧ____________ЁЃ
діДѓЗДЖјМѕаЁЃЌЦфдвђЪЧ____________ЁЃ
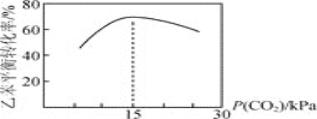
![]() баОПБэУїН№ЪєДЮпВпјЖўМзѕЅФмЙЛЫГРћЕибЁдёадДпЛЏбѕЛЏБНввЯЉЩњГЩБНМзШЉЃЌвдИУЗДгІдРэЩшМЦГЩЫсадШМСЯЕчГиЃЌдђЕчГиИКМЋЕФЕчМЋЗДгІЪНЮЊ ________ЁЃШєИУЕчГиЯћКФБъзМзДПіЯТ22.4LЕФ
баОПБэУїН№ЪєДЮпВпјЖўМзѕЅФмЙЛЫГРћЕибЁдёадДпЛЏбѕЛЏБНввЯЉЩњГЩБНМзШЉЃЌвдИУЗДгІдРэЩшМЦГЩЫсадШМСЯЕчГиЃЌдђЕчГиИКМЋЕФЕчМЋЗДгІЪНЮЊ ________ЁЃШєИУЕчГиЯћКФБъзМзДПіЯТ22.4LЕФ![]() ЃЌдђЭтЕчТЗжаРэТлЩЯзЊвЦЕчзгЕФЮяжЪЕФСПЮЊ________ЁЃ
ЃЌдђЭтЕчТЗжаРэТлЩЯзЊвЦЕчзгЕФЮяжЪЕФСПЮЊ________ЁЃ
(4)ЩЯКЃНЛЭЈДѓбЇГ№вуЯшЕШбаОПСЫВЛЭЌКЌН№ЛЏКЯЮяДпЛЏввЯЉМгЧт![]() ЕФЗДгІРњГЬШчЯТЭМЫљЪОЃК
ЕФЗДгІРњГЬШчЯТЭМЫљЪОЃК

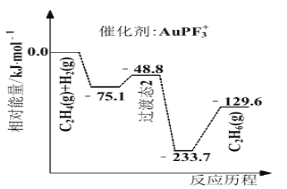
дђ![]() ____________ЃЌДпЛЏввЯЉМгЧтаЇЙћНЯКУЕФДпЛЏМСЪЧ________(бЁЬюЁА
____________ЃЌДпЛЏввЯЉМгЧтаЇЙћНЯКУЕФДпЛЏМСЪЧ________(бЁЬюЁА![]() ЁБЛђЁА
ЁБЛђЁА![]() ЁБ)ЁЃ
ЁБ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com