
用10mL的0.1 mol·L-1BaCl2溶液恰好使同体积的硫酸铁.硫酸锌和硫酸钾三种溶液中的SO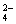 完全沉淀,则这三种溶液的物质的量浓度之比为( )
完全沉淀,则这三种溶液的物质的量浓度之比为( )
A.3:2:2 B.1:2:3 C.1:3:3 D.3:1:1
科目:高中化学 来源: 题型:
已知25 ℃、101 kPa条件下:
4Al(s)+3O2(g)===2Al2O3(s) ΔH=-2 834. 9 kJ·mol-1
4Al(s)+2O3(g)===2Al2O3(s) ΔH=-3 119.1 kJ·mol-1 由此得出的正确结论是( )
①等质量的O2比O3能量低; ②等质量的O2比O3能量高;
③等质量的O3比O2稳定; ④等质量的O2比O3稳定;
A.①③ B.①④ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对实验现象的描述中错误的是
A.向FeCl3和KSCN混合溶液中加入少量KCl固体,溶液血红色变浅
B.向5mL0.1mol/LK2Cr2O7溶液中加入少量NaOH固体,溶液由橙色变为黄色
C.等体积等浓度Na2S2O3和H2SO4混合,温度升高出现浑浊和生成气体速度加快
D.酸性KMnO4溶液中滴加H2C2O4,H2C2O4浓度越大褪色和生成气体速度越快
查看答案和解析>>
科目:高中化学 来源: 题型:
煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.
已知:CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
试回答下列问题:
(1)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有 (选填A、B、C、D、E);
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 2 | 1 | 2 | 3 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
(2)在1L密闭容器中通入10 molCO和10 mol水蒸气,在500℃下经过30s达
到平衡,则30s内CO的平均反应速率为
(3)已知在一定温度下,C(s)+CO2(g)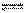 2CO(g)平衡常数K;K的表达式 ;
2CO(g)平衡常数K;K的表达式 ;
C(s)+H2O(g)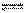 CO(g)+ H2(g)平衡常数K1;
CO(g)+ H2(g)平衡常数K1;
CO(g)+H2O(g)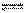 H2(g)+ CO2(g)平衡常数K2;
H2(g)+ CO2(g)平衡常数K2;
则K、K1、K2之间的关系是:
(4)某温度、容积固定容器中,投入一定反应物,对可逆反应
C(s)+ CO2(g)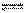 2CO(g)不能判断该反应达到化学平衡状态的是
2CO(g)不能判断该反应达到化学平衡状态的是
A.c(CO2)= c(CO) B.混合气体相对分子质量不变
C.容器中的压强不变 D.v正(CO)= 2v正(CO2) E.c(CO)保持不变
(5)如图1所示,在甲、乙两容器中都充入1mol C和1mol CO2,并使甲、乙
两容器初始容积相等.在相同温度下发生反应C(s)+CO2(g) 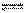 2CO(g),
2CO(g),
并维持反应过程中温度不变.已知甲容器中CO2的转化率随时间变化的
图象如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图象.

查看答案和解析>>
科目:高中化学 来源: 题型:
某500mL溶液中含0.1 mol Fe2+.0.2molFe3+,加入0.2mol铁粉,待Fe3+ 完全还原后,溶液中Fe2+的物质的量浓度为(假设反应前后体积不变) ( )
(提示:2 Fe3+ + Fe =3 Fe2+ )
A.0.4 mol/L B.0.6 mol/L C.0.8 mol/L D. l.0 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用固体烧碱配制500 mL 0.1 mol/L的NaOH溶液。
(1)需称量________g的烧碱固体,固体应放在________中称量。
(2)配制过程中,不需要使用的仪器是(填代号)________。
A.烧杯 B.量筒 C.玻璃棒
D.1000 mL容量瓶 E.漏斗 F.胶头滴管
(3)完成该实验还需要的仪器是________________。
(4)在容量瓶确定溶液体积的过程中,完成后期加入少量水的操作是________________。
(5)为什么容量瓶设计为细颈?
(6)下列操作使得溶液浓度偏高、偏低、不变?
①将取药品的药匙用水洗涤,洗涤液倒入容量瓶中,则所配溶液浓度________。
②定容摇匀后,有少量溶液外流,则所配溶液浓度________。
③未将溶液冷却,直接转移到容量瓶,则引起结果________。
④称量时间过长,所配溶液浓度________。
⑤称量时所用砝码生锈,则引起结果________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com