
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A.25℃,1 LpH=13的NaOH溶液中含有OH-的数目为0.1NA
B.标准状况下,4.6 g NO2和N2O4混合物中含氧原子数为0.3NA
C.标准状况下,6.72 L Cl2与水充分反应,转移电子数为0.3NA
D.0.1 mol/L NaHCO3溶液中,HCO3-、H2CO3和CO32-总数为0.1NA
【答案】A
【解析】
A. 室温下pH=13的NaOH溶液中含有OH-的浓度c(OH-)=0.1 mol/L,由于溶液的体积是1 L,所以其中含有OH-的数目为0.1NA,A正确;
B. 若4.6 g完全是 NO2,其物质的量n(NO2)=![]() =0.1 mol,由于1个NO2分子中含有2个O原子,则0.1 mol该气体中含有O原子的物质的量是0.2 mol,含有的O原子数目为0.2NA;若4.6 g完全是N2O4,则其物质的量n(N2O4)=
=0.1 mol,由于1个NO2分子中含有2个O原子,则0.1 mol该气体中含有O原子的物质的量是0.2 mol,含有的O原子数目为0.2NA;若4.6 g完全是N2O4,则其物质的量n(N2O4)=![]() =0.05 mol,由于1个N2O4分子中含有4个O原子,则0.05 mol该气体中含有O原子的物质的量是0.2 mol,含有的O原子数目为0.2NA,B错误;
=0.05 mol,由于1个N2O4分子中含有4个O原子,则0.05 mol该气体中含有O原子的物质的量是0.2 mol,含有的O原子数目为0.2NA,B错误;
C. Cl2与水的反应为可逆反应,反应物不能完全转化为生成物,所以标准状况下,6.72 L Cl2与水充分反应,转移电子数小于0.3NA,C错误;
D. 只有溶液的浓度,缺少溶液的体积,不能计算微粒的数目,D错误;
故合理选项是A。


科目:高中化学 来源: 题型:
【题目】氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制流程:

依照上述流程回答以下问题:
(1)混合①中发生反应的化学方程式为_______。
(2)操作Ⅱ和操作Ⅲ的名称分别是_______、_______。操作Ⅲ一般适用于分离____________混合物。〔选填编号〕
a、固体和液体b、固体和固体c、互不相溶的液体d、互溶的液体
(3)混合②中加入Na2SO3的目的是_______。
(4)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸〔工业氢溴酸〕带有淡淡的黄色。因此甲乙两同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,那么用于证明该假设所用的试剂的名称为_______。乙同学假设工业氢溴酸呈淡黄色是因为________,其用于证明该假设所用的试剂的化学式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷((POCl3)可用于制备增塑剂,常温下为无色透明液体,易挥发,易水解。一中化学兴趣小组探究制备POCl3所需的装置如下图所示:

反应原理:PCl3+Cl2+H2O![]() POCl3+2HCl(PC13常温下为液态,易挥发)。
POCl3+2HCl(PC13常温下为液态,易挥发)。
(1)仪器3的名称是 _________,仪器2中装入的物质为______,仪器I的作用是_____.
(2)请选择上述必要装置并组装,用小写字母连接:________________________。
(3)开始通入氯气。同时慢慢滴加水,控制氯气和水的质量比在3.94左右,理由是:________________________.
(4)上述装置有一处不足,请指岀该不足:__________________________.
(5)上述反应剩余PCl3可以继续通入Cl2,再和P4O10反应,也可以产生的POC13 .。 写出该反应的化学方程式:__________________________________ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向10 mL 0.1 mol/L醋酸溶液中加水稀释后,下列说法正确的是( )
A. 溶液中离子的数目减小
B. 再加入CH3COONa固体能促进醋酸的电离
C. 醋酸的电离程度增大,c(H+)亦增大
D. 溶液中c(CH3COO-)/c(CH3COOH)c(OH-)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:① X、Y、Z、W、R、Q为原子序数依次增大的短周期元素。X 是所有元素中原子半径最小的元素,Y是形成化合物种类最多的元素,W的最外层电子数是次外层电子数的3倍,Q与W同主族,Y、R原子的最外层电子数之和等于Z的最外层电子数。
②莱纳斯·卡尔·鲍林在1932年提出electronegativity作为元素原子在化合物某种性质的标度,electronegativity的大小可以判断元素金属性与非金属性强弱,下表列出部分短周期元素的Electronegativity的值。
元素 | X | Y | Z | W | R | Q |
electronegativity | 2.1 | 2.5 | 3.0 | 3.5 | 0.9 | 2.5 |
元素 | Mg | Li | Al | Cl | P | Be |
electronegativity | 1.2 | 1.0 | 1.5 | 3.0 | 2.1 | 1.5 |
请回答下列问题(涉及X、Y、Z、W、R、Q时,用元素符号表示):
(1)根据上表给出的数据,可知元素的electronegativity越大,__(填“金属性”或“非金属性”)越强。
(2)元素Q在周期表中的位置为_________。
(3)W、R、Q单核简单离子半径由大到小排列顺序为______。
(4)元素X、Z、W之间能形成多种10电子微粒,请写出反应物和产物均为X、Z、W之间形成的10电子微粒的一个离子方程式______________。
(5)一种由元素W、R组成的白色固体化合物,其电子式为_______________。
(6)试比较稳定性:X2W_____ X2Q;沸点:X2W_____ X2Q (填“<”或“>”)。
(7)元素 X、Y、Z、W、R、Q中的两种元素可形成原子个数比为1∶2的共价化合物,则这两种元素的原子序数之差不可能是_________。
A.2 B.4 C.5 D.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有14.4 g CO和CO2的混合气体,在标准状况下所占的体积约为8.96 L。回答下列问题:
(1)该混合气体的平均摩尔质量:_________________________。
(2)混合气体中碳原子的个数:_________________________
(用NA表示阿伏加德罗常数的值)。
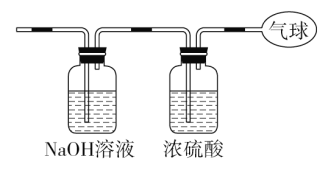
(3)将混合气体依次通过如图装置,最后收集在气球中。
①气球中收集到的气体摩尔质量:_______________________;
②标况下气球中收集到的气体的体积为___________________;
③气球中收集到的气体的电子总数为_____________________
(用NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学实验中,通常利用如图所示的装置进行喷泉实验,来验证气体的“溶解性”,下列有关说法不正确的是

A.用滴管加入液体后,由于气体的“溶解”,使瓶内压强减小,导致瓶内压强小于外界压强,从而形成喷泉
B.选用合适的溶液,CO2也能做喷泉实验
C.HCl、NH3和SO2均能用该装置做喷泉实验
D.用NO2气体做喷泉实验,烧瓶中将充满稀硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行如下反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H=-764.5kJ·mol-1,达到平衡后,为提高反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+2CO2(g) △H=-764.5kJ·mol-1,达到平衡后,为提高反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度
B.升高温度同时充入氮气
C.加催化剂同时增大压强
D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组拟设计实验探究乙醇的还原性及产物,装置如图所示。

已知:几种有机物的部分物理性质如表所示:
有机物 | 乙醇 | 乙酸 | 乙醛 |
溶解性 | 易溶于水和乙酸、乙醛 | 易溶于水和乙醇、乙醛 | 易溶于水和乙醇、乙酸 |
沸点 | 78.5 | 117.9 | 20.8 |
(1)为了获得比较稳定的气流,A装置还缺少一种仪器是____(填仪器名称)。A装置使用____(填“冷水浴”或“热水浴”)。
(2)当B中氧化铜完全反应后,正确的操作排序为____(填序号)。
①从C装置中取出试管 ②继续通入乙醇蒸气至B装置中的试管冷却
③熄灭酒精灯 ④从A装置中取出烧瓶
(3)分离和提纯产品。实验完毕后,取少量粗产品于试管,滴加紫色石蕊溶液,溶液变红色,则粗产品中含有___(填化学式)。对粗产品进行____操作(填名称)可以获得较纯的乙醛。
(4)已知:Cu2O呈红色,在酸性条件下发生反应为Cu2O+2H+=Cu+Cu2++H2O。乙同学取少量B中红色粉末于试管,滴加稀硫酸溶液,观察到____(填实验现象),证明红色产物中含有Cu2O。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com